
| A”¢Įņ»ÆÄĘÅØČÜŅŗÓŠ³ōĪ¶ |
| B”¢¼ÓČČĀČ»ÆĢśČÜŅŗŃÕÉ«±äÉī |
| C”¢ĢśŌŚ³±ŹŖµÄ»·¾³ĻĀÉśŠā |
| D”¢“æ¼īČÜŅŗČ„ÓĶĪŪ |


 Õć“óÓÅѧŠ”ѧğ¼¶ĻĪ½Ó½Ż¾¶Õć½“óѧ³ö°ęÉēĻµĮŠ“š°ø
Õć“óÓÅѧŠ”ѧğ¼¶ĻĪ½Ó½Ż¾¶Õć½“óѧ³ö°ęÉēĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
 ČēĶ¼ĖłŹ¾£¬ŌŚČŻĘ÷A”¢BÖŠ·Ö±š×°ÓŠ20”ęµÄĖ®50mL£¬ŹŌ¹ÜC”¢DĻąĮ¬ĶØ£¬ĘäÖŠ“ęŌŚĻĀĮŠĘ½ŗā£ŗ2NO2£Øg£©?N2O4£Øg£©”÷H=-57kJ/mol£»µ±ĻņAÖŠ¼ÓČė2gæĮŠŌÄĘŹ±£ŗ
ČēĶ¼ĖłŹ¾£¬ŌŚČŻĘ÷A”¢BÖŠ·Ö±š×°ÓŠ20”ęµÄĖ®50mL£¬ŹŌ¹ÜC”¢DĻąĮ¬ĶØ£¬ĘäÖŠ“ęŌŚĻĀĮŠĘ½ŗā£ŗ2NO2£Øg£©?N2O4£Øg£©”÷H=-57kJ/mol£»µ±ĻņAÖŠ¼ÓČė2gæĮŠŌÄĘŹ±£ŗ²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
| AӢ1mol | BӢ2mol |
| CӢ2.5mol | DӢ3mol |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
| A”¢»ŲŹÕĘäÖŠµÄŹÆÄ«µē¼« |
| B”¢·ĄÖ¹µē³ŲÖŠÉųŠ¹µÄµē½āŅŗøÆŹ“ĘäĖūĪļĘ· |
| C”¢ĄūÓƵē³ŲĶāæĒµÄ½šŹō²ÄĮĻ |
| D”¢·ĄÖ¹µē³ŲÖŠ¹Æ”¢ļÓŗĶĒ¦µČÖŲ½šŹōĄė×Ó¶ŌĶĮČĄŗĶĖ®Ō“µÄĪŪČ¾ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
| A”¢0.1mol/LCH3COOHČÜŅŗ¼ÓĖ®Ļ”ŹĶ£¬ČÜŅŗÖŠc£ØOH-£©Ōö“ó | ||
B”¢½«NaOHŗĶ°±Ė®ČÜŅŗø÷Ļ”ŹĶŅ»±¶£¬Į½ÕßµÄOH-ÅØ¶Č¾ł¼õÉŁµ½ŌĄ“µÄ
| ||
| C”¢ĻąĶ¬ÅØ¶ČµÄHClŗĶCH3COOH£¬Į½ČÜŅŗÖŠc£ØH+£©ĻąĶ¬ | ||
| D”¢ČōHA”¢HB¾łĪŖČõĖį£¬ĖįŠŌHA£¾HB£¬ŌņĻąĶ¬Ģõ¼žĻĀ£¬ČÜŅŗµÄpH“óŠ”ĪŖNaA£¾NaB |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
| ĪļÖŹ | ŌÓÖŹ | ĖłŃ”ŹŌ¼Į | Ąė×Ó·½³ĢŹ½ |
| NaClČÜŅŗ | Na2CO3 | ||
| Mg·Ū | Al ·Ū | ||
| FeCl2ČÜŅŗ | FeCl3 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
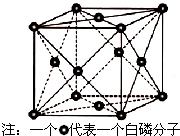 VA×åµÄµŖ”¢Į×”¢Éé£ØAs£©µČŌŖĖŲµÄ»ÆŗĻĪļŌŚæĘŃŠŗĶÉś²śÖŠÓŠŠķ¶ąÖŲŅŖÓĆĶ¾£¬Ēė»Ų“šĻĀĮŠĪŹĢā£®
VA×åµÄµŖ”¢Į×”¢Éé£ØAs£©µČŌŖĖŲµÄ»ÆŗĻĪļŌŚæĘŃŠŗĶÉś²śÖŠÓŠŠķ¶ąÖŲŅŖÓĆĶ¾£¬Ēė»Ų“šĻĀĮŠĪŹĢā£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
A”¢ ÖʱøĒāŃõ»ÆŃĒĢś²¢¹Ū²ģĘäŃÕÉ« |
B”¢ ÓĆÅØĮņĖįøÉŌļCl2 |
C”¢ ¼ģ²é×°ÖĆĘųĆÜŠŌ |
D”¢ ĄūÓĆÅÅæÕĘų·ØŹÕ¼ÆCO2 |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com