
| A. | 离子半径:A2->D->B+ | |
| B. | 元素B、C的最高价氧化物对应水化物的碱性:B>C | |
| C. | 简单氢化物的稳定性:A>D | |
| D. | A与B形成的化合物中可能既有离子键又有共价键 |
分析 A、D的最低价离子分别为A2-、D-,则A为第ⅥA族元素,D为ⅦA族元素;B+和D-具有相同的电子层结构,则B在D的下一周期,则B为Na元素,D为F元素,B、C同周期,则A为O元素,元素C的简单离子是同周期元素中半径最小的,应为Al,结合元素在周期表中的位置以及元素周期律知识解答该题.
解答 解:A、D的最低价离子分别为A2-、D-,则A为第ⅥA族元素,D为ⅦA族元素;B+和D-具有相同的电子层结构,则B在D的下一周期,则B为Na元素,D为F元素,B、C同周期,则A为O元素,元素C的简单离子是同周期元素中半径最小的,应为Al,
A.O2-、Na+、F-具有相同的核外电子排布,离子的核电荷数越大,半径越小,故A正确;
B.金属性Na>Al,元素的金属性越强,对应的最高价氧化物对应水化物的碱性越强,故B正确;
C.非金属性O<F,元素的非金属性越强,对应的氢化物越稳定,故C错误;
D.A与B可形成过氧化钠,能既有离子键又有共价键,故D正确.
故选C.
点评 本题考查原子结构与元素周期律的关系,为高考常见题型,侧重于学生的分析能力的考查,题目难度不大,本题的关键是根据原子结构特点正确推断元素的种类.


 寒假乐园北京教育出版社系列答案
寒假乐园北京教育出版社系列答案科目:高中化学 来源: 题型:选择题
| A. | O2与Cu反应生成CuO,S与Cu反应生成CuS | |
| B. | CaC2能水解:CaC2+2H2O=Ca(OH)2+C2H2↑,则Al4C3也能水解:Al4C3+12H2O═4Al(OH)3+3CH4↑ | |
| C. | 根据化合价Fe3O4可表示为FeO•Fe2O3,则Pb3O4也表示为PbO•Pb2O3 | |
| D. | SO2通入BaCl2溶液不产生沉淀,则SO2通入Ba(NO3)2溶液不产生沉淀 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 氧化亚铜(Cu2O)作为一种重要的无机化工原料,在涂料、有色玻璃和催化剂等领域有着广泛的用途.回答下列问题:
氧化亚铜(Cu2O)作为一种重要的无机化工原料,在涂料、有色玻璃和催化剂等领域有着广泛的用途.回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在密闭容器中加入l.5mol H2和0.5molN2,充分反应后可得到NH3分子数为NA | |
| B. | 100ml 1mol/L的FeCl3溶液中Fe3+数目为0.1NA | |
| C. | 标准状况下,22.4L的CCl4中含有的CCl4分子数为NA | |
| D. | 常温常压下,92g的NO2和N2O4混合气体含有的原子数为6NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 序号 | ① | ② | ③ | ④ |
| 溶液 | CH3COONa | NaHCO3 | Na2CO3 | NaClO |
| pH | 8.8 | 9.7 | 11.6 | 10.3 |
| A. | 将等浓度的CH3COOH和HClO溶液,pH小的是HClO | |
| B. | Na2CO3和NaHCO3溶液中粒子种类不同 | |
| C. | 溶液水的电离程度①>②>④>③ | |
| D. | NaHCO3溶液中,c(Na +)=c(CO3 2-)+c(HCO3-)+c(H2CO3) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
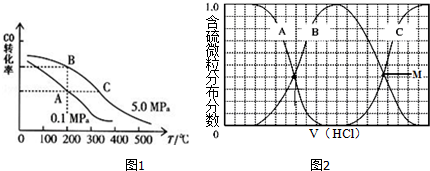
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温下,正丁烷的燃烧热为-2878.0kJ/mol | |
| B. | 相同质量的丙烷和正丁烷分别完全燃烧,前者需要的氧气少产生的热量也多 | |
| C. | 常温下,CO的燃烧热为283.0 kJ/mol | |
| D. | 人类利用的能源都是通过化学反应获得的 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 被氧化和被还原的元素分别为铜和氮 | |
| B. | 当产生0.2mol气体时,转移电子为0.6mol | |
| C. | 被还原的CuO占参与反应CuO的$\frac{1}{2}$ | |
| D. | 参加反应的氧化剂和还原剂的物质的量之比为3:2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 加入溶液 | ①适量铋酸钠溶液 | ②过量的双氧水 | ③适量KI淀粉溶液 |
| 实验现象 | 溶液呈紫红色 | 紫红色消失,产生气泡 | 溶液变成蓝色 |
| A. | I2,H2O2,KMnO4,NaBiO3 | B. | H2O2,I2,NaBiO3,KMnO4 | ||
| C. | NaBiO3,KMnO4,H2O2,I2 | D. | KMnO4,NaBiO3,I2,H2O2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com