
���� I����1���÷�Ӧ��CuԪ�ػ��ϼ���+2�۱�Ϊ0�ۡ�SԪ�ػ��ϼ���-2�۱�Ϊ+4�ۣ�OԪ�ػ��ϼ���0�۱�Ϊ-2�ۣ��õ��ӻ��ϼ۽��͵ķ�Ӧ������������
��2�����������ж�����ֱ���ſգ���������������ܺͼ�Һ��Ӧ�����Σ��������β��ȶ��ױ��������������Σ�����������С�����
��3��¯���м������ϡ���ᣬFeO��Fe2O3��Al2O3��ϡ���ᷴӦ����FeCl2��FeCl3��AlCl3��SiO2����Ӧ��Ȼ����ˣ�����Һ�м�����������FeCl2ת��ΪFeCl3��Ȼ������Һ�м���NaOH��Һ��FeCl3��Ӧ����Fe��OH��3������AlCl3��Ӧ����NaAlO2��Ȼ����˵õ�Fe��OH��3����Fe��OH��3���յõ�Fe2O3��
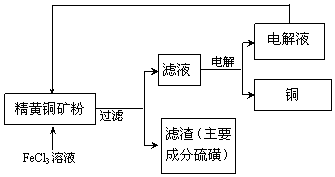
II����ͭ����м����Ȼ�����Һ��Ȼ����˵õ�S��˵�����߷�Ӧ����S�����ͭ������ԭ�����Ȼ����������������߷�Ӧ����ʽΪCuFeS2+4Fe3+=Cu2++5Fe2++2S������Һ���õ�Cu�͵������Һ��������ͭ���ӵõ�������Cu����������������ʧ�������������ӣ�
��4��CuFeS2��FeCl3��Һ��Ӧ�����������ӡ�ͭ���Ӻ�S��
��5������������ͼ�вμӷ�Ӧ�����ɵ���ѭ�����ã�
��6������ʯī�缫�����Һ����������������ʧ�������������ӣ�
��7��KSP��PbCl2��=1��10-5=c��Pb2+����c2��C1-����c��Pb2+��=$\frac{{K}_{sp}}{{c}^{2}��C{l}^{-}��}$��
��� �⣺I����1���÷�Ӧ��CuԪ�ػ��ϼ���+2�۱�Ϊ0�ۡ�SԪ�ػ��ϼ���-2�۱�Ϊ+4�ۣ�OԪ�ػ��ϼ���0�۱�Ϊ-2�ۣ��õ��ӻ��ϼ۽��͵ķ�Ӧ���������������Ը÷�Ӧ����������CuFeS2��O2��
�ʴ�Ϊ��CuFeS2��O2��
��2��A�����������ж�������ֱ�Ӹ߿��ŷţ��������Ⱦ������Ӧ���ü�Һ���գ���A����
B�����������ˮ��Ӧ���ɵ����������Դ���̼�ᣬ���Զ��������ܺʹ�����Һ��Ӧ�����������ƣ������ô�����Һ�����Ʊ��������ƣ���B��ȷ��
C���������������������һˮ�ϰ��Ǽ���߷�Ӧ��������泥������ð�ˮ���պ��پ������Ʊ�����泥���C��ȷ��
D���������Դ��������ᣬ���Զ��������BaCl2����Ӧ�������ö���������Ȼ�����Һ��ȡBaSO3����D����
��ѡBC��
��3��¯���м������ϡ���ᣬFeO��Fe2O3��Al2O3��ϡ���ᷴӦ����FeCl2��FeCl3��AlCl3��SiO2����Ӧ��Ȼ����ˣ�����Һ�м�����������FeCl2ת��ΪFeCl3��Ȼ������Һ�м���NaOH��Һ��FeCl3��Ӧ����Fe��OH��3������AlCl3��Ӧ����NaAlO2��Ȼ����˵õ�Fe��OH��3����Fe��OH��3���յõ�Fe2O3������û���漰�IJ���ΪC���ʴ�Ϊ��C��
II����ͭ����м����Ȼ�����Һ��Ȼ����˵õ�S��˵�����߷�Ӧ����S�����ͭ������ԭ�����Ȼ����������������߷�Ӧ����ʽΪCuFeS2+4Fe3+=Cu2++5Fe2++2S������Һ���õ�Cu�͵������Һ��������ͭ���ӵõ�������Cu����������������ʧ�������������ӣ�
��4��CuFeS2��FeCl3��Һ��Ӧ�����������ӡ�ͭ���Ӻ�S�����ӷ���ʽΪCuFeS2+4Fe3+=Cu2++5Fe2++2S
���ʴ�Ϊ��CuFeS2+4Fe3+=Cu2++5Fe2++2S��
��5��CuFeS2��FeCl3��Һ��Ӧ����FeCl2��CuCl2��Һ��������Һ�õ�Cu��Fe3+������ʱ��Ӧ����FeCl3�����Կ���ѭ�����õ�������FeCl3��
�ʴ�Ϊ��FeCl3��
��6��ʯī�缫�����Һ��������ʧ���ӷ���������Ӧ������ʧ���������������Ӵ��������ӣ���������������������ʧ�������������ӣ���缫��ӦʽΪ��Fe2+-e-=Fe3+���ʴ�Ϊ��Fe2+-e-=Fe3+��
��7����֪�����ӵ�Ũ��c��Cl-��=2mol•L-1��KSP��PbCl2��=1��10-5=c��Pb2+����c2��Cl-������Pb2+���ʵ���Ũ��c��Pb2+��=��7��KSP��PbCl2��=1��10-5=c��Pb2+����c2��C1-����c��Pb2+��=$\frac{{K}_{sp}}{{c}^{2}��C{l}^{-}��}$=$\frac{1��1{0}^{-5}}{2��2}$mol/L=2.5��10-6mol/L��
�ʴ�Ϊ��2.5��10-6��
���� ���⿼�������ʵ��Ʊ�������ƣ�Ϊ��Ƶ���㣬��Ŀ�漰������ԭ��Ӧ��ʵ�鷽����ơ����ԭ����Ӧ�á��ܶȻ����йؼ���ȣ����ضԻ�ѧ���������뼼�ܡ���ѧ���������Ŀ��飬��Ҫѧ���߱���ʵ�Ļ��������������������Ŀ�Ѷ��еȣ�


 ��У���˳�̾�ϵ�д�
��У���˳�̾�ϵ�д� ��У���һ��ͨϵ�д�
��У���һ��ͨϵ�д� �γ̴����Ծ�����100��ϵ�д�
�γ̴����Ծ�����100��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ʵ�� ��� | Ũ�� mol•L-1 �¶ȣ��棩ʱ�䣨 min�� | 0 | 10 | 20 | 30 | 40 | 50 | 60 |
| 1 | 800 | 1.0 | 0.80 | 0.67 | 0.57 | 0.50 | 0.50 | 0.50 |
| 2 | 800 | c2 | 0.60 | 0.50 | 0.50 | 0.50 | 0.50 | 0.50 |
| 3 | 800 | c3 | 0.92 | 0.75 | 0.63 | 0.60 | 0.60 | 0.60 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | S��g��+O2��g��=SO2��g��+Q3 Q3��297.16 kJ | |
| B�� | ��б���������Ϊͬ���칹�� | |
| C�� | �����µ�б����������ȶ� | |
| D�� | ��б��ת��Ϊ������ķ�Ӧ�����ȷ�Ӧ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��C��ʾ�÷�Ӧ������Ϊ0.03mol/��L•s�� | |
| B�� | �ﵽƽ�⣬��÷ų�����Ϊx��kJ����x=Q | |
| C�� | �����������ٳ���1��mol��C�����´ﵽƽ�⣬A������������ֲ��� | |
| D�� | �������¶ȣ���V���棩����V��������С��ƽ�������ƶ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �Ȼ����Ba��OH��2•8H2O��Ӧ | B�� | ������ˮ��Ӧ | ||
| C�� | пƬ��ϡ���ᷴӦ | D�� | �����������������ķ�Ӧ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��H��0��ʾ���ȷ�Ӧ����H��0��ʾ���ȷ�Ӧ | |
| B�� | �Ȼ�ѧ����ʽ�еĻ�ѧ������ֻ��ʾ���ʵ����������Ƿ��� | |
| C�� | 1 mol H2SO4��1 mol Ba��OH��2��Ӧ����BaSO4����ʱ�ų������������к��� | |
| D�� | 1 mol H2��0.5 mol O2��Ӧ�ų����Ⱦ���H2��ȼ���� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com