解答:
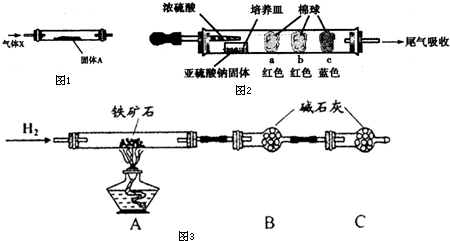
解:I.A.无水硫酸铜和水反应生成蓝色的五水硫酸铜,故固体A为无水硫酸铜时,可以检验气体X中是否含有水蒸气,故A正确;
B.灼热的铜和氧气反应生成氧化铜,而而氮气性质稳定和铜不反应,故B正确;
C.加热氯化铁晶体,氯化铁水解得到氢氧化铁,得不到氯化铁,应在氯化氢气流中加热,故C错误;
D.氨气和氧气在铂催化下生成一氧化氮,一氧化氮和氧气反应生成二氧化氮二氧化氮为红棕色,故D正确;
故答案为:C;
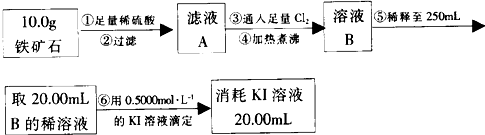
Ⅱ.a.红色棉球变白,微热后又恢复红色,说明二氧化硫使品红溶液褪色,则棉球上滴有品红溶液,该实验说明二氧化硫具有漂白性,但其漂白性不稳定,
b.二氧化硫属于酸性氧化物,能和NaOH溶液反应生成亚硫酸钠和水,导致溶液碱性减弱,所以溶液变为白色,离子方程式为:SO
2+2OH
-=SO
32-+H
2O,
c.碘遇淀粉试液变蓝色,二氧化硫具有还原性,碘具有氧化性,二者反应生成氢碘酸和硫酸,所以棉球变为白色,离子方程式为:SO
2+I
2+2H
2O=4H
++SO
42-+2I
-,该实验说明二氧化硫具有还原性,
故答案为:
| 棉球 | 棉球上滴加的试剂 | 实验现象 |
解释和结论 |
| a | 品红试液
| | |
| b | | | 离子方程式:2OH-+SO2=SO32-+H2O |
| c | 含淀粉的碘水
| | 结论:该气体具有 还原 性 |
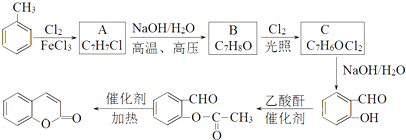
Ⅲ.(1)氢气中混有氧气时点燃会产生爆炸,为防止安全事故发生,待C装置出口处H
2验纯后,点燃A处酒精灯,故答案为:待C装置出口处H
2验纯后;
(2)测的反应后装置B增重1.35g,根据反应的实质,增加的是水的质量,所以氧元素的质量分数是:
×100%=24%,
故答案为:24%;
(3)向铁矿石中加入硫酸,酸化反应生成硫酸的铁盐溶液,还存在过量的硫酸溶液,加入过量的氯气,煮沸的作用是赶走溶液中溶解的过量的Cl
2,否则会影响与KI的反应,带来实验误差,
故答案为:赶走溶液中溶解的过量的Cl
2;
(4)过滤需要的玻璃仪器有:烧杯、漏斗、玻璃棒,若稀释到250mL时采用的仪器有:烧杯、玻璃棒、胶头滴管、250mL容量瓶,则两个过程都需要的玻璃仪器有:烧杯、玻璃棒,故答案为:烧杯、玻璃棒;
(5)a.滴定管用蒸馏水洗涤后再用待装液润洗,否则会导致测量结果偏大,故正确;
b.锥形瓶不需要用待测液润洗,如果润洗,会导致测量结果偏大,故正确;
c.碘水为黄色,三价铁离子也是黄色溶液,滴定过程中需加指示剂,故错误;
故选c;
(6)由于所取溶液(含Fe
3+)的体积与消耗KI溶液的体积相等,反应的方程式为2Fe
3++2I
-=2Fe
2++I
2,结合方程式可知,c(Fe
3+)=c(KI)=0.5mol?L
-1,所以铁元素的百分含量为:
| 0.5mol/L×0.25L×56g/mol |
| 10g |
×100%=70%,
铁的质量分数是70%,氧元素的质量分数是24%,所以100g铁矿石中,铁元素的质量是70g,氧元素质量是24g,铁元素和氧元素的物质的量比为:
:
=5:6,铁的氧化物的化学式为:Fe
5O
6,
故答案为:Fe
5O
6.




 与乙酸酐(
与乙酸酐(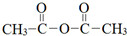 )反应,除生成
)反应,除生成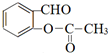 外,另一种产物是
外,另一种产物是

 为测定气球内的气体成分,有学生用超薄材料的气球按如图装置进行实验,开始时气球沉于烧杯底部,打开开关后,过一会儿气球从烧杯底部慢慢浮起,最后悬于烧杯口.气球内可能的气体是( )
为测定气球内的气体成分,有学生用超薄材料的气球按如图装置进行实验,开始时气球沉于烧杯底部,打开开关后,过一会儿气球从烧杯底部慢慢浮起,最后悬于烧杯口.气球内可能的气体是( )
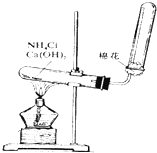 如图是实验室制取氨气的装置图,请回答下列问题:
如图是实验室制取氨气的装置图,请回答下列问题: