
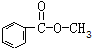 属于酯类的同分异构体还有4种;
属于酯类的同分异构体还有4种;| A. | ①② | B. | ③④ | C. | ①③ | D. | ②④ |
分析 ①C4H8O2属于酯类的同分异构体,为饱和一元酯,根据形成酯的酸和醇的种类来确定;
②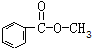 属于酯类,根据形成酯的酸和醇或酚的种类来确定;
属于酯类,根据形成酯的酸和醇或酚的种类来确定;
③C7H8O遇氯化铁溶液呈紫色,故分子中含有1个苯环,含有酚羟基,则还含有1个甲基,结合甲基与酚羟基的位置关系解答;
④C5H10O能发生银镜反应,说明此物质为戊醛,C5H10O可以看做丁基代替HCHO中的H原子,所以,丁基有几种,C5H10O就有几种同分异构体.
解答 解:①C4H8O2属于酯类的同分异构体,为饱和一元酯,可以为甲酸与丙醇形成的酯,甲酸只有1种结构,丙醇可以可知1个-OH取代丙烷中的H原子,丙烷分子中有2种H原子,形成的丙醇有2种,形成的酯有2种,可以为乙酸与乙醇形成的酯,只有乙酸乙酯1种,为丙酸与甲醇形成的酯,注意丙酸甲酯1种,故C4H8O2属于酯类的同分异构体共有4种,故①正确;
②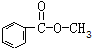 属于酯类,可以为甲酸与甲基苯酚形成的酯,甲酸只有1种结构,甲基苯酚有3种:邻甲基苯酚、间甲基苯酚、对甲基苯酚,形成的酯有3种,可以为甲酸与苯甲醇形成的酯,甲酸只有1种结构,苯甲醇只有1种结构,故
属于酯类,可以为甲酸与甲基苯酚形成的酯,甲酸只有1种结构,甲基苯酚有3种:邻甲基苯酚、间甲基苯酚、对甲基苯酚,形成的酯有3种,可以为甲酸与苯甲醇形成的酯,甲酸只有1种结构,苯甲醇只有1种结构,故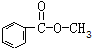 属于酯类的同分异构体还有4种,故②错误;
属于酯类的同分异构体还有4种,故②错误;
③芳香族化合物A的分子式为C7H8O,故A含有1个苯环,遇FeCl3溶液可发生显色反应,含有酚羟基,故还含有1个甲基,甲基与酚羟基有邻、间、对三种位置关系,故符合条件的A的结构有3种,故③正确;
④C5H10O能发生银镜反应,说明此物质为戊醛,C5H10O可以看做丁基代替HCHO中的H原子,丁基有四种,所以C5H10O就有四种同分异构体,故④错误;
故选C.
点评 本题考查同分异构体的种类,根据官能团异构和位置异构和碳链异构来综合分析同分异构体的种数,难度不大,有利于培养学生的逻辑推理能力.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 可用25 mL碱式滴定管量取20.00 mL KMnO4溶液 | |
| B. | 除去乙醇中少量的乙酸:加足量生石灰,蒸馏 | |
| C. | 用苯萃取溴水中的溴,分液时有机层从分液漏斗的下口放出 | |
| D. | 向SO2水溶液中滴加盐酸酸化的BaCl2溶液,有白色沉淀生成,说明BaSO3难溶于盐酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该溶液中不一定含有Na+ | |
| B. | 该溶液中肯定含有NH4+、SO42-、CO32-、NO3- | |
| C. | 该溶液中一定不含NO3- | |
| D. | 该溶液中一定含Na+,且c(Na+)≥0.1 mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氮族元素的氢化物中,NH3的沸点最低 | |
| B. | 非金属性:Cl>Br>I,所以酸性:HCl>HBr>HI | |
| C. | Na和Cs同主族,所以NaCl和CsCl晶胞的结构相同 | |
| D. | O和S同主族,所以CO2和CS2都是直线型非极性分子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1mol•L-1的FeCl3 溶液中Fe3+个数少于NA | |
| B. | 46gNO2 中含有N原子数为NA | |
| C. | 17g羟基(-OH)与17gOH-所含电子数均为10 NA | |
| D. | 8.4g Fe与标准状况下3.36LCl2充分反应,转移电子数为0.3 NA,生成FeCl2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ;
; ;
;查看答案和解析>>
科目:高中化学 来源: 题型:解答题
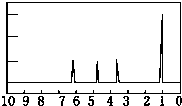
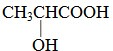 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com