
| 滴定次数 | 待测液体积 (mL) | 标准KMnO4溶液体积(mL) | |
| 滴定前读数 | 滴定后读数 | ||
| 第一次 | 25.00 | 0.50 | 20.40 |
| 第二次 | 25.00 | 3.00 | 23.00 |
| 第三次 | 25.00 | 4.00 | 24.10 |
| 难溶物 | AgCl | AgBr | AgCN | Ag2CrO4 | AgSCN |
| 颜色 | 白 | 浅黄 | 白 | 砖红 | 白 |
| Ksp | 1.77×10-10 | 5.35×10-13 | 1.21×10-16 | 1.12×10-12 | 1.0×10-12 |
分析 (1)根据c(待测)=$\frac{c(标准)×V(标准)}{V(待测)}$分析不当操作对V(标准)的影响,以此判断浓度的误差;
(2)①根据高锰酸钾溶液具有强氧化性选择滴定管类型;根据滴定结束前溶液为无色,滴定结束时溶液变成紫红色偏大滴定终点;
②先判断滴定数据的有效性,然后计算出消耗标准液的平均体积,再根据c(待测)=$\frac{c(标准)×V(标准)}{V(待测)}$计算出待测液的浓度;
(3)滴定结束时,继续滴加滴定剂,滴定剂和指示剂反应生成有明显颜色变化的沉淀,保证滴定剂和被滴定物完全反应.
解答 解:(1)A.滴定终点读数时,俯视滴定管刻度,其他操作正确,导致V(标准)偏小,根据c(待测)=$\frac{c(标准)×V(标准)}{V(待测)}$分析,测定结果偏低,故A错误;
B.盛装NaOH溶液的锥形瓶用蒸馏水洗过,未用NaOH溶液润洗,此操作正确,不影响测定结果,故B错误;
C.酸式滴定管用蒸馏水洗净后,未用标准盐酸润洗,导致标准液浓度减小,导致V(标准)增大,根据c(待测)=$\frac{c(标准)×V(标准)}{V(待测)}$分析,测定结果偏高,故C正确;
D.滴定前,滴定管尖嘴有气泡,滴定后气泡消失,导致V(标准)增大,根据c(待测)=$\frac{c(标准)×V(标准)}{V(待测)}$分析,测定结果偏高,故D正确;
故选CD;
(2)①高锰酸钾溶液具有强氧化性,能够氧化碱式滴定管的橡胶管,所以应该使用酸式滴定管盛装高锰酸钾溶液;滴定结束前混合液为无色,滴定结束时混合液变成了紫红色,所以滴定终点现象为:锥形瓶中溶液由无色变为紫红色,且半分钟内不褪色,
故答案为:酸;锥形瓶中溶液由无色变为紫红色,且半分钟内不褪色;
②三次滴定消耗标准液体积为19.90mL,20.00mL,20.10mL,三次数据均有效,消耗标准液的平均体积为:$\frac{19.90mL+20.00mL+20.10mL}{3}$=20.00mL,高锰酸钾的物质的量为:0.10mol/L×0.020L=0.0020mol,由2KMnO4+5H2C2O4+3H2SO4=K2SO4+10CO2↑+2MnSO4+8H2O可知,n(H2C2O4)=$\frac{5}{2}$n(KMnO4)=0.005mol,待测液草酸的物质的量浓度为:$\frac{0.005mol}{0.025L}$=0.2 mol•L-1;
故答案为:0.2 mol•L-1;
(3)若用AgNO3去滴定NaSCN溶液,可选用的滴定指示剂的物质的溶解度应比AgSCN大,且现象明显,应为Na2CrO4,混合物中有砖红色沉淀生成,
故答案为:D.
点评 本题考查了酸碱中和滴定,注意掌握中和滴定的操作方法及误差分析方法和技巧,该题难易适中,注重灵活性,侧重对学生能力的培养和解题方法的指导和训练,有利于培养学生的逻辑思维能力和严谨的规范实验操作能力.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源:2016-2017学年陕西省高一上第一次月考化学卷(解析版) 题型:选择题
质量相等的下列物质中,含分子数最多的是
A.CH4 B.O2 C.NH3 D.CO2
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
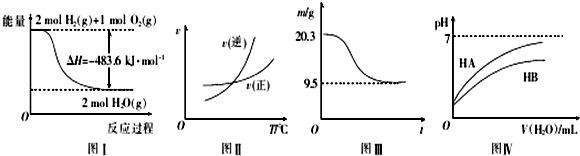
| A. | 图I表示H2与O2发生反应过程中的能量变化,则H2的燃烧热△H=-241.8 kJ.mol-1 | |
| B. | 图Ⅱ表示某可逆反应正、逆反应速率随温度的变化,则该反应的正反应是放热反应 | |
| C. | 图Ⅲ表示0.1 mol MgCl2•6H2O在空气中充分加热时固体质量随时间的变化 | |
| D. | 图Ⅳ表示常温下,稀释HA、HB两种酸的稀溶液时,溶液pH随加水量的变化,则NaA溶液的pH大于同浓度NaB溶液的pH |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
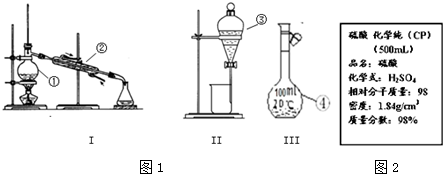
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
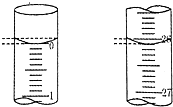 某学生用已知物质的量浓度的盐酸来滴定未知物质的量浓度的氢氧化钠溶液时,选择酚酞作指示剂.请填写下列空白:
某学生用已知物质的量浓度的盐酸来滴定未知物质的量浓度的氢氧化钠溶液时,选择酚酞作指示剂.请填写下列空白:| 滴定次数 | 待测氢氧化钠溶液的体积/mL | 0.1000mol/L盐酸的体积(mL) | |
| 滴定前刻度 | 滴定后刻度 | ||
| 第一次 | 25.00 | 0.00 | 26.11 |
| 第二次 | 25.00 | 1.56 | 30.30 |
| 第三次 | 25.00 | 0.22 | 26.31 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
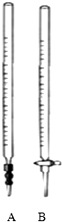 实验室中有一瓶含有一定量杂质的烧碱样品,某学生用中和滴定法测定烧碱的纯度,若烧碱中含有与酸不反应的杂质,请根据实验回答:
实验室中有一瓶含有一定量杂质的烧碱样品,某学生用中和滴定法测定烧碱的纯度,若烧碱中含有与酸不反应的杂质,请根据实验回答:| 滴定次数 | 待测液体积(mL) | 标准盐酸体积(mL) | |
| 滴定前读数(mL) | 滴定后读数(mL) | ||
| 第一次 | 10.00 | 0.50 | 20.40 |
| 第二次 | 10.00 | 4.00 | 24.10 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com