
 ;
;分析 (1)①质子数与中子数决定具体原子;
②元素性质由原子最外层电子数决定;
③质量数=质子数+中子数;
(2)氟离子核电荷数为9,核外电子数为10,有2个电子层,各层电子数为2、8;
(3)根据n=$\frac{V}{{V}_{m}}$计算氨气物质的量;根据H原子数目相同计算硫化氢的物质的量,再根据m=nM计算其质量;
(4)${\;}_{1}^{1}$H2${\;}_{8}^{18}$O的摩尔质量为20g/mol,根据n=$\frac{m}{M}$计算3g${\;}_{1}^{1}$H2${\;}_{8}^{18}$O的物质的量;根据质量数=质子数+中子数计算原子含有中子数,进而计算3g该分子含有的中子数目;
(5)根据n=$\frac{m}{M}$计算物质的量之比,相同条件下,气体的密度之比等于其摩尔质量之比.
解答 解:(1)①质子数与中子数决定具体原子,故答案为:AB;
②元素性质由原子最外层电子数决定,故答案为:D;
③由于质量数=质子数+中子数,故答案为:AB;
(2)氟离子核电荷数为9,核外电子数为10,有2个电子层,各层电子数为2、8,离子结构示意图为: ,故答案为:
,故答案为: ;
;
(3)在标准状况下,4.48L氨气(NH3)的物质的量为$\frac{4.48L}{22.4L/mol}$=0.2mol,与之含有相同氢原子数目的 H2S气体的物质的量为$\frac{0.2mol×3}{2}$=0.3mol,H2S气体的质量为0.3mol×34g/mol=10.2g,故答案为:0.2mol;10.2;
(4)${\;}_{1}^{1}$H2${\;}_{8}^{18}$O的摩尔质量为20g/mol,3g${\;}_{1}^{1}$H2${\;}_{8}^{18}$O的物质的量为$\frac{3g}{20g/mol}$=0.15mol,分子含有中子数为[0+(18-8)]=10,故含有的中子数目为0.15mol×10×6.02×1023mol-1=9.03×1023,
故答案为:0.15mol;9.03×1023;
(5)由n=$\frac{m}{M}$可知,相同质量的H2和N2中物质的量之比为28g/mol:2g/mol=14:1,相同条件下,气体的密度之比等于其摩尔质量之比,故二者密度之比为2g/mol:28g/mol=1:14,
故答案为:14:1;1:14.
点评 本题考查原子构成、结构示意图、物质的量有关计算,侧重对基础知识的巩固,注意掌握以物质的量为中心的有关计算.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:解答题
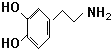
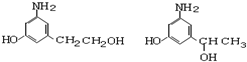 .
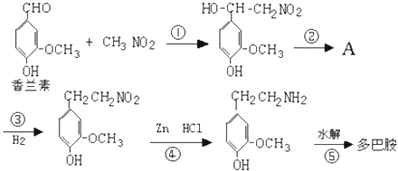
.
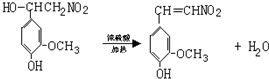 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 砷元素的最高化合价为+3 | |
| B. | 砷的气态氢化物比NH3稳定 | |
| C. | 砷的最高价氧化物的水溶液呈强碱性 | |
| D. | 砷原子的第3电子层含有18个电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将某种稀酸溶液,用蒸馏水稀释10倍,其pH一定增大一个单位 | |
| B. | 100℃时的NaCl溶液,PH约为6时呈中性. | |
| C. | pH相同的醋酸和H2SO4分别能恰好中和等物质的量的NaOH | |
| D. | 将0.1mol/L CH3COOH溶液加水稀释10倍,溶液中所有离子的浓度均减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| X | Y | ||
| W | Z | ||
| T |
| A. | W、X、Y三种元素最低价氢化物的稳定性依次降低 | |
| B. | X、Z、W的最高价氧化物对应的水化物酸性最强的是X | |
| C. | 五种元素均为非金属元素 | |
| D. | T元素的单质具有半导体的特性,T与Z元素可形成化合物TZ4 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
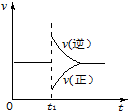 可逆反应2SO2(g)+O2(g)═2SO3(g)△H<0一定条件下在某密闭容器中达到平衡.t1时改变某一条件,化学反应速率与反应时间关系如图.下列说法中正确的是( )
可逆反应2SO2(g)+O2(g)═2SO3(g)△H<0一定条件下在某密闭容器中达到平衡.t1时改变某一条件,化学反应速率与反应时间关系如图.下列说法中正确的是( )| A. | t1时改变某一条件,平衡将向逆反应方向移动 | |
| B. | 维持压强不变,t1时升高反应体系温度 | |
| C. | 维持温度不变,t1时扩大反应体系体积 | |
| D. | 维持温度、压强不变,t1时充入SO2(g) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铜、石墨均能导电,所以它们均是电解质 | |
| B. | NH3、CO2的水溶液均能导电,所以NH3、CO2均是电解质 | |
| C. | 将25gCuSO4.5H2O晶体加水配成100mL溶液,该溶液的物质的量浓度为1mol/L | |
| D. | 实验室要用容量瓶配制0.2mol/L的NaCl溶液950mL,应称量NaCl固体11.1g |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③④ | B. | ②③④⑤ | C. | ②③④ | D. | ②③⑤ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com