
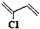
 )是制备氯丁橡胶的原料,它只比1,3-丁二烯(
)是制备氯丁橡胶的原料,它只比1,3-丁二烯( )多了一个氯原子,但由于双键上的氢原子很难发生取代反应,不能通过1,3-丁二烯直接与氯气反应制得,2-氯-1,3-丁二烯的逆合成分析为:
)多了一个氯原子,但由于双键上的氢原子很难发生取代反应,不能通过1,3-丁二烯直接与氯气反应制得,2-氯-1,3-丁二烯的逆合成分析为: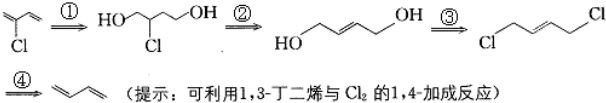
分析 根据逆合成分析可知,1,3-丁二烯合成2-氯-1,3-丁二烯的路线为:l,3-丁二烯与Cl2发生1,4加成反应生成1,4-二氯-2丁烯;1,4-二氯-2-丁烯在碱性条件下发生取代反应生成CH2OHCH=CHCH2OH,CH2OHCH=CHCH2OH含有双键与氯化氢发生加成反应生成CH2OHCHClCH2CH2OH,CH2OHCHClCH2CH2OH在浓硫酸做催化剂、脱水剂条件下发生消去反应生成2-氯-1,3-丁二烯,据此写出合成路线并判断反应类型.
解答 解:结合逆合成法可知,用1,3-丁二烯合成2-氯-1,3-丁二烯的过程为:
①l,3-丁二烯为二烯烃,与氯气按照物质的量之比1:1发生1,4加成加成反应生成1,4-二氯-2-丁烯;
②1,4-二氯-2丁烯在碱性条件下发生取代反应生成CH2OHCH=CHCH2OH,
③CH2OHCH=CHCH2OH有双键与氯化氢发生加成反应生成CH2OHCHClCH2CH2OH,
④CH2OHCHClCH2CH2OH在浓硫酸做催化剂、脱水剂条件下发生消去反应生成2-氯-1,3-丁二烯,
所以合成路线为: $→_{催化剂}^{Cl_{2}}$CH2(Cl)CH=CHCH2Cl$→_{△}^{NaOH的水溶液}$CH2OHCH=CHCH2OH$→_{催化剂}^{HCl}$CH2OHCHClCH2CH2OH$→_{△}^{浓硫酸}$
$→_{催化剂}^{Cl_{2}}$CH2(Cl)CH=CHCH2Cl$→_{△}^{NaOH的水溶液}$CH2OHCH=CHCH2OH$→_{催化剂}^{HCl}$CH2OHCHClCH2CH2OH$→_{△}^{浓硫酸}$ ,其中反应①为加成反应,反应②为取代反应,反应③为加成反应,反应④为消去反应,
,其中反应①为加成反应,反应②为取代反应,反应③为加成反应,反应④为消去反应,
答:该合成流程为 $→_{催化剂}^{Cl_{2}}$CH2(Cl)CH=CHCH2Cl$→_{△}^{NaOH的水溶液}$CH2OHCH=CHCH2OH$→_{催化剂}^{HCl}$CH2OHCHClCH2CH2OH$→_{△}^{浓硫酸}$
$→_{催化剂}^{Cl_{2}}$CH2(Cl)CH=CHCH2Cl$→_{△}^{NaOH的水溶液}$CH2OHCH=CHCH2OH$→_{催化剂}^{HCl}$CH2OHCHClCH2CH2OH$→_{△}^{浓硫酸}$ ;反应①③为加成反应、反应②为取代反应、反应④为消去反应.
;反应①③为加成反应、反应②为取代反应、反应④为消去反应.
点评 本题考查了有机合成,题目难度中等,明确常见有机物结构与性质为解答根据,注意掌握有机反应类型及判断方法,试题培养了学生灵活应用基础知识的能力.


 通城学典默写能手系列答案
通城学典默写能手系列答案科目:高中化学 来源: 题型:解答题
 ③2-甲基-1-戊烯:CH2=CH(CH3)CH2CH2CH3
③2-甲基-1-戊烯:CH2=CH(CH3)CH2CH2CH3查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 元素 | N | S | O | Si |
| 原子半径/10-10m | 0.75 | 1.02 | 0.74 | 1.17 |
| A. | 0.80×10-10m | B. | 0.70×10-10m | C. | 1.20×10-10m | D. | 1.10×10-10m |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
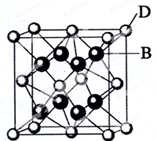 已知A、B、C、D和E都是元素周期表中前36号元素,它们的原子序数依次增大.A与其他4种元素既不在同一周期又不在同一主族.B和C属同一主族,D和E属同一周期,D的原子序数比E小5,又知E是周期表中1-18列中的第7列元素.D的价电子数为2,D跟B可形成离子化合物,其晶胞结构如图.请回答:
已知A、B、C、D和E都是元素周期表中前36号元素,它们的原子序数依次增大.A与其他4种元素既不在同一周期又不在同一主族.B和C属同一主族,D和E属同一周期,D的原子序数比E小5,又知E是周期表中1-18列中的第7列元素.D的价电子数为2,D跟B可形成离子化合物,其晶胞结构如图.请回答:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将pH=5的醋酸溶液稀释后,恢复至原温度,pH和Kw均增大 | |
| B. | 25℃时,pH=3的氯化铵溶液中:c(OH-)=1.0×10-11mol•L-1 | |
| C. | 25℃时,pH=4的氯化铵溶液中:c(Cl-)>c(NH4+)>c(H+)>c(OH-) | |
| D. | 向NH4HSO4溶液中加入等物质的量的NaOH形成的溶液中:c(Na+)=c(SO42-)>c(NH4+)>c(H+)>c(OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 50mL 0.50mol•L-1盐酸与50mL 0.55mol•L-1NaOH溶液在如图所示的装置中进行中和反应.通过测定反应过程中所放出的热量可计算中和反应的反应热.
50mL 0.50mol•L-1盐酸与50mL 0.55mol•L-1NaOH溶液在如图所示的装置中进行中和反应.通过测定反应过程中所放出的热量可计算中和反应的反应热.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 使用环形玻璃搅拌棒是为了加快反应速率,使其充分反应,减小实验误差 | |
| B. | 为了准确测定反应混合溶液的温度,实验中温度计水银球应与小烧杯底部接触 | |
| C. | 为了使反应均匀进行,可以向酸(碱)中分次加入碱(酸) | |
| D. | 在测定中和热实验中需要使用的仪器有量筒、烧杯、胶头滴管、温度计等 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com