
已知A、B、C、D、E是短周期的五种元素,它们的原子序数依次增大。A是短周期元素中原子半径最小的元素;C、D、E三种元素的最高价氧化物对应水化物之间可以两两反应;A与C同主族;B与E同主族;E的单质为淡黄色晶体。
(1)写出E元素在周期表中的位置 ;
(2)写出C元素的离子结构示意图 ;
(3)写出化合物A2B的电子式 ;
(4)写出C、D的最高价氧化物对应水化物相互反应的化学方程式: 。
(5分)(1)第三周期第ⅥA族 (2) (3)
(3) (4)NaOH+Al(OH)3=NaAlO2+2H2O
(4)NaOH+Al(OH)3=NaAlO2+2H2O
解析试题分析:A是短周期元素中原子半径最小的元素,则A是氢元素;C、D、E三种元素的最高价氧化物对应水化物之间可以两两反应,则一定含有铝元素,根据原子序数可知D是铝; E的单质为淡黄色晶体,则E是S。B与E同主族,所以B是氧元素。A与C同主族,且C的原子序数大于B的,小于D的,因此C是Na。
(1)E元素在周期表中的位置第三周期第ⅥA族。
(2)C元素的离子结构示意图 。
。
(3)化合物A2B是水,含有共价键的共价化合物,电子式为 。
。
(4)氢氧化铝是两性氢氧化物,能溶解在氢氧化钠溶液中,反应的化学方程式是NaOH+Al(OH)3=NaAlO2+2H2O。考点:考查元素周期表的结构以及常见化学用语的书写
点评:该题设计新颖,基础性强,有利于调动学生的学习积极性,激发学生的学习兴趣。该题以“周期表中元素的推断”为载体,比较全面考查学生有关元素推断知识和灵活运用知识的能力。考查学生对元素周期表的熟悉程度及其对表中各元素性质和相应原子结构的周期性递变规律的认识和掌握程度。考查了学生对物质结构与性质关系以及运用元素周期律解决具体化学问题的能力。


科目:高中化学 来源: 题型:填空题
有A、B、C、D、E、F六种短周期元素,其元素特征信息如下表:
| 元素编号 | 元素特征信息 |
| A | A的单质是密度最小的物质 |
| B | B的单质能与冷水剧烈反应,所得强碱性溶液中含有两种电子数相同的阴、阳离子 |
| C | C的原子最外层电子数是其内层电子数的三倍 |
| D | D与B同周期,该周期中D的简单离子半径最小 |
| E | B、C、E组成的36电子的化合物Y是家用消毒剂的主要成分 |
| F | F元素最高正价与最低负价的代数和为4 |
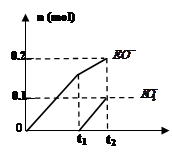
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
A、B、C、D、E是周期表中前四周期的元素,其有关性质或结构信息如下表:
| 元素 | 有关性质或结构信息 |
| A | 负二价的A元素的氢化物在通常状况下是一种液体,其中A的质量分数为88.9% |
| B | B原子得到一个电子后3p轨道全充满 |
| C | C原子的p轨道半充满,它的气态氢化物能与其最高价氧化物的水化物反应生成一种常见的盐X |
| D | D元素的最高化合价与最低化合价的代数和为零,其最高价氧化物为分子晶体 |
| E | E元素的核电荷数等于A原子和B元素氢化物的核电荷数之和 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
硼元素B在化学中有很重要的地位。硼的化合物在农业、医院、玻璃等方面用途很广。请回答下列问题:
(1)写出与B元素同主族的Ga元素的基态原子核外电子分布式 ,从原子结构的角度分析,B、N、O元素的第一电离能由大到小的顺序为 。
(2)立方氮化硼可利用人工方法在高温高压条件下合成,属于超硬材料,同属原子晶体的氮化硼(BN)比晶体硅具有更高硬度和耐热性的原因是 。
(3)在BF3分子中中心原子的杂化轨道类型是 ,SiF4微粒的空间构型是 。
(4)科学家发现硼化镁在39K时呈超导性,在硼化镁晶体的理想模型中,镁原子和硼原子是分层排布的,一层镁一层硼相间排列。图23是该晶体微观窨中取出的部分原子沿Z轴方向的投影,白球是镁原子投影,黑球是硼原子投影,图中的硼原子和镁原子投影在同一平面上。根据图示确定硼化镁的化学式为 。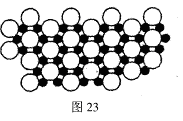
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
X~R是元素周期表中的短周期元素,其性质或结构信息如下表:
| 元素 | X | Y | Z | W | R |
| 性质信息 | 能形成+7价的化合物 | 日常生活中常见金属,熔化时并不滴落,好象有一层膜兜着 | 通常状况下能形成短周期中最稳定的双原子分子 | 焰色反应为黄色 | 位于第IVA,是形成化合物种类最多的元素 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
砷(As)在地壳中含量不大,但砷的化合物却是丰富多彩。
(1)砷的基态原子的电子排布式为 。
(2)目前市售的发光二极管,其材质以砷化镓(GaAs)为主。Ga和As相比,电负性较大的是 ,GaAs中Ga的化合价为 。
(3)AsH3是无色稍有大蒜气味的气体,在AsH3中As原子的杂化轨道类型为 ;
AsH3的沸点高于PH3,其主要原因为 。
(4)Na3AsO4可作杀虫剂。AsO43-的立体构型为 ,与其互为等电子体的分子的化学式为 (任写一种)。
(5)H3AsO4和H3AsO3是砷的两种含氧酸,请根据结构与性质的关系,解释H3AsO4比H3AsO3酸性强的原因 。
(6)磷与砷同主族,磷的一种单质白磷(P4)属于分子晶体,其晶胞如图。已知最近的两个白磷分子间距离为 a pm,阿伏加德罗常数的值为NA,则该晶体的密度为______g/cm3(只要求列算式,不必计算)。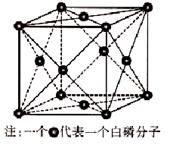
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
下表是元素周期表的一部分,根据表中10种元素,用元素符号或化学式填空。
| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
| 2 | | | | ① | | ② | | |
| 3 | | | ③ | ④ | | ⑤ | ⑥ | ⑦ |
| 4 | ⑨ | ⑧ | | | | ⑩ | | |
查看答案和解析>>
科目:高中化学 来源: 题型:问答题
(14分)元素周期表是学习化学的重要工具,它隐含着许多信息和规律,下面是八种短周期元素的相关信息(已知铍的原子半径为0.089nm)
| 元素代号 | A | B | C | D | E |
| 原子半径/nm | 0.16 | 0.143 | 0.102 | 0.099 | 0.074 |
| 主要化合价 | +2 | +3 | +6,-2 | -1 | -2 |
查看答案和解析>>
科目:高中化学 来源: 题型:问答题
已知A、B、C、D、E、F为元素周期表中原子序数依次增大的前20号元素,A、B与C;D、E与F分别位于同一周期。A原子L层上有3个未成对电子,B的简单负二价离子与C原子核外电子排布相同、含有D元素的盐的焰色反应火焰为黄色,EF3是由活泼金属和活泼非金属组成的共价化合物,G有多种氧化物,其中一种氧化物有磁性,填写下列空白
(1)元素的第一电离能最大的是________,属于过渡元素的是________(填写元素符号)
(2)写出B元素的基态原子价电子排布式__________________,F离子电子排布式_________________。
(3)AF3分子中A原子的杂化类型是________,AF3分子的几何构型为___________。
(4)已知E2B3的晶格比DF的晶格能大得多,试分析导致两者晶格能差异的主要原因是:________________________________________________________。
(5)构成G晶体的微粒是________,G的晶胞结构如下图甲所示,G的晶胞为________结构。若G原子的半径为1.27×10-10 m,G金属晶体中的晶胞长度,即下图乙中AB的长度为________m。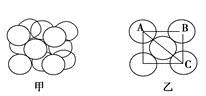
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com