
在氧、氟、钠、氯四种元素中,原子半径最大的元素是( )
A.氧 B.氟
C.钠 D.氯
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
甲、乙、丙、丁分别是Al2(SO4)3、FeSO4、NaOH、BaCl24种物质的一种,若将丁溶液滴入乙溶液中,发现有白色沉淀生成,继续滴加则沉淀消失;丁溶液滴入甲溶液时,无明显现象发生,据此可推断丙物质是( )
A.Al2(SO4)3 B.NaOH C.BaCl2 D.FeSO4
查看答案和解析>>
科目:高中化学 来源: 题型:
已知H—H键能为436 KJ/mol,H—N键能为391KJ/mol,根据化学方程式:N2 + 3H2 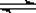 2 NH3 ΔH=—92.4 KJ/mol,则N≡N键的键能是 ( )
2 NH3 ΔH=—92.4 KJ/mol,则N≡N键的键能是 ( )
A.431 KJ/mol B.946KJ/mol C.649 KJ/mol D.869 KJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
实验室用固体烧碱配制0.1mol/L的NaOH溶液500mL,回答下列问题:
(1)计算需要NaOH固体的质量_______g
(2)有以下仪器和用品:配制时,必须使用的仪器或用品有①烧杯 ②药匙 ⑥托盘天平,还缺少的玻璃仪器是_______
(3)配制时,一般分为以下几个步骤:
①称量 ②计算 ③溶解 ④摇匀 ⑤移液 ⑥洗涤 ⑦定容 ⑧装瓶
其正确的操作顺序为:_______ (填序号)
(4)配制过程中,若其它操作均正确,下列操作会引起结果偏高的是_______(填序号)
①定容摇匀后,液面下降,又加水至刻度线
②未洗涤烧杯、玻璃棒
③容量瓶不干燥,含有少量蒸馏水
④称量NaOH的时间太长
⑤定容时俯视刻度.
查看答案和解析>>
科目:高中化学 来源: 题型:
以下有关原子结构及元素周期律的叙述正确的是( )
A.第ⅠA族元素铯的两种同位素137Cs比133Cs多4个质子
B.同周期元素(除0族元素外)从左到右,原子半径逐渐减小
C.第Ⅶ A族元素从上到下,其氢化物的稳定性逐渐增强
D.同主族元素从上到下,单质的熔点逐渐降低
查看答案和解析>>
科目:高中化学 来源: 题型:
原子序数由小到大排列的四种短周期元素X、Y、Z、W,其中X、Z、W与氢元素可组成XH3、H2Z和HW共价化合物,Y与氧元素可组成Y2O和离子化合物Y2O2。
(1)写出Y2O2的电子式____________________________________________________。
其中含有的化学键是______________________________________________。
(2)用电子式表示Z和Y形成化合物的过程______________________________________
______________________。
(3)XH3、H2Z和HW三种化合物,其中一种与另外两种都能反应的是________(填写电子式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
把少量的溴水加到过量的KI溶液中,再加入CCl4振荡后静置,下列现象中正确的是( )
A.得到均匀的紫色溶液
B.无色水层下有橙红色液体
C.无色水层下有紫色油状液体
D.无色水层上有紫色油状液体
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com