
”¾ĢāÄæ”æŌŚŅ»¶ØĢõ¼žĻĀ£¬½«³äĀśNO2ŗĶO2µÄŹŌ¹Üµ¹Į¢ÓŚĖ®²ŪÖŠ£¬³ä·Ö·“Ó¦ŗó£¬Ź£ÓąĘųĢåµÄĢå»żĪŖŌ»ģŗĻĘųĢåĢå»żµÄ![]() £¬ŌņŌ»ģŗĻĘųĢåÖŠNO2ŗĶO2µÄĢå»żÖ®±ČŹĒ
£¬ŌņŌ»ģŗĻĘųĢåÖŠNO2ŗĶO2µÄĢå»żÖ®±ČŹĒ
A.8£ŗ1B.7£ŗ3C.1£ŗ7D.4£ŗ1
”¾“š°ø”æB
”¾½āĪö”æ
NO2ŗĶO2µÄ»ģŗĻĘųĢåĶØČėµ¹Į¢ÓŚĖ®²ŪÖŠŹ¢ĀśĖ®µÄŹŌ¹ÜÖŠ£¬·¢Éś·“Ó¦æÉÄÜĪŖ£ŗ4NO2+O2+2H2O=4HNO3”¢3NO2+H2O=2HNO3+NO£¬Ź£ÓąĘųĢåµÄĢå»żĪŖŌ»ģŗĻĘųĢåµÄ![]() £¬ŹŌ¹ÜÖŠŹ£Óą
£¬ŹŌ¹ÜÖŠŹ£Óą![]() Ģå»żµÄæÉÄÜĪŖNO»ņO2£¬½įŗĻ·“Ó¦·½³ĢŹ½ĮŠŹ½¼ĘĖć”£
Ģå»żµÄæÉÄÜĪŖNO»ņO2£¬½įŗĻ·“Ó¦·½³ĢŹ½ĮŠŹ½¼ĘĖć”£
·¢Éś·“Ó¦ĪŖ£ŗ4NO2+O2+2H2O=4HNO3”¢3NO2+H2O=2HNO3+NO£¬Ź£ÓąĘųĢåµÄĢå»żĪŖŌ»ģŗĻĘųĢåµÄ![]() £¬ŌņŹŌ¹ÜÖŠŹ£Óą
£¬ŌņŹŌ¹ÜÖŠŹ£Óą![]() Ģå»żµÄĪŖNO»ņO2”£ÉčNO2ŗĶO2µÄ×ÜĢå»żĪŖV£¬
Ģå»żµÄĪŖNO»ņO2”£ÉčNO2ŗĶO2µÄ×ÜĢå»żĪŖV£¬
µ±Ź£ÓąĘųĢåĪŖNOŹ±£¬ĖµĆ÷ŃõĘų²»×ć£¬Éś³É![]() VĢå»żµÄNOĻūŗĶžŃõ»ÆµŖµÄĢå»żĪŖ£ŗ
VĢå»żµÄNOĻūŗĶžŃõ»ÆµŖµÄĢå»żĪŖ£ŗ![]() V”Į3=
V”Į3=![]() £»
£»
Ōņ·“Ó¦4NO2+O2+2H2O=4HNO3ÖŠ×ܹ²ĻūŗĶžŃõ»ÆµŖŗĶŃõĘųµÄ×ÜĢå»żĪŖ£ŗ![]() £¬Ō»ģŗĻĘųĢåÖŠŃõĘųµÄĢå»żĪŖ£ŗ
£¬Ō»ģŗĻĘųĢåÖŠŃõĘųµÄĢå»żĪŖ£ŗ![]() ”Į
”Į![]() =
=![]() V£¬Ō»ģŗĻĘųĢåÖŠ¶žŃõ»ÆµŖµÄĢå»żĪŖ£ŗ
V£¬Ō»ģŗĻĘųĢåÖŠ¶žŃõ»ÆµŖµÄĢå»żĪŖ£ŗ![]() £¬Ō»ģŗĻĘųĢåÖŠNO2ŗĶO2µÄĢå»ż±ČĪŖ£ŗ
£¬Ō»ģŗĻĘųĢåÖŠNO2ŗĶO2µÄĢå»ż±ČĪŖ£ŗ![]() £ŗ
£ŗ![]() V=7£ŗ1£»
V=7£ŗ1£»
µ±ŃõĘų¹żĮæŹ±£¬Ź£ÓąµÄ![]() VĢå»żĪŖO2£¬ĖµĆ÷NO2²»×ćĮ棬Ōņ²Ī¼Ó·“Ó¦4NO2+O2+2H2O=4HNO3ÖŠ×ܹ²ĻūŗÄNO2ŗĶO2µÄ×ÜĢå»żĪŖ
VĢå»żĪŖO2£¬ĖµĆ÷NO2²»×ćĮ棬Ōņ²Ī¼Ó·“Ó¦4NO2+O2+2H2O=4HNO3ÖŠ×ܹ²ĻūŗÄNO2ŗĶO2µÄ×ÜĢå»żĪŖ![]() £¬»ģŗĻĘųĢåÖŠ¶žŃõ»ÆµŖµÄ×ÜĢå»żĪŖ£ŗ
£¬»ģŗĻĘųĢåÖŠ¶žŃõ»ÆµŖµÄ×ÜĢå»żĪŖ£ŗ![]() ”Į
”Į![]() =
=![]() £¬O2×ÜĢå»żĪŖ
£¬O2×ÜĢå»żĪŖ![]() £¬¹ŹŌĘųĢåÖŠNO2ŗĶO2µÄĢå»ż±ČĪŖ
£¬¹ŹŌĘųĢåÖŠNO2ŗĶO2µÄĢå»ż±ČĪŖ![]() £ŗ
£ŗ![]() =7£ŗ3£¬
=7£ŗ3£¬
¹ŹŗĻĄķŃ”ĻīŹĒB”£



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ¾ŪŗĻ¼īŹ½ĀČ»ÆĢś[![]() £ØmĪŖ¾ŪŗĻ¶Č£©ĪŖĪŽ»śøß·Ö×ÓŠõÄż¼Į£¬¹ć·ŗÓ¦ÓĆÓŚĖ®“¦Ąķ”£ŅŌĢśæóŹÆ”¢Ńõ»ÆĢśĘ¤»ņ
£ØmĪŖ¾ŪŗĻ¶Č£©ĪŖĪŽ»śøß·Ö×ÓŠõÄż¼Į£¬¹ć·ŗÓ¦ÓĆÓŚĖ®“¦Ąķ”£ŅŌĢśæóŹÆ”¢Ńõ»ÆĢśĘ¤»ņ![]() ĪŖŌĮĻ£¬ŌŚĖįŠŌĢõ¼žĻĀ¾Ńõ»Æ”¢Ė®½ā”¢¾ŪŗĻ”¢Źģ»ÆµČ²½Öč£¬æÉÖĘµĆ¾ŪŗĻ¼īŹ½ĀČ»ÆĢś”£
ĪŖŌĮĻ£¬ŌŚĖįŠŌĢõ¼žĻĀ¾Ńõ»Æ”¢Ė®½ā”¢¾ŪŗĻ”¢Źģ»ÆµČ²½Öč£¬æÉÖĘµĆ¾ŪŗĻ¼īŹ½ĀČ»ÆĢś”£
(1)øÖĢśĖįĻ“·ĻŅŗÖŠÖ÷ŅŖŗ¬ÓŠ![]() ŗĶ
ŗĶ![]() £¬ĶØČėæÕĘųæÉÖʵĆ
£¬ĶØČėæÕĘųæÉÖʵĆ![]() £¬·“Ó¦µÄ»Æѧ·½³ĢŹ½________”£Ńõ»Æ¼Į
£¬·“Ó¦µÄ»Æѧ·½³ĢŹ½________”£Ńõ»Æ¼Į![]() Ņ²æÉŅŌ½«
Ņ²æÉŅŌ½«![]() Ńõ»Æ³É
Ńõ»Æ³É![]() £¬µ«“ęŌŚµÄȱµćŹĒ________________”£
£¬µ«“ęŌŚµÄȱµćŹĒ________________”£
(2)”°Ńõ»Æ”±¹ż³ĢÖŠ£¬ČōŃĪĖįµÄÅØ¶Č»ņĶ¶ČėĮæŌö“󣬳żĮĖ»į½µµĶ![]() µÄ×Ŗ»ÆĀŹ£¬»¹æÉÄܲśÉśµÄÓ°ĻģĪŖ________________”£
µÄ×Ŗ»ÆĀŹ£¬»¹æÉÄܲśÉśµÄÓ°ĻģĪŖ________________”£
(3)¢Ł×¼Č·³ĘČ”¾ŪŗĻ¼īŹ½ĀČ»ÆĢśŃłĘ·1.5000g£¬ÖĆÓŚ250mLµÄ׶ŠĪĘæÖŠ£¬¼ÓČėŹŹĮæĻ”ŃĪĖį£¬¼ÓČČ£¬ŃøĖŁ¼ÓČėÉŌ¹żĮæµÄ![]() ČÜŅŗ£Ø
ČÜŅŗ£Ø![]() ±»
±»![]() Ńõ»Æ³ÉĪŖ
Ńõ»Æ³ÉĪŖ![]() £©£¬³ä·Ö·“Ó¦ŗ󣬶ąÓąµÄ
£©£¬³ä·Ö·“Ó¦ŗ󣬶ąÓąµÄ![]() ÓĆ
ÓĆ![]() Ńõ»Æ³żČ„”£ŌŁ¼ÓČėŹŹĮæµÄ
Ńõ»Æ³żČ„”£ŌŁ¼ÓČėŹŹĮæµÄ![]() ×é³ÉµÄ»ģĖį¼°4~5µĪÖøŹ¾¼Į£¬ÓĆ
×é³ÉµÄ»ģĖį¼°4~5µĪÖøŹ¾¼Į£¬ÓĆ![]() ČÜŅŗµĪ¶ØÖĮÖÕµć£ØµĪ¶Ø¹ż³ĢÖŠ
ČÜŅŗµĪ¶ØÖĮÖÕµć£ØµĪ¶Ø¹ż³ĢÖŠ![]() Óė
Óė![]() ·“Ӧɜ³É
·“Ӧɜ³É![]() ŗĶ
ŗĶ![]() £©£¬ĻūŗÄ
£©£¬ĻūŗÄ![]() ČÜŅŗ
ČÜŅŗ![]() ”£
ӣ
¢ŚĮķ³ĘČ”µČÖŹĮæµÄ¾ŪŗĻ¼īŹ½ĀČ»ÆĢśŃłĘ·ČÜÓŚĖ®ÖŠ£¬Åä³É500mLČÜŅŗ£¬Č”25mLČÜŅŗӌ׶ŠĪĘæÖŠ£¬ÓĆøõĖį¼Ų£Ø![]() £©ČÜŅŗ×÷ÖøŹ¾¼Į£¬ÓĆ
£©ČÜŅŗ×÷ÖøŹ¾¼Į£¬ÓĆ![]() ±ź×¼ČÜŅŗµĪ¶ØÖĮÖÕµć£¬ĻūŗÄ
±ź×¼ČÜŅŗµĪ¶ØÖĮÖÕµć£¬ĻūŗÄ![]() ČÜŅŗ8.10mL”£
ČÜŅŗ8.10mL”£
¼ĘĖćøĆѳʷ֊ĀČŌŖĖŲŗĶĢśŌŖĖŲµÄÖŹĮæ·ÖŹżÖ®±Č![]() ĪŖ________£ØŠ“³ö¼ĘĖć¹ż³Ģ£¬½į¹ū±£ĮōĖÄĪ»ÓŠŠ§Źż×Ö£©”£
ĪŖ________£ØŠ“³ö¼ĘĖć¹ż³Ģ£¬½į¹ū±£ĮōĖÄĪ»ÓŠŠ§Źż×Ö£©”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŅŃÖŖ£ŗ¢ŁH2O(g)===H2O(l)”” ¦¤H1£½£Q1 kJ”¤mol£1
¢ŚC2H5OH(g)===C2H5OH(l) ¦¤H2£½£Q2 kJ”¤mol£1
¢ŪC2H5OH(g)£«3O2(g)===2CO2(g)£«3H2O(g) ¦¤H3£½£Q3 kJ”¤mol£1
ČōŹ¹23 gŅŗĢ¬ĪŽĖ®¾Ę¾«ĶźČ«Č¼ÉÕ£¬×īŗó»Öø“µ½ŹŅĪĀ£¬Ōņ·Å³öµÄČČĮæĪŖ(µ„Ī»£ŗkJ)
A. Q1£«Q2£«Q3B. 1.5Q1£0.5Q2£«0.5Q3
C. 0.5Q1£1.5Q2£«0.5Q3D. 0.5(Q1£«Q2£«Q3)
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æÄ³Ń§Ļ°Š”×éµÄĶ¬Ń§¶ŌĀČĘųÓėĢśµÄ·“Ó¦¼°²śĪļ½ųŠŠĮĖČēĻĀĢ½¾æ:
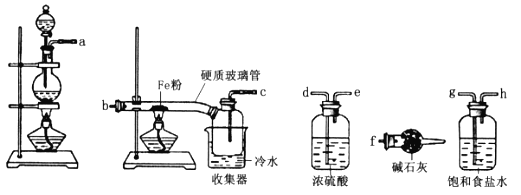
£Ø1£©×°ÖƵÄĮ¬½ÓĖ³ŠņĪŖa”ś_____”ś______”ś_____”ś_____”śb”śc”śf”£________
£Ø2£©Ó²ÖŹ²£Į§¹ÜÓėŹÕ¼ÆĘ÷Ö®¼äƻӊÓƵ¼¹ÜĮ¬½Ó£¬ÕāŃł×öµÄÓŵćŹĒ________________”£
£Ø3£©·“Ó¦Ņ»¶ĪŹ±¼ä£¬ĻØĆš¾Ę¾«µĘ£¬ĄäČ“ŗ󣬽«ŹÕ¼ÆĘ÷¼°Ó²ÖŹ²£Į§¹ÜÖŠµÄĪļÖŹæģĖŁ×ŖŅĘÖĮ׶ŠĪĘæÖŠ£¬¼ÓČė¹żĮæµÄĻ”ŃĪĖįŗĶÉŁŠķÖ²ĪļÓĶ(·“Ó¦¹ż³ĢÖŠ²»Õńµ“)£¬³ä·Ö·“Ó¦ŗ󣬽ųŠŠČēĻĀŹµŃé:
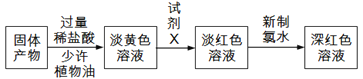
ŹŌ¼ĮXÖŠČÜÖŹµÄ»ÆѧŹ½ĪŖ____________£»¹ĢĢå²śĪļµÄ³É·ÖæÉÄÜĪŖ_____(Ģī×ÖÄø)”£
A£®FeŗĶFeCl3 B£®FeCl2ŗĶFeCl3 C£®Fe”¢FeCl2ŗĶFeCl3 D£®FeŗĶFeCl2
£Ø4£©¼ÓČėÉŁŠķÖ²ĪļÓĶµÄ×÷ÓĆŹĒ____________£¬¼ÓČėŠĀÖĘĀČĖ®ŗóČÜŅŗŗģÉ«¼ÓÉīµÄŌŅņ£ŗ___________(ÓĆĄė×Ó·½³ĢŹ½±ķŹ¾)”£
£Ø5£©ĻÖÓŠŅ»ŗ¬FeCl2ŗĶFeCl3»ģŗĻĪļµÄѳʷ£¬ÓĆĄė×Ó½»»»·Ø²āµĆn(Fe)£ŗn(Cl)=1£ŗ2.1£¬ŌņøĆѳʷ֊FeCl3µÄĪļÖŹµÄĮæ·ÖŹżĪŖ______”££Ø¼ĘĖć½į¹ū±£ĮōĮ½Ī»ÓŠŠ§Źż×Ö£©
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĶź³ÉĻĀĮŠÓėČÜŅŗpHÓŠ¹ŲµÄ¼ĘĖć
£Ø1£©ŹŅĪĀĻĀpH=2µÄHClČÜŅŗŗĶpH=10µÄNaOHČÜŅŗÖŠÓÉĖ®µēĄė³öµÄc(H+)Ö®±ČĪŖ____”£
£Ø2£©ŌŚ25”ꏱ£¬pHµČÓŚ9ŗĶpHµČÓŚ11µÄĮ½ÖÖĒāŃõ»ÆÄĘČÜŅŗµČĢå»ż»ģŗĻŗó£¬ČÜŅŗÖŠµÄĒāĄė×ÓÅضČĪŖ__”£
£Ø3£©Ä³ĪĀ¶ČŹ±£¬Ė®µÄKW=10-13£¬½«“ĖĪĀ¶ČĻĀpH=12µÄNaOHČÜŅŗaLÓėpH=2µÄH2SO4ČÜŅŗbL»ģŗĻ£¬ČōĖłµĆ»ģŗĻČÜŅŗpH=3£¬Ōņa£ŗb=___”£
£Ø4£©ŅŃÖŖijĪĀ¶ČŹ±0.1molL-1NaOH pHµČÓŚ11£¬ŌŚ“ĖĪĀ¶ČĻĀ£¬Čō½«100Ģå»żpH1£½aµÄH2SO4ČÜŅŗÓė1Ģå»żpH2£½bµÄNaOHČÜŅŗ»ģŗĻŗóČÜŅŗ³ŹÖŠŠŌ£¬Ōņ»ģŗĻĒ°£¬øĆĒæĖįµÄpH1ÓėĒæ¼īµÄpH2Ö®¼äÓ¦Āś×ćµÄ¹ŲĻµŹĒ___£ØÓĆŗ¬a”¢bµÄ±ķ“ļŹ½±ķŹ¾£©
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æÓĆĻĀĶ¼ĖłŹ¾×°ÖĆ½ųŠŠĻĀĮŠŹµŃé£ŗ½«¢ŁÖŠČÜŅŗµĪČė¢ŚÖŠ£¬Ō¤²āµÄĻÖĻóÓėŹµ¼ŹĻą·ūµÄŹĒ
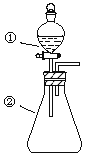
Ń”Ļī | ¢ŁÖŠĪļÖŹ | ¢ŚÖŠĪļÖŹ | Ō¤²ā¢ŚÖŠµÄĻÖĻó |
A | Ļ”ŃĪĖį | Ģ¼ĖįÄĘÓėĒāŃõ»ÆÄʵĻģŗĻČÜŅŗ | Į¢¼“²śÉśĘųÅŻ |
B | ÅØĻõĖį | ÓĆÉ°Ö½“ņÄ„¹żµÄĀĮĢõ | ²śÉśŗģ×ŲÉ«ĘųĢå |
C | ŠĀÖĘĀČĖ® | µķ·Ūµā»Æ¼ŲČÜŅŗ | ČÜŅŗ±äĄ¶É« |
D | ÅØŃĪĖį | MnO2 | ²śÉś»ĘĀĢÉ«ĘųĢå |
A.AB.BC.CD.D
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŌŚŅ»ĆܱյÄČŻĘ÷ÖŠ£¬·“Ó¦aA(g)![]() bB(g)“ļĘ½ŗāŗ󣬱£³ÖĪĀ¶Č²»±ä£¬½«ČŻĘ÷Ģå»żŌö¼ÓŅ»±¶£¬µ±“ļµ½ŠĀµÄĘ½ŗāŹ±£¬BµÄÅØ¶ČŹĒŌĄ“µÄ60%£¬Ōņ£Ø £©
bB(g)“ļĘ½ŗāŗ󣬱£³ÖĪĀ¶Č²»±ä£¬½«ČŻĘ÷Ģå»żŌö¼ÓŅ»±¶£¬µ±“ļµ½ŠĀµÄĘ½ŗāŹ±£¬BµÄÅØ¶ČŹĒŌĄ“µÄ60%£¬Ōņ£Ø £©
A.ĪļÖŹAµÄ×Ŗ»ÆĀŹĢįøßĮĖB.Ę½ŗāĻņÄę·“Ó¦·½ĻņŅʶÆĮĖ
C.ĪļÖŹBµÄÖŹĮæ·ÖŹż¼õÉŁĮĖD.a>b
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŃĒĢśĒč»Æ¼Ų¾§Ģå»ÆѧŹ½ĪŖ£ŗKxFey(CN)znH2O£¬Ė×³Ę»ĘŃŖŃĪ£¬³£ÓĆ×÷Ź³Ę·æ¹½į¼Į”£Ņ»ÖÖÓĆNaCN£ØNĻŌ-3¼Ū£©·ĻŅŗÖĘČ”»ĘŃŖŃĪµÄÖ÷ŅŖ¹¤ŅÕĮ÷³Ģ£ŗ
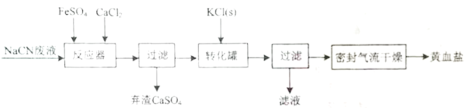
£Ø1£©ŹµŃéŹŅÓĆĀĢ·Æ¹ĢĢåÅäÖĘFeSO4ČÜŅŗŹ±£¬Ó¦ĻČ________£¬ŌŁÓĆÕōĮóĖ®Ļ”ŹĶ”£
£Ø2£©”°×Ŗ»Æ¹Ž”±ÖŠÉś³É»ĘŃŖŃĪ¾§ĢåµÄ·“Ó¦ĄąŠĶĪŖ________”£
£Ø3£©²ÉÓĆĆÜ·āĘųĮ÷øÉŌļČ”“śŌŚĶØ·ē³÷ÄŚøÉŌļµÄŌŅņŹĒ________”£
£Ø4£©»ĘŃŖŃĪµÄ»ÆѧŹ½æÉĶعżĻĀĮŠŹµŃé²ā¶Ø£ŗ
¢Ł×¼Č·³ĘČ”4.220gѳʷ¼ÓČėĖ®ÖŠ³ä·ÖČܽā£¬½«ĖłµĆČÜŅŗ×ŖŅĘÖĮČŻĮæĘæÅäÖĘ³É100.00mLČÜŅŗA”£
¢ŚĮæČ”25.00mLČÜŅŗA£¬ÓĆ2.000molL-1KMnO4ČÜŅŗµĪ¶Ø£¬“ļµ½µĪ¶ØÖÕµćŹ±£¬¹²ĻūŗÄKMnO4ČÜŅŗ15.25mL”£·“Ó¦ČēĻĀ£ØĪ“ÅäĘ½£©£ŗ![]() ¢ŪĻņ¢ŚĖłµĆČÜŅŗ¼ÓČėMn2+Ąė×Ó½»»»Ź÷Ö¬£¬½«Mn2+ĶźČ«Īüø½ŗóŌŁµĪ¼Ó×ćĮæNaOHČÜŅŗ£¬¹żĀĖ”¢Ļ“µÓ”¢×ĘÉÕ£¬×īÖÕµĆ¹ĢĢå0.2g”£
¢ŪĻņ¢ŚĖłµĆČÜŅŗ¼ÓČėMn2+Ąė×Ó½»»»Ź÷Ö¬£¬½«Mn2+ĶźČ«Īüø½ŗóŌŁµĪ¼Ó×ćĮæNaOHČÜŅŗ£¬¹żĀĖ”¢Ļ“µÓ”¢×ĘÉÕ£¬×īÖÕµĆ¹ĢĢå0.2g”£
Ķعż¼ĘĖćČ·¶ØѳʷµÄ»ÆѧŹ½£ØŠ“³ö¼ĘĖć¹ż³Ģ£©”£______________
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ¶ŌÓŚ·“Ó¦3Cl2 + 6NaOH ![]() 5NaCl + NaClO3 + 3H2O£¬ŅŌĻĀŠšŹöÕżČ·µÄŹĒ( )
5NaCl + NaClO3 + 3H2O£¬ŅŌĻĀŠšŹöÕżČ·µÄŹĒ( )
A.Cl2ŹĒŃõ»Æ¼Į£¬NaOHŹĒ»¹Ō¼Į
B.±»Ńõ»ÆµÄClŌ×ÓÓė±»»¹ŌµÄClŌ×ÓµÄøöŹż±ČĪŖ1”Ć5
C.Ńõ»Æ²śĪļÓė»¹Ō²śĪļµÄĪļÖŹµÄĮæµÄ±ČĪŖ5”Ć1
D.ĆæÉś³É1molµÄNaClO3×ŖŅĘ6molµÄµē×Ó
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com