
等质量的两份锌粉a、b分别加入到两份质量相同的过量的稀硫酸中,同时向a中加入少量的CuSO4溶液,下列各图为产生H2的体积V(L)与时间t(min)的关系,其中正确的是( )
|
| A. |
| B. |
| C. |
| D. |
|
考点:
化学反应速率的影响因素;原电池和电解池的工作原理.
专题:
化学反应速率专题.
分析:
锌和硫酸反应,加入硫酸铜,会置换出金属铜,形成锌、铜、稀硫酸原电池,加快金属锌和硫酸反应的速率,产生氢气的量取决于金属锌的质量.
解答:
解:锌和硫酸反应,加入硫酸铜,会置换出金属铜,形成锌、铜、稀硫酸原电池,加快金属铁和硫酸反应的速率,所以反应速率是:a>b,速率越大,锌完全反应时所用的时间越短,所以a所用的时间小于b的时间;
产生氢气的量取决于金属锌的质量,而a中,金属锌一部分用于置换金属铜,导致和硫酸反应生成氢气的量减少,所以氢气的体积是:a<b.
故选A.
点评:
本题考查了图象与反应速率,题目难度不大,分析图象时注意图象中坐标的含义、拐点变化趋势来解答,注意原电池反应较一般化学反应速率更大及硫酸过量为易错点.


科目:高中化学 来源: 题型:
有机物A的分子式为C9H10O2,A在光照条件下生成一溴代物B,B~K十种有机物之间发生的转化关系如下:
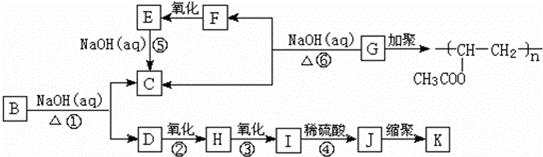
其中J物质与氯化铁溶液能发生显色反应,且环上的一元取代物只有两种结构.
已知:①当羟基与双键碳原子相连时,易发生如下转化:RCH=CHOH→RCH2CHO;
②﹣ONa连在烃基上不会被氧化.
请回答下列问题:
(1)写出下列反应的化学方程式:
J生成K
反应①
J与足量碳酸钠溶液反应: .
(2)同时符合下列要求的A的同分异构体有14种.
Ⅰ.含有苯环
Ⅱ.能发生银镜反应和水解反应
其中核磁共振氢谱有5个吸收峰且1mol该同分异构体能与1molNaOH反应,其结构简式为: .
查看答案和解析>>
科目:高中化学 来源: 题型:
若pH=3的酸溶液和pH=11的碱溶液等体积混合后溶液呈酸性,其原因可能是( )
|
| A. | 生成了一种强酸弱碱盐 |
|
| B. | 弱酸溶液和强碱溶液反应 |
|
| C. | 强酸溶液和弱碱溶液反应 |
|
| D. | 一元强酸溶液和一元强碱溶液反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
氢化铵(NH4H)与氯化铵的结构相似,又知NH4H与水反应有H2生成,下列叙述不正确的是( )
|
| A. | NH4H的电子式为 |
|
| B. | NH4Cl的电子式为 |
|
| C. | NH4H含有极性共价键和离子键 |
|
| D. | NH4H固体投入少量热水中,有两种气体生成 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关热化学方程式的叙述正确的是( )
|
| A. | 2H2(g)+O2(g)═2H2O(g)△H=﹣483.6 kJ/mol,则氢气的燃烧热为241.8 kJ |
|
| B. | 已知C(石墨,s)═C(金刚石,s)△H>0,则金刚石比石墨稳定 |
|
| C. | 含20.0g NaOH的稀溶液与稀盐酸完全中和,放出28.7 kJ的热量,则该反应的热化学方程式为:NaOH(aq)+HCl(aq)═NaCl(aq)+H2O(l)△H=﹣57.4 kJ/mol |
|
| D. | 已知2C(s)+2O2(g)═2CO2(g)△H1;2C(s)+O2(g)═2CO(g)△H2.则△H1>△H2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
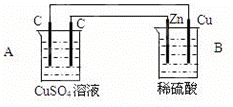
如图装置中,已知A、B两池溶液的体积均为200mL:
(1)判断装置的名称:A池为 ;
(2)A池中左边石墨棒为 极,电极反应式为 ;A池中总反应化学方程式为 4 ;
(3)若反应开始时,CuSO4溶液的浓度为1.0mol/L.工作一段时间后取出电极,测得导线上通过了0.04mol e﹣.则反应后A池c(Cu2+)为 mol/L(体积变化忽略不计).
查看答案和解析>>
科目:高中化学 来源: 题型:
据科学家预测,月球的土壤中吸附着数百万吨的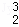 He,每百吨
He,每百吨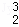 He核聚变所释放出的能量相当于目前人类一年消耗的能量.在地球上氦元素主要以
He核聚变所释放出的能量相当于目前人类一年消耗的能量.在地球上氦元素主要以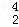 He的形式存在.下列说法正确的是()
He的形式存在.下列说法正确的是()
A. 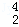 He原子核内含有4个质子
He原子核内含有4个质子
B. 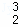 He原子核内含有3个中子
He原子核内含有3个中子
C. 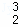 He和
He和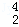 He互为同位素
He互为同位素
D. 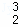 He和
He和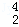 He互为同素异形体
He互为同素异形体
查看答案和解析>>
科目:高中化学 来源: 题型:
金属镍有广泛的用途.粗镍中含有少量Fe、Zn、Cu、Pt等杂质,可用电解法制备高纯度的镍,下列叙述正确的是(已知:氧化性Fe2+<Ni2+<Cu2+)()
A. 阳极发生还原反应,其电极反应式:Ni2++2e﹣═Ni
B. 电解过程中,阳极质量的减少与阴极质量的增加相等
C. 电解后,溶液中存在的金属阳离子只有Fe2+和Zn2+
D. 电解后,电解槽底部的阳极泥中只有Cu和Pt
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com