
(1)根据NaH的存在,有人提议可把氢元素放在 族,那么根据其最高正价与最低负价的绝对值相等,又可把氢元素放在周期表中的 族。
(2)现有甲、乙两种元素,甲元素在第三周期第VIIA族,甲元素与碘元素相比较,非金属性较强的是 (填元素名称),写出可以验证该结论的一个化学反应方程式
(3)现有甲、乙两种短周期元素,室温下,甲元素单质在冷的浓硫酸或空气中,表面都生成致密的氧化膜,乙元素原子核外M电子层与K电子层上的电子数相等。甲、乙两元素相比较,金属性较强的是 (填名称),可以验证该结论的实验是( )。
(a)将在空气中放置已久的这两种元素的块状单质分别放入热水中
(b)将这两种元素的单质粉末分别和同浓度的盐酸反应
(c)将这两种元素的单质粉末分别和热水作用,并滴入酚酞溶液
(d)比较这两种元素的气态氢化物的稳定性
(8分)(1) ,
, (各1分) (2)氯(1分);Cl2+2KI=I2+2KCl(2分)
(各1分) (2)氯(1分);Cl2+2KI=I2+2KCl(2分)
(3)镁(1分);bc(2分)
【解析】
试题分析:(1)NaH中氢元素的化合价是-1价,据此可以把氢元素放在第ⅦA族。第ⅣA族元素的最高正价与最低负价的绝对值相等。而氢元素的在最高价是+1价,据此又可把氢元素放在周期表中的第ⅣA族。
(2)甲元素在第三周期第VIIA族,则甲是氯元素。同主族自上而下,非金属性逐渐较弱,所以甲元素与碘元素相比较,非金属性较强的是氯元素。根据活泼性较强的可以置换出活泼性较弱的可知,该反应的化学方程式可以是Cl2+2KI=I2+2KCl。
(3)室温下,甲元素单质在冷的浓硫酸或空气中,表面都生成致密的氧化膜,所以甲是铝。乙元素原子核外M电子层与K电子层上的电子数相等,则乙是Mg。比较元素金属性强弱的一般依据是:在一定条件下金属单质与水反应的难易程度和剧烈程度。一般情况下,与水反应越容易、越剧烈,其金属性越强;常温下与同浓度酸反应的难易程度和剧烈程度。一般情况下,与酸反应越容易、越剧烈,其金属性越强,据此可知选项bc正确,a中因为久置Al表明含有氧化膜,不正确。金属没有氢化物,d不正确,答案选bc。
考点:考查元素周期表的结构、金属性和非金属性强弱比较
点评:该题是中等难度的试题,试题基础性强,难易适中,注重知识的灵活性,侧重能力的培养和解题方法的指导和训练。有助于培养学生的逻辑思维能力,提高学生分析问题,特别是灵活运用基础知识解决实际问题的能力。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
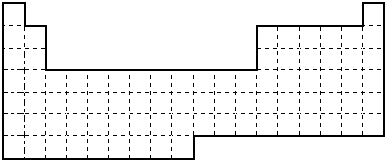
| 元素 | 相关信息 |
| X | X的基态原子核外3个能级上有电子,且每个能级上的电子数相等 |
| Y | M层上有2对成对电子 |
| Z | Z和Y同周期,Z的电负性大于Y |
| W | W的一种核素的质量数为63,中子数为34 |
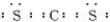
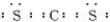
查看答案和解析>>
科目:高中化学 来源: 题型:
 (1)根据氢元素最高正价与最低负价的绝对值相等,有人提议可把氢元素放在周期表中的ⅣA族.那么根据NaH的存在,又可把氢元素放在
(1)根据氢元素最高正价与最低负价的绝对值相等,有人提议可把氢元素放在周期表中的ⅣA族.那么根据NaH的存在,又可把氢元素放在查看答案和解析>>
科目:高中化学 来源: 题型:
(2)某元素X的核外电子数等于核内中子数,取该元素单质
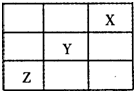
(3)短周期元素X、Y、Z在周期表中的位置关系如下图所示,则:

①Y、Z元素的气态氢化物的稳定性_______________>_______________。(填化学式)
②与Y元素同主族且相邻的元素的单质与NaOH溶液反应的离子方程式为______________。
查看答案和解析>>
科目:高中化学 来源:2012-2013学年四川省雅安中学高一4月月考化学试卷(带解析) 题型:填空题
(1)根据NaH的存在,有人提议可把氢元素放在 族,那么根据其最高正价与最低负价的绝对值相等,又可把氢元素放在周期表中的 族。
(2)现有甲、乙两种元素,甲元素在第三周期第VIIA族,甲元素与碘元素相比较,非金属性较强的是 (填元素名称),写出可以验证该结论的一个化学反应方程式
(3)现有甲、乙两种短周期元素,室温下,甲元素单质在冷的浓硫酸或空气中,表面都生成致密的氧化膜,乙元素原子核外M电子层与K电子层上的电子数相等。甲、乙两元素相比较,金属性较强的是 (填名称),可以验证该结论的实验是( )。
(a)将在空气中放置已久的这两种元素的块状单质分别放入热水中
(b)将这两种元素的单质粉末分别和同浓度的盐酸反应
(c)将这两种元素的单质粉末分别和热水作用,并滴入酚酞溶液
(d)比较这两种元素的气态氢化物的稳定性
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com