
已知2SO2+O2 2SO3为放热反应,关于该反应的下列说法正确的是( )
2SO3为放热反应,关于该反应的下列说法正确的是( )
A.O2的能量一定高于SO2的能量 B.SO2和O2的总能量一定高于SO3的总能量
C.SO2的能量一定高于SO3的能量 D.因该反应为放热反应,故不必加热反应就可发生
 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案科目:高中化学 来源: 题型:
利用相关数据作出的推理或判断一定正确的是:
A.用弱酸的电离常数比较相同条件下强碱弱酸盐溶液的碱性强弱
B.用物质的熔沸点数据推断物质的晶体类型
C.根据溶液的pH判断该溶液的酸碱性
D.根据焓变数据判断反应能否自发进行
查看答案和解析>>
科目:高中化学 来源: 题型:
工业[b16] 上用铝土矿(主要成分为Al2O3,Fe2O3等)提取Al2O3做冶炼铝的原料,由熔盐电解法获得的粗铝中含一定量的金属钠和氢气,这些杂质可采用吹气精炼法除去,产生的尾气经处理后可用于钢材镀铝。工艺流程如下图所示:
(已知:NaCl熔点为801℃;AlCl3在181℃升华)
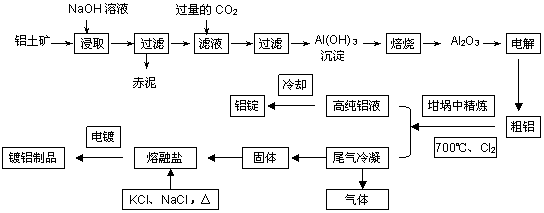 |
(1)向滤液中通入过量CO2所发生反应的离子方程式为 ▲ 。
(2)精炼前,需清除坩埚表面的氧化铁和石英砂,防止精炼时它们分别与铝发生置换反应产生新的杂质,则铝和氧化铁反应的化学方程式为 ▲ 。
(3)将Cl2连续通入坩埚中的粗铝熔体,杂质随气泡上浮而除去。气泡的主要成分除Cl2外还含有___▲___。固态杂质粘附于气泡上,在熔体表面形成浮渣,浮渣中肯定存在____▲____。
(4)镀铝电解池中,金属铝为阳极,熔融盐电镀液中铝元素主要以AlCl4-形式存在,则阳极的电极反应式为____▲_________。
(5)钢材镀铝后,抗腐蚀性能会大大增强,其原因是____▲_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)原子序数小于36的X、 Y、Z、W四种元素,其中X是元素周期表原子半径最小的元素, Y原子基态时最外层电子数是其内层电子数的2倍,Z原子基态时2p原子轨道上有3个未 成对的电子,w的原子序数为29。回答下列问题:
①Y2X2分子中Y原子轨道的杂化类型为_________,1molY2X2含有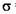 键的数目为____ __________________.
键的数目为____ __________________.
②化合物ZX3的沸点比化台物YX4的高,其主要原因是_____________。
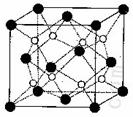 ③元素Y的一种氧化物与元素z的一种氧化物互为等电子体,元素z的这种氧化物的分子式是_____________。
③元素Y的一种氧化物与元素z的一种氧化物互为等电子体,元素z的这种氧化物的分子式是_____________。
(2)铁元素能形成多种配合物,如:Fe(CO)x
①基态Fe3+的M层电子排布式为___________________________。
②配合物Fe(CO)x的中心原子价电子数与配体提供电子数之和为
18.则x=_________。常温下呈液态,熔点为-20.5℃,沸
点为103℃,易溶于非极性溶剂,据此可判断Fe(CO)x晶体属于
(填晶体类型):
(3)O和Na形成的一种只含有离子键的离子化合物的晶胞结构如右图,距一个阴离子周围最近的所有阳离子为顶点构成的几何体为_________。已知该晶胞的密度为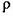 g/cm
g/cm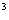 ,阿伏加德罗常数为
,阿伏加德罗常数为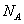 ,求晶胞边长a=________cm。(用含
,求晶胞边长a=________cm。(用含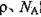 的计算式表示)
的计算式表示)
(4)下列有关的说法正确的是_____________。
A.第一电离能大小:S>P>Si
B.电负性顺序:C<N<O<F
C.因为品格能Ca0比KCl高,所以KCl比CaO熔点低
D.SO2与CO2的化学性质类似,分子结构也都呈直线型,相同条件下SO2的溶解度更大
E分子晶体中,共价键键能越大,该分子晶体的熔沸点越高
查看答案和解析>>
科目:高中化学 来源: 题型:
反应A(g)+3B(g) 2C(g)+2D(g),在不同情况下测得反应速率如下,其中化学反应速率最快的是( )
2C(g)+2D(g),在不同情况下测得反应速率如下,其中化学反应速率最快的是( )
A.v(D)=0.4 mol/(L•s) B. v(C)=0.5 mol/(L•s)
C. v(B)=0.6 mol/(L•s) D. v(A)=0.15 mol/(L•s)
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于乙烯和乙烷比较的说法中,不正确的是 ( )
A.乙烯的结构简式为CH2CH2,乙烷的结构简式为CH3CH3
B.乙烯分子中所有原子处于同一平面上,乙烷分子则为立体结构,原子不都在同一平面上
C.乙烯分子中含有碳碳双键,乙烷分子中含有碳碳单键,双键不如单键稳定,导致乙烯的性质比乙烷活泼
D.乙烯分子中因含有不饱和键,导致乙烯能使酸性KMnO4溶液和溴的四氯化碳溶液褪色
查看答案和解析>>
科目:高中化学 来源: 题型:
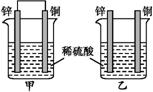
将相同表面积的纯锌片和纯铜片按图示方式插入同浓度的稀硫酸
中一段时间,下列叙述正确的是( )
A.两烧杯中铜片表面均无气泡产生
B.甲中铜片是正极,乙中铜片是负极
C.甲中铜被氧化,乙中锌被氧化
D.产生气泡的速率甲比乙大
查看答案和解析>>
科目:高中化学 来源: 题型:
A、B、C都是金属,把A浸入C的盐溶液中,A的表面有C析出,A与B和酸溶液组成原电池时,B为电池的负极。A、B、C金属的活动性顺序为 ( )
A.B>A>C B.A>C>B C.A>B>C D.B>C>A
查看答案和解析>>
科目:高中化学 来源: 题型:
在含有Ag+的酸性溶液中,以铁铵矾NH4Fe(SO4)2作指示剂,用KSCN的标准溶液滴定Ag+。已知:AgSCN(白色,s)Ag++SCN-,Ksp=1.0×10-12,Fe3++SCN-(FeSCN)2+(红色),K=138,下列说法不正确的是( )
A.边滴定,边摇动溶液,溶液中首先析出AgSCN白色沉淀
B.当Ag+定量沉淀后,少许过量的SCN-与Fe3+生成红色配合物,即为终点
C.上述实验可用KCl标准溶液代替KSCN的标准溶液滴定Ag+
D.滴定时,必须控制溶液一定的酸性,防止Fe3+水解,以免影响终点的观察
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com