
【题目】防治环境污染,改善生态环境已成为全球共识.
①下列各图中表示我国节能标志的是(填字母).
②煤矿有时会发生瓦斯爆炸事故,瓦斯的主要成分与天然气相同,写出瓦斯爆炸的化学方程式: .
③环境污染已对人类造成重大威胁.下列名词与环境污染无关的是
A.潮汐B.温室效应C.臭氧层空洞D.工业废水
④减少室内空气污染,下列措施正确的是
A、在室内种植芦荟、常青藤等绿色植物
B、随意对室内装饰,装饰材料可以随意用
C、紧闭门窗
D、室内有异味时,要即时多喷洒香水.
【答案】C;CH4+2O2 ![]() CO2+2H2O;A;A
CO2+2H2O;A;A
【解析】解:①中间有艺术字节字的是我国的节能徽记,故答案为:C;
②煤矿有时会发生瓦斯爆炸事故,瓦斯的主要成分与天然气相同为甲烷,瓦斯爆炸的化学方程式为:CH4+2O2 ![]() CO2+2H2O,故答案为:CH4+2O2
CO2+2H2O,故答案为:CH4+2O2 ![]() CO2+2H2O;
CO2+2H2O;
③A、潮汐现象是指是指海水在天体(主要是月球和太阳)引潮力作用下所产生的周期性运动,习惯上把海面垂直方向涨落称为潮汐,与环境污染无关,故A正确;
B、温室效应与二氧化碳的排放有关,导致全球温度升高,故B错误;
C、含氟冰箱能破坏臭氧层,引起臭氧层空洞,所以与环境污染有关,故C错误;
D、空气的污染途径是工厂废气的任意排放,大量燃烧化石燃料,汽车尾气的排放,所以工业工业废水与环境污染有关,故D错误;
故答案为:A;
④A.芦荟吸收室内污染性气体,对人体健康有益,故A正确;
B.很多装修材料中含有大量的甲醛、苯等有害物质,不要随意对室内装饰,故B错误;
C.居室内经常产生一些有害气体,经常通风可降低有害气体的浓度,紧闭门窗有害气体不能排出,故C错误;
D.室内洒香水,不能减少有害气体的危害,是一种掩耳盗铃的做法,对减少有害气体无益,故D错误.
故选A.
①中间有艺术字节字的是我国的节能徽记;
②瓦斯的主要成分与天然气相同为甲烷,甲烷燃烧生成二氧化碳和水;
③根据酸雨的形成与产生的二氧化硫有关、臭氧层空洞与破坏臭氧层有关、工业三废包括废水、废气、废渣都与环境污染有关;
④A.在室内种植芦荟、常青藤等绿色植物,可加强光合作用,并吸收室内污染性气体;
B.很多装修材料中含有大量的甲醛、苯等有害物质;
C.居室经常通风,可减小室内有害气体的浓度;
D.室内洒香水,不能减少有害气体的危害.


科目:高中化学 来源: 题型:
【题目】溴乙烷中含有少量乙醇杂质,下列方法中可以除去该杂质的是( )
A. 加入浓硫酸并加热到170℃,使乙醇变成乙烯而逸出
B. 加入氢溴酸并加热,使乙醇转化为溴乙烷
C. 加入金属钠,使乙醇发生反应而除去
D. 加水振荡,静置分层后,用分液漏斗分离去水层
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A、B、C、D、E都是周期表中前四周期的元素,且原子序数依次增大,其中A原子核外有三个未成对电子;A与B可形成离子化合物B3A2;C元素是地壳中含量最高的金属元素;D原子核外的M层中有两对成对电子;E原子核外最外层只有1个电子,其余各层电子均充满。请根据以上信息,回答下列问题(答题时,A、B、C、D、E用所对应的元素符号表示):
(1)比E核外电子数少5的元素的原子核外电子排布式是 ,A、B、C、D的第一电离能由小到大的顺序为 。
(2)B的氯化物的熔点远高于C的氯化物的熔点,理由是 。
(3)A的氢化物属于 (填“极性”或“非极性”)分子,D的低价氧化物分子的立体构型是 。
(4)A、E形成的某种化合物的晶胞结构如图所示,则其化学式为 (每个球均表示1个原子)。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用钛白工业的副产品FeSO4[含Al2(SO4)3和少量重金属离子],可以生产电池级高纯超微细草酸亚铁.其工艺流程如图1: 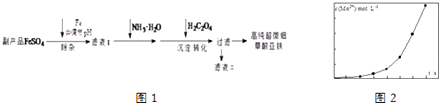
已知:①5Fe2++MnO ![]() +8H+═5Fe3++Mn2++4H2O
+8H+═5Fe3++Mn2++4H2O
②5C2O42﹣+2MnO ![]() +16H+═10CO2↑+2Mn2++8H2O
+16H+═10CO2↑+2Mn2++8H2O
(1)沉淀过程的反应温度为40℃,温度不宜过高的原因除了控制沉淀的粒径外,还有 .
(2)滤液Ⅱ经处理可得到副产品 .
(3)实验室测定高纯超微细草酸亚铁组成的步骤依次为:
步骤1:准确称量一定量草酸亚铁样品,加入25mL 2molL﹣1的H2SO4溶解.
步骤2:用0.2000molL﹣1标准KMnO4溶液滴定,消耗其体积30.40mL.
步骤3:向滴定后的溶液中加入2g Zn粉和5mL 2molL﹣1的H2SO4溶液,将Fe3+还原为Fe2+ .
步骤4:过滤,滤液用上述标准KMnO4溶液滴定,消耗溶液10.40mL.
则样品中C2O42﹣的物质的量为 .
(4)将一定量高锰酸钾溶液与酸化的草酸亚铁溶液混合,测得反应液中Mn2+的浓度随反应时间t的变化如图2,产生这种变化趋势的原因可能为
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】H2C2O4水溶液中H2C2O4、HC2O4﹣和C2O42﹣三种形态的粒子的分布分数δ随溶液pH变化的关系如图所示,下列说法正确的是( ) 
A.曲线①代表的粒子是HC2O4﹣
B.0.1molL﹣1NaHC2O4溶液中:c(C2O42﹣)>c(H2C2O4)
C.pH=5时,溶液中主要含碳微粒浓度大小关系为:c(C2O42﹣)>c(H2C2O4)>c(HC2O4﹣)
D.在一定温度下,往CaC2O4饱和溶液中加入少量CaCl2固体,c(C2O42﹣)将减小,c(Ca2+)增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氢氧化镁是一种用途广泛、极具开发前景的环保材料,广泛应用在阻燃、废水中和、烟气脱硫等方面.镁硅酸盐矿石(主要成分Mg3Si2O5(OH)4 , 含氧化铝、氧化铁、氧化亚铁等杂质)可用于生产氢氧化镁,简要工艺流程如图1: 
已知:几种金属阳离子的氢氧化物沉淀时的pH如下表所示:
Fe3+ | Al3+ | Fe2+ | Mg2+ | |
开始沉淀时 | 1.5 | 3.3 | 6.5 | 9.4 |
沉淀完全时 | 3.7 | 5.2 | 9.7 | 12.4 |
(1)对矿石焙烧的目的是 .
(2)加入H2O2溶液反应的离子方程式是 .
(3)向溶液Ⅰ中加入的X可以是 , 作用是 .
(4)加入氨水时,Mg2+转化率随温度t的变化如图2所示: ①溶液Ⅱ中发生反应的离子方程式是 .
②t1前Mg2+转化率增大的原因是;
t1后Mg2+转化率下降的原因是(用化学方程式表示) .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】脱去冶金工业排放烟气中SO2的方法有多种.
(1)利用本生(Bunsen)热化学循环吸收SO2工艺由下列三个反应组成: 2H2(g)+O2(g)═2H2O(I)△H1=﹣572kJmol﹣1
2HI(g)═H2(g)+I2(g)△H2=+10kJmol﹣1
2H2SO4(I)═2SO2(g)+2H2O(g)+O2(g)△H3=+462kJmol﹣1
则得SO2(g)+I2(g)+2H2O(I)═2HI (g)+H2SO4(I)△H=kJmol﹣1
(2)氧化锌吸收法.配制ZnO悬浊液,在吸收塔中封闭循环脱硫.测得pH、吸收效率η随时间t的变化如图1所示;溶液中部分微粒与PH的关系如图2所示. 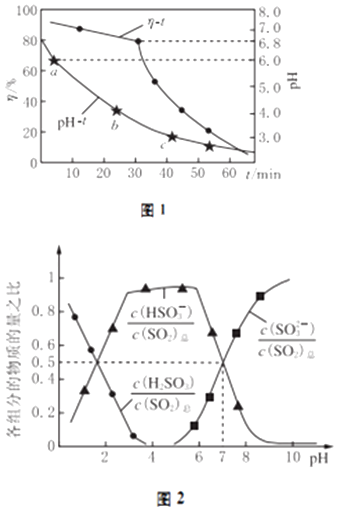
①为提高SO2的吸收效率η,可采取的措施有:增大悬浊液中ZnO的量、 .
②图1中的pH﹣t曲线ab段发生的主要化学方程式为
③pH=7时,溶液中 ![]() =
=
(3)如图3所示,利用惰性电解电解含SO2的烟气回收S及H2SO4 , 以实现废物利用. 
①阴极的电极反应式为 .
②每处理含19.2g SO2的烟气,理论上回收S、H2SO4的物质的量分别为、 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关实验室一般事故的预防和处理方法正确的是
A. 燃着的酒精灯打翻失火,应立即用水浇灭
B. 皮肤上沾有少量浓硫酸,可立即用NaOH冲洗。
C. 少量酸或碱滴到实验台上,立即用湿抹布擦净,再用水冲洗抹布
D. 蒸发食盐溶液时,发生液滴飞溅现象,应立即加水冷却
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列解释事实的方程式不正确的是( )
A.硫酸型酸雨的形成涉及反应:2H2SO3+O2 ![]() ?2H2SO4
?2H2SO4
B.SO2的水溶液显酸性:SO2+H2O?H2SO3?2H++SO32﹣
C.常温下,0.1mol/L醋酸溶液pH≈3:CH3COOH?CH3COO﹣+H+
D.Mg(OH)2固体在溶液中存在平衡:Mg(OH)2(s)?Mg2+(aq)+2OH﹣(aq),该固体可溶于NH4Cl溶液
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com