
 ;
;
分析 (1)尿素[CO(NH2)2]中C原子半径最大;
(2)①羟胺被氧化生成氮气;
②i二氧化硫和氢氧化钙反应生成盐和水;
ii电解时,得电子的微粒在阴极上发生还原反应,电解亚硝酸根离子溶液时,阴极上亚硝酸根离子得电子发生还原反应生成氮气和水.
解答 解:(1)①原子的电子层数越多,其原子半径越大,相同周期的元素中,原子半径随着原子序数的增大而减小,所以原子半径最大的元素是C元素,其原子结构示意图为 ,
,
故答案为: ;
;
(2)①羟胺被氧化生成氮气和水,反应的离子方程式为2NH2OH+2Fe3+=2Fe2++N2↑+2H2O+2H+,
故答案为:2NH2OH+2Fe3+=2Fe2++N2↑+2H2O+2H+;
②i二氧化硫和氢氧化钙反应生成盐和水,反应化学方程式:Ca(OH)2+2SO2=Ca(HSO3)2,
故答案为:Ca(OH)2+2SO2=Ca(HSO3)2;
ⅱ电解时,得电子的微粒在阴极上发生还原反应,电解亚硝酸根离子溶液时,阴极上亚硝酸根离子得电子发生还原反应生成氮气和水,电极反应式为2NO2-+8H++6e-=N2↑+4H2O,
故答案为:2NO2-+8H++6e-=N2+4H2O.
点评 本题考查氮及其化合物的知识,涉及原子结构、电解池、氧化还原反应等,注重高频考点的考查,有一定的综合性,题目难度中等.


科目:高中化学 来源: 题型:选择题
| A. | 在气体发生装置上直接点燃一氧化碳气体时,必须要先检验一氧化碳气体的纯度,最简单的方法是用排空气的方法先收集一试管气体,点燃气体,听爆鸣声 | |
| B. | 进行蒸馏操作时,冷凝管中的冷凝水应从上口进,下口出 | |
| C. | 萃取操作时,振荡过程中需要放气,通过旋转分液漏斗的上口的玻璃活塞进行 | |
| D. | 将饱和FeCl3溶液滴入沸水中,继续加热煮沸,并用玻璃棒不断搅拌直至体系呈红褐色即得Fe(OH)3胶体 |
查看答案和解析>>
科目:高中化学 来源:2017届江苏省高三上学期月考一化学试卷(解析版) 题型:选择题
下列实验“操作和现象”与“结论”对应关系正确的是
操作和现象 | 结论 | |
A | 用玻璃棒蘸取某溶液做焰色反应,可看到黄色火焰 | 溶液中一定有Na+ |
B | 向淀粉溶液中加入稀H2SO4,加热几分钟, 冷却后再加入新制Cu(0H)2浊液,加热,没有红色沉淀生成 | 淀粉没有水解成葡萄糖 |
C | 向无水乙醇中加入浓H2SO4,加热至170℃ 产生的气体通入酸性KMnO4溶液,红色褪去 | 使溶液褪色的气体一定是乙烯 |
D | 向某溶液中加稀盐酸无现象,再加入BaCl2溶液,生成白色沉淀 | 该溶液中一定含有SO42- |
查看答案和解析>>
科目:高中化学 来源:2017届河北省高三上期中化学试卷(解析版) 题型:选择题
下列有关化学用语表示正确的是
A.甲酸甲酯的结构简式:CH2O
B.Na+的结构示意图: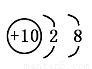
C.质子数为53、中子数为78的碘原子:13153I
D.CO2的电子式: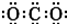
查看答案和解析>>
科目:高中化学 来源: 题型:填空题

查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 利用废铝箔(主要成分为Al、少量的Fe、Si等)既可制取有机合成催化剂AlBr3又可制取净水剂硫酸铝晶体[A12(SO4)3•18H2O].
利用废铝箔(主要成分为Al、少量的Fe、Si等)既可制取有机合成催化剂AlBr3又可制取净水剂硫酸铝晶体[A12(SO4)3•18H2O].查看答案和解析>>
科目:高中化学 来源: 题型:解答题
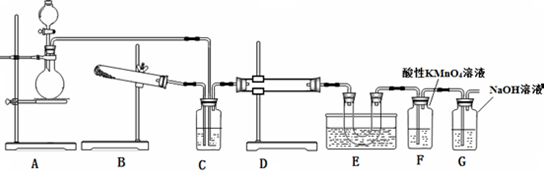
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
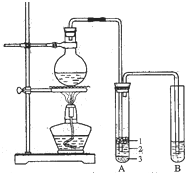 实验室制取少量溴乙烷的装置如图所示.
实验室制取少量溴乙烷的装置如图所示.查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com