
| A、0.2mol H2O2 |
| B、0.1mol H2SO4 |
| C、0.2mol NaOH |
| D、0.3mol H2O |


科目:高中化学 来源: 题型:
| A、混合气体的压强不随时间变化 |
| B、B的生成速率和D的生成速率1:1 |
| C、混合气体的密度不随时间变化 |
| D、D的分子数之比为3:2:1. |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、鉴别苯和甲苯:分别加入溴水振荡 |
| B、检验酒精中的少量水:向酒精中加入无水硫酸铜 |
| C、制备纯净的氯乙烷(C2H5Cl):将乙烷和氯气的混合气放在光照条件下反应 |
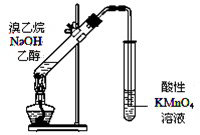
| D、证明溴乙烷与NaOH醇溶液共热生成乙烯:用如图所示的实验装置 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、298K,反应③的△H3═+47.3 kJ?mol-1 |
| B、平衡时,其他条件不变,升高温度,反应①中正反应速率加快 |
| C、平衡时,其他条件不变,增大NO2浓度可增大反应③中SO2转化率 |
| D、反应③中,每有1mol O=O键断裂,同时生成2molSO3,则该反应达平衡状态 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、在NaH中的氢离子半径比锂离子半径大 |
| B、在NaH中的氢离子的电子层排布与氦原子不相同 |
| C、NaH跟水反应后溶液呈酸性 |
| D、NaH中的氢离子被还原成氢气 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、0.25mol |
| B、1.0mol |
| C、0.65mol |
| D、0.5mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、金刚石>碳化硅>晶体硅 |
| B、氧化铝>氯化钾>氯化钠 |
| C、H2O>NH3>PH3>AsH3 |
| D、SiC>生铁>纯铁>Mg |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com