
工业制氢气的一个重要反应是: 已知在25℃时:
已知在25℃时: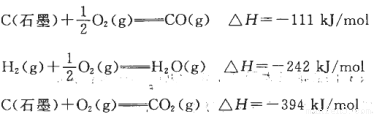
则2 5℃时1 mol CO与水蒸气作用转化为氢气和二氧化碳反应△H为
A.+41.kJ/mol B.-41kJ/mol C.283kJ/mol D.-131kJ/mol
科目:高中化学 来源:2015-2016学年山西大学附属中学高一上学期第一次月考化学试卷(解析版) 题型:选择题
某溶液中含有较高浓度的Cl﹣、CO32﹣、OH﹣等3种阴离子,如果只取一次该溶液就能够分别将3种阴离子依次检验出来,下列实验操作顺序正确的是
①滴加Mg(NO3)2溶液;②过滤;③滴加AgNO3溶液;④滴加Ba(NO3)2溶液
A.①②④②③ B.④②①②③
C.①②③②④ D.④②③②①
查看答案和解析>>
科目:高中化学 来源:2016届湖南省浏阳市高三上学期第二次月考化学试卷(解析版) 题型:选择题
下列实验装置不能达到实验目的的是

A.比较非金属性强弱:S > C > Si
B.分离CH3COOC2H5和饱和碳酸钠溶液
C.观察纯碱的焰色反应
D.比较Na2CO3和NaHCO3的热稳定性
查看答案和解析>>
科目:高中化学 来源:2016届湖南省衡阳市高三上学期第三次月考化学试卷(解析版) 题型:选择题
实验室保存下列药品的方法,正确的是
A.氢氟酸贮存在细口玻璃瓶里
B.盛溴的试剂瓶里加一些水来防止溴挥发
C.盛放浓硫酸的广口瓶应当用磨口玻璃塞,不能用橡皮塞
D.氯水保存在无色玻璃瓶中;液氯存贮存在钢瓶里
查看答案和解析>>
科目:高中化学 来源:2015-2016学年广东省高一上学期第一次月考化学试卷(解析版) 题型:选择题
下列物质的分离方法不正确的是
A.用过滤的方法除去食盐水中的泥沙
B.用蒸馏的方法将自来水制成蒸馏水
C.用酒精萃取碘水中的碘
D.用淘洗的方法从沙里淘金
查看答案和解析>>
科目:高中化学 来源:2016届安徽省安庆市高三上学期第一次质检化学试卷(解析版) 题型:选择题
下列说法正确的是
A.工业用电解熔融AlCl3的方法制金属铝
B.铅蓄电池工作时,正极反应为:PbO2+2e-+4H++SO42-=PbSO4+2H2O
C.电解饱和食盐水时,用铁作阳极,Cl-发生氧化反应
D.电解精炼铜时,阳极泥中含有Zn、Fe、Ag、Au等金属
查看答案和解析>>
科目:高中化学 来源:2016届吉林省扶余市高三上学期第一次月考化学试卷(解析版) 题型:填空题
(15分)有以下六种元素:A是宇宙中最轻的元素。D原子核外有1个未成对电子,D+比E原子少一个电子层,E原子得一个电子填入3P轨道后,3P轨道呈全充满状态。G原子2P轨道有2个未成对电子,M的最高化合价和最低化合价的代数和为4,与G的原子序数差8.
L位于周期表第四周期、第12纵行且是六种元素中原子序数最大的。R是由M、L形成的化合物,其晶胞结构如图所示,
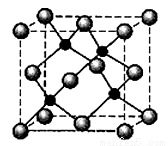
请回答下列问题:
(1)E元素的电负性____________(填“>”“<”或“=”)M元素的电负性。
(2)G的第一电离能比它同周期前一族相邻元素的第一电离能____________(填“大”或“小”)。
(3)M2E2广泛用于橡胶工业,在该化合物分子中,所有原子最外层均满足8电子稳定结构。则在M2E2分子中M原子的杂化类型是__________,M2E2是___________(填“极性”或“非极性”)分子。
(4)L的外围电子排布式为____________,该元素位于周期表中的____________族。
(5)R的化学式为________________(用元素符号表示),属于____________晶体。
已知R晶体的密度为ρ g.cm-3,则该晶胞的边长a____________cm。(阿常数用NA表示)
查看答案和解析>>
科目:高中化学 来源:2016届河北省邯郸市高三上学期10月月考化学试卷(解析版) 题型:选择题
下列正确的叙述有
①CO2、NO2、P2O5均为酸性氧化物
②Ca(HCO3)2、Fe(OH)3、FeCl2均可由化合反应制得
③碘晶体分散到酒精中、饱和氯化铁溶液滴入沸水中所形成的分散系分别为:溶液、胶体
④金属元素和非金属元素形成的化合物一定是离子化合物
⑤苛性钾、次氯酸、氯气按顺序分类依次为:强电解质、弱电解质和非电解质.
A.①②③⑤ B.②③⑤ C.②③ D.全部
查看答案和解析>>
科目:高中化学 来源:2015-2016学年湖南省高二上学期第一次月考化学试卷(解析版) 题型:选择题
2.0molPCl3和1.0molCl2充入体积不变的密闭容器中,在一定条件下发生下述反应PCl3(g)+Cl2(g) PCl5(g),达平衡时PCl5为0.4mol,如果此时移走1.0molPCl3和0.5molCl2,在相同温度下再达平衡时PCl5物质的量是
PCl5(g),达平衡时PCl5为0.4mol,如果此时移走1.0molPCl3和0.5molCl2,在相同温度下再达平衡时PCl5物质的量是
A.0.4 mol B.0.2 mol
C.小于0.2 mol D.大于0.2 mol小于0.4mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com