
【题目】某小组报用含稀硫酸的KMnO4,溶液与H2C2O4溶液(弱酸)的反应(此反应为放热反应)来探究"条件对化学反应速率的影响",并设计了如表的方案记录实验结果(忽略溶液混合体积变化),限选试剂和仪器:0.2mol L-1H2C2O4溶液、0.010mol·L-1KMnO4溶液(酸性)、蒸馏水、试管、量筒、秒表、恒温水浴槽
项目 | V(0.2mol L-1H2C2O4溶液)/mL | V(蒸馏水)/mL | V(0.010mol·L-1KMnO4溶液)/mL | M(MnSO4固体)/g | T/℃ | 乙 |
① | 2.0 | 0 | 4.0 | 0 | 50 | |
② | 2.0 | 0 | 4.0 | 0 | 25 | |
③ | 1.0 | a | 4.0 | 0 | 25 | |
④ | 2.0 | 0 | 4.0 | 0.1 | 25 |
回答下列问题
(1完成上述反应原理的化学反应方程式____________________________________
(2)上述实验①②是探究___________对化学反应速率的影响;若上述实验②③是探究浓度的对化学反应速率的影响,则a为______;乙是实验需要测量的物理量,则表格中“乙”应填写_______;上述实验②④是探究__________对化学反应速率的影响
(3)已知草酸为二元弱酸,其电离方程式为___________________________
【答案】5H2C2O4+2KMnO4+3H2SO4═10CO2↑+2MnSO4+K2SO4+8H2O 温度 1.0 溶液褪色时间/s 催化剂 H2C2O4 ![]() HC2O4-+ H+ , HC2O4-
HC2O4-+ H+ , HC2O4- ![]() H++C2O42-
H++C2O42-
【解析】
(1)酸性高锰酸钾是用稀硫酸酸化,混合溶液发生氧化还原反应,KMnO4被还原为MnSO4,H2C2O2被氧化为CO2,根据得失电子数守恒和原子守恒写出反应方程式;
(2)当探究某一种因素对反应速率的影响时,必须保持其他影响因素一致;要探究H2C2O4溶液浓度不同对反应速率的影响,则加入的H2C2O4溶液的体积不同,但反应体积溶液的总体积需相同,故应加入蒸馏水来确保溶液的总体积均为6mL;要准确描述反应速率的快慢,必须准确测得溶液褪色时间的长短;④中加了MnSO4固体,锰离子对该反应起催化作用;
(3)草酸是二元弱酸,应分步电离。
(1)酸性高锰酸钾是用稀硫酸酸化,H2SO4、KMnO4与H2C2O2发生反应,KMnO4被还原为MnSO4,化合价降低5价,H2C2O2被氧化为CO2,每个C原子的化合价升高1价,1个H2C2O2升高2价,则高锰酸钾与草酸计量数之比为2:5,根据原子守恒配平可得:5H2C2O4+2KMnO4+3H2SO4═10CO2↑+2MnSO4+K2SO4+8H2O;
(2)当探究某一种因素对反应速率的影响时,必须保持其他影响因素一致,通过比较实验①②的反应条件可知,实验①②可探究温度对反应速率的影响;实验②③中的H2C2O4溶液的加入体积不同,故要探究H2C2O4溶液浓度不同对反应速率的影响,但反应体积溶液的总体积需相同,故应加入蒸馏水来确保溶液的总体积均为6.0mL,则a的值为1.0;要准确描述反应速率的快慢,必须准确测得溶液褪色时间的长短,故乙要测量的物理量是溶液褪色的时间(t溶液褪色时间·s-1);其他条件相同,④中加了MnSO4固体,锰离子对该反应起催化作用,则②④探究的是催化剂对反应速率的影响;
(3)草酸(H2C2O4)是一种二元弱酸,分步电离,电离方程式为:H2C2O4 ![]() HC2O4-+ H+ , HC2O4-
HC2O4-+ H+ , HC2O4- ![]() H++C2O42-
H++C2O42-


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】青蒿素是从黄花蒿中提取的一种无色针状晶体,其结构如图1,请回答下列问题:
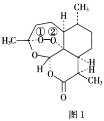
(1)基态O原子的价电子排布图为___。
(2)组成青蒿素的三种元素中电负性最大的是__(填元素符号,下同),第一电离能最大的是__。
(3)基态N原子的未成对电子数为___。
(4)双氢青蒿素是青蒿素的重要衍生物,其抗疟疾疗效优于青蒿素,双氢青蒿素的合成一般是在相转移催化剂聚乙二醇的作用下,用硼氢化钠(NaBH4)还原青蒿素。两种硼氢化物的合成原理如下:
2LiH+B2H6=2LiBH4;4NaH+BF3=NaBH4+3NaF
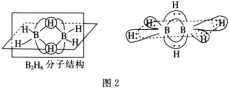
BH4-的空间构型为__;B2H6分子的结构如图2,B2H6中B的杂化方式为__。
聚乙二醇[HO(CH2CH2O)nH]随着n值的增大,水溶性降低,原因是___。
(5)NaH的晶胞与NaCl相同,NaH晶体中阳离子的配位数是__;设晶胞中阴、阳离子为刚性球体且恰好相切,阴、阳离子的半径比约为__(已知![]() ≈1.414,结果保留三位有效数字)。
≈1.414,结果保留三位有效数字)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碘化钠在光学器件石油探测、安检、环境监测等领域有重要应用。某研究小组开发设计的制备高纯NaI的简化流程如图:

已知:
①I2(s)+I-(aq)![]() I3-(aq)。
I3-(aq)。
②水合肼(N2H4H2O)具有强还原性,可分别将碘的各种酸根和I2还原为I-,本身被氧化为无毒物质。
③NaI易溶于水,也易溶于酒精,在酒精中的溶解度随温度的升高增加不大。
请回答:
(1)步骤Ⅰ,I2与NaHCO3溶液发生歧化反应,生成物中含IO-和IO3-离子。
①I2与NaHCO3溶液反应适宜温度为40~70℃,则采用的加热方式为___。
②实验过程中,加少量NaI固体能使反应速率加快,其原因是___。
(2)步骤Ⅱ,水合肼与IO反应的离子方程式为___。
(3)步骤Ⅲ,多步操作为:
①将步骤Ⅱ得到的pH为6.5~7的溶液调整pH值至9~10,在100℃下保温8h,得到溶液A;
②将溶液A的pH值调整至3~4,在70~80℃下保温4h,得溶液B;
③将溶液B的pH调整至6.5~7,得溶液C;
④在溶液C中加入活性炭,混合均匀后煮沸,静置10~24h后,过滤除杂得粗NaI溶液。上述①②③操作中,调整pH值时依次加入的试剂为___。
A.NaOH B.HI C.NH3H2O D.高纯水
(4)步骤Ⅳ,采用改进的方案为用“减压蒸发”代替“常压蒸发”。
①“减压蒸发”需选用的仪器除了圆底烧瓶、蒸馏头、温度计、接收管、接收瓶之外,还有___。
A.直形冷凝管 B.球形冷凝管 C.烧杯 D.抽气泵
②采用“减压蒸发”的优点为___。
(5)将制备的NaI2H2O粗品以无水乙醇为溶剂进行重结晶。请给出合理的操作排序___。
加热乙醇→ → → → →纯品(选填序号)。
①高纯水洗涤 ②减压蒸发结晶 ③NaI2H2O粗品溶解 ④趁热过滤 ⑤真空干燥 ⑥抽滤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图中,A为一种中学化学中常见的单质,B、C、D、E是含有A元素的常见化合物。它们的焰色反应均为黄色。
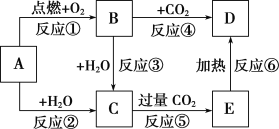
(1)以上6个反应中属于氧化还原反应的有________(填写编号)。
(2)B中阴、阳离子数目比为________。
(3)写出A→C反应的化学方程式__________________________________。
(4)写出B→C反应的离子方程式:________________________________。
(5)写出C→E反应的离子方程式:________________________________。
(6)加热5.00 g D和E的固体混合物,使E完全分解,固体混合物的质量减少了0.62 g,则原混合物中D的质量分数为_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】生产生活中常用84消毒液杀菌消毒。化学课外小组用Cl2和NaOH固体、水制取84消毒液。请回答下列问题:
(1)实验室制取Cl2的化学方程式为________,收集Cl2应使用_____法,要得到干燥的Cl2可选用_____作干燥剂,标准状况下,4.48LCl2的物质的量为______mol。
(2)制取84消毒液需要4.0mol·L-1的NaOH溶液100mL,配制时称量NaOH固体的质量为_____g,配制过程中使用的玻璃仪器有烧杯、玻璃棒、胶头滴管、_______。
(3)制取84消毒液的离子方程式为_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向一定体积的Ba(OH)2溶液中逐滴加入稀硫酸,测得混合溶液的导电能力随时间变化 的曲线如右图所示,下列说法正确的是
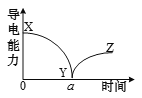
A.XY段溶液的导电能力不断减弱,说明H2SO4不是电解质
B.a时刻表明参加反应的两种溶液的体积相等
C.Y处溶液的导电能力约为0,说明溶液中几乎没有自由移动的离子
D.YZ段溶液的导电能力不断增大,主要是由于Ba(OH)2电离出的离子导电
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机化合物J是治疗心脏病药物的一种中间体,分子结构中含有3个六元环。合成路线如图:
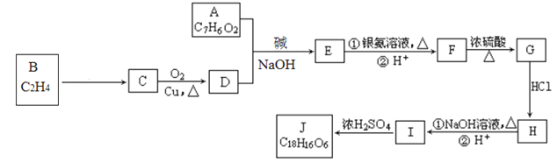
已知:R1—CHO+ R2—CH2—CHO![]()
![]() 。
。
请回答:
(1)已知:A能发生银镜反应,与![]() 溶液发生显色反应,核磁共振氢谱显示有4组峰,峰面积之比为1:2:2:1,则A的结构简式是__。
溶液发生显色反应,核磁共振氢谱显示有4组峰,峰面积之比为1:2:2:1,则A的结构简式是__。
(2)J的结构简式是__,G所含官能团的名称是__。
(3)写出A与D反应生成E的化学方程式__,H→I的反应类型是__。
(4)符合下列条件E的酸化产物的同分异构体有__种。
①苯环上有2个取代基②能遇FeCl3溶液发生显色反应③能发生水解反应
(5)结合题中给信息,设计以C2H4为原料反应制备1,3-丁二烯的合成路线___(其他试剂任选)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子组加入相应试剂后,发生反应的离子方程式正确的是( )
离子组 | 加入试剂 | 离子方程式 | |
A | Na+、 | Ba(OH)2溶液 | 2Na++ |
B | H+、Cl- | 足量石灰乳 | 2H++2OH-=2H2O |
C | K+、 | NaHSO4溶液 |
|
D | Ag+、 | 少量盐酸 | Ag++ |
A.AB.BC.CD.D
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com