
【题目】下列离子方程式书写正确的是( )
A. 氢氧化钡溶液中加入硫酸铵:Ba2++OH-+NH4++SO42-=BaSO4↓+NH3·H2O
B. 用惰性电极电解CuCl2溶液:Cu2++2Cl-+2H2O![]() Cu(OH)2↓+H2↑+Cl2↑
Cu(OH)2↓+H2↑+Cl2↑
C. 向漂白粉溶液中通入少量二氧化硫:Ca2++2ClO-+SO2+H2O=CaSO3↓+2HClO
D. 向苯酚钠溶液中通入少量的CO2:C6H5O-+CO2+H2O→C6H5OH+HCO3-
【答案】D
【解析】
A.该反应不符合正确配比,离子方程式为Ba2++2OH-+2NH4++SO42-=BaSO4↓+2NH3H2O,故A错误;
B.用惰性电极电解饱和CuCl2溶液时,阴极上Cu2+放电能力大于H+,阳极上氯离子放电,所以电解氯化铜本身,电解反应的离子方程式为Cu2++2Cl- ![]() Cu+Cl2↑,故B错误;
Cu+Cl2↑,故B错误;
C.向漂白粉溶液中通入少量二氧化硫,发生氧化还原反应,离子方程式为SO2+Ca2++3ClO-+H2O=CaSO4↓+2HClO+Cl-,故C错误;
D.苯酚钠溶液中通入少量CO2,反应生成苯酚和碳酸氢钠,反应的离子方程式为:C6H5O-+CO2+H2O→C6H5OH+HCO3-,故D正确;
答案选D。


科目:高中化学 来源: 题型:
【题目】下列变化为放热反应的是( )
A.H2O(g)=H2O(l) △H=-44.0 kJ/mol
B.2HI(g)=H2(g)+I2(g) △H=+14.9 kJ/mol
C.形成化学键时共放出能量862 kJ的化学反应
D.能量变化如图所示的化学反应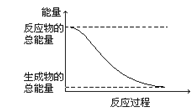
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是( )
A.金刚石晶体中的最小碳原子环由6个碳原子构成
B.金刚石晶体中的碳原子是sp2杂化的
C.12g金刚石中含有C-C键的个数为4NA
D.金刚石化学性质稳定,即使在高温下也不会和O2反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有关氨气的实验较多,对这些实验的实验原理的分析中,正确的是
A.氨气极易液化的性质可以解释氨气的喷泉实验
B.氨气的还原性可以解释氨气与氯化氢的反应实验
C.NH3H2O的热不稳定性可以解释实验室中用加热氨水的方法制取氨气
D.铵盐的水溶性大是实验室中用NH4Cl和Ca(OH)2的混合物制取氨气的原因
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将2.56 g Cu和一定量的浓硝酸反应,随着Cu的不断减少,反应生成气体的颜色逐渐变浅,当Cu反应完毕时,共收集到气体1.12 L(标准状况),则反应中消耗HNO3的物质的量为 ( )
A.0.13 molB.1 molC.1.05 molD.0.05 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机物R的结构如右所示。下列说法不正确的是

A. R的分子式为C9H8O5
B. R分子中的所有原子可能共平面
C. R能发生酯化、水解、加成反应
D. 与R含有相同取代基的苯环上的位置异构体还有9种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图中的实线表示元素周期表的边界。①~⑧分别表示元素周期表中对应位置的元素。

(1)上述元素所能形成的简单离子中半径最小的是________(填离子符号),最高价氧化物对应水化物酸性最强的是________(填分子式)。
(2)写出④与⑥形成的化合物的形成过程____________________
(3)元素①的氢化物电子式为______________。
(4)④、⑤、⑥各自的最高价氧化物对应的水化物两两皆能反应,它们反应的离子方程式为____________,______________,_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“绿色化学实验”已走进课堂,下列做法符合“绿色化学”的是

①实验室收集氨气采用图1所示装置
②实验室做氯气与钠的反应实验时采用图2所示装置
③实验室中用玻璃棒分别蘸取浓盐酸和浓氨水做氨气与酸生成铵盐的实验
④实验室中采用图3所示装置进行铜与稀硝酸的反应
A. ②③④B. ①②③C. ①②④D. ①③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮的氧化物是造成大气污染的主要物质。研究氮氧化物的反应机理对于消除环境污染有重要意义。回答下列问题:
(1)已知2NO2(g)=N2O4(g) △H=-55.3kJ/mol;N2O5(g)=2NO2 (g)+![]() O2(g) △H=+53.1 kJ/mol;写出N2O5分解生成N2O4与O2的热化学方程式________________
O2(g) △H=+53.1 kJ/mol;写出N2O5分解生成N2O4与O2的热化学方程式________________
(2)一定温度下2N2O5(g)=4NO2(g)+O2(g),在恒容密闭容器中充入一定量N2O5进行该反应,能判断反应已达到化学平衡状态的是______(填字母序号)。
a.NO2和O2的浓度比保持不变 b.容器中压强不再变化
c.2v正(NO2)=v逆(N2O5) d.气体密度不变
(3)以乙烯(C2H4)作为还原剂脱硝(NO),脱硝机理如图1。若反应中n(NO)︰n(O2)=2︰1,则总反应的化学方程式为_____;脱硝率与温度、负载率(分子筛中催化剂的质量分数)的关系如图2,为达到最佳脱硝效果,应采用的条件是负载率____温度____。

(4)T温度时在容积为2L的恒容密闭容器中发生反应:2NO(g)+O2(g)![]() 2NO2(g) △H<0。实验测得:v正=v(NO)消耗=2v(O2)消耗=k正c2(NO)·c(O2),v逆=(NO2)消耗=k逆c2(NO2),k正、k逆为速率常数只受温度影响。不同时刻测得容器中n(NO)、n(O2)如表:
2NO2(g) △H<0。实验测得:v正=v(NO)消耗=2v(O2)消耗=k正c2(NO)·c(O2),v逆=(NO2)消耗=k逆c2(NO2),k正、k逆为速率常数只受温度影响。不同时刻测得容器中n(NO)、n(O2)如表:

①从0~2s内该反应的平均速率v(NO)=________。
②T1温度时化学平衡常数K=_________ (结果保留3位有效数字)。
③若将容器的温度改变为T2时其k正=k逆,则T2_______T1(填“>”、“<”或“=")
④已知2NO(g)+O2(g)![]() 2NO2的反应历程为:
2NO2的反应历程为:
第一步NO+NO![]() N2O2 快速平衡 第二步N2O2+O2→2NO2 慢反应
N2O2 快速平衡 第二步N2O2+O2→2NO2 慢反应
下列叙述正确的是________(填标号)。
A.v(第一步的正反应)<v(第二步的反应) B.总反应快慢由第二步决定
C.第二步的活化能比第一步的高 D.第二步中N2O2与O2的碰撞100%有效
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com