
【题目】T ℃时,将5mol A和7mol B气体通入体积为10L的密闭容器中(容积不变),反应过程中A、B、C的浓度变化如图Ⅰ所示。若保持其他条件不变,温度分别为T1和T2时,B的体积分数与时间关系如图Ⅱ所示:
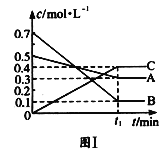
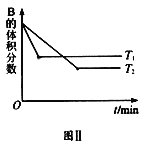
则下列结论正确的是( )
A.T ℃时,将4mol A、4mol B和2mol C气体通入体积为10L的密闭容器中(容积不变),达到平衡时,C的浓度为0.4 mol·L-1
B.保持其他条件不变,在(t1+10)min 时,加入催化剂,平衡向正反应方向移动
C.保持其他条件不变,在(t1+10)min 时,通入稀有气体,平衡向逆反应方向移动
D.保持其他条件不变,升高温度,正、逆反应速率均增大,A的转化率也增大
【答案】A
【解析】
反应达到平衡状态时,A浓度的变化量=(0.50.3)mol/L=0.2mol/L,B浓度的变化量=(0.70.1)mol/L=0.6mol/L,C浓度的变化量=(0.40)mol/L=0.4mol/L,同一化学反应同一时间段内,各物质浓度的变化量之比等于其计量数之比,所以该反应方程式为:A(g)+3B(g)2C(g),根据“先拐先平数值大”结合图II知,T1>T2,升高温度,B的体积发生增大,则该反应的正反应是放热反应。
A. 根据图I知,化学平衡常数K=(0.4)2/0.3×(0.1)3,
假设C的平衡浓度是0.4mol/L,
A(g)+3B(g)2C(g),
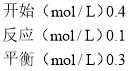
![]()
![]()
化学平衡常数K′=(0.4)2/0.3×(0.1)3,所以符合平衡常数K,故A正确;
B. 因为催化剂只改变反应速率,不改变平衡移动,所以在(t1+10)min时,加入催化剂,平衡不移动,故B错误;
C. 密闭容器中,通入稀有气体,各物质的浓度不变,平衡不移动,所以在(t1+10)min时,通入稀有气体,平衡不移动,故C错误;
D. 其它条件不变,升高温度,正逆反应速率都增大,平衡向吸热反应方向移动,根据图II知,正反应是放热反应,所以平衡向逆反应方向移动,A的转化率降低,故D错误;
故选A


科目:高中化学 来源: 题型:
【题目】利用SCR技术可有效降低柴油发动机NOx排放。SCR工作原理为尿素[CO(NH2)2]水溶液热分解为NH3和CO2,再利用NH3转化NOx,装置如图所示,下列说法不正确的是( )

A.转化NO2过程的化学方程式为:8NH3+6NO2![]() 7N2+12H2O
7N2+12H2O
B.转化器工作过程中,当转移0.6mol电子时,会消耗4.48LNH3
C.尿素水溶液热分解反应不属于氧化还原反应
D.该装置转化NO时,还原剂与氧化剂物质的量之比为2:3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】美国斯坦福大学的工程师设计出一种从污水“提取”潜在电能的新型微生物电池,该电池能将生活污水中的有机物分解同时发电,电池结构如图所示。已知a电极为惰性材料,b电极为Ag2O。下列说法不正确的是( )
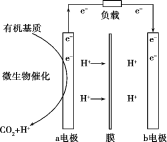
A.a电极是负极,b电极是正极
B.b电极发生的反应是Ag2O+2e-+2H+=2Ag+H2O
C.a电极每生成标准状况下2.24LCO2,可向b电极转移0.1mol电子
D.高温条件下,该电池不能正常工作
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,下列各组离子在指定溶液中一定能大量共存的是( )
A.水电离的c(H+)=10-13 mol/L 的溶液中:Na+、K+、![]() 、
、![]()
B.pH=7的溶液中:Na+、Fe3+、Cl-、![]()
C.常温下的溶液中:Cl-、Al3+、Na+、![]()
D.c(H+)=1×10-12mol/L的溶液中:K+、ClO-、![]() 、
、![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有A、B、C、三种元素,已知C原子最外层电子数为次外层电子数的3倍;B和C原子核外电子层数相等,而最外层电子数之和为10;A、C能形成AC型化合物,A2+离子和B原子电子层数也相同。回答:
(1)画出A2+离子的结构示意图 _____________________;
(2)A、B、C三元素符号分别为___________ 、_____________ 、__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学用滤纸折成一个纸蝴蝶,并喷洒一种溶液(保持湿润),挂在铁架台上,将盛某种溶液的烧杯放在纸蝴蝶的下方,如图所示。向烧杯中加入另一种物质,过一会儿发现纸蝴蝶变为红色且保持红色不变,下面的组合能够实现上述变化的是( )
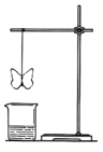
A | B | C | D | |
纸蝴蝶上的喷洒液 | 石蕊 | 酚酞 | 酚酞 | 石蕊 |
烧杯中的溶液 | 浓硫酸 | 氯化铵 | 稀硫酸 | 高锰酸钾 |
加入烧杯中的物质 | 铜 | 氢氧化钠浓溶液 | 氨水 | 浓盐酸 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验过程中产生的现象与对应的图形相符的是( )
A.  NaHSO3 粉末加入HNO3溶液中B.
NaHSO3 粉末加入HNO3溶液中B. 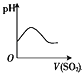 SO2气体通入新制氯水中
SO2气体通入新制氯水中
C. 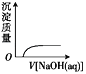 NaOH溶液滴入 Ba(HCO3)2溶液中D.
NaOH溶液滴入 Ba(HCO3)2溶液中D.  CO2气体通入澄清石灰水中
CO2气体通入澄清石灰水中
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】德国化学家哈伯(F. Haber, 1868-1930)发明的合成氨技术使大气中的氮气变成了生产氮肥的永不枯竭的廉价来源,从而使农业生产依赖土壤的程度减弱,解决了地球上因粮食不足导致的饥饿和死亡问题。因此这位解救世界粮食危机的化学天才获得了1918年诺贝尔化学奖。现在我们在实验室模拟工业制氨的过程,以探究外界条件对平衡的影响。
查阅资料,获得以下键能数据:
化学键 | N≡N | H-H | N-H |
键能/(kJ/mol) | 946 | 436 | 391 |
(1)计算工业合成氨反应的反应热:N2(g)+3H2(g)2NH3(g)△H=________kJ/mol
(2)一定温度下,向一个恒压容器中充入N20.6mol,H20.5mol,在一定温度下进行反应:N2(g)+3H2(g) 2NH3(g),达到平衡时,N2的转化率为![]() ,此时容器的体积为1L。
,此时容器的体积为1L。
该温度时容器中平衡体系的平衡常数是______________。
(3)合成氨工业会产生大量副产物CO2,工业上常用高浓度的K2CO3溶液吸收CO2,得溶液X,再利用电解法K2CO3溶液再生,其装置如图所示:
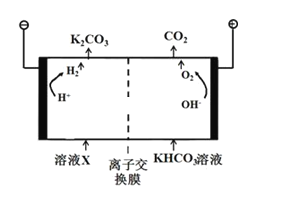
①在阳极区发生的反应包括____________________和H++HCO3- ═H2O+CO2↑。
②简述CO32-在阴极区再生的原理__________。
③再生装置中产生的CO2和H2在一定条件下反应生成甲醇,工业上利用该反应合成甲醇。
已知:25 ℃,101 KPa下:
2H2(g)+ O2(g)═2H2O(g) Δ H1═-484kJ/mol
2CH3OH(g)+ 3O2(g)═2CO2(g)+4H2O(g) Δ H2═-1352kJ/mol
写出CO2和H2生成CH3OH(g)和H2O(g)的热化学方程式__________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com