
����Ŀ��Fe�����岻��ȱ�ٵ���Ԫ�أ����뺬��������ɲ�������������������(FeSO4��7H2O)��ҽҩ������Ѫ����ij����С��ⶨ�ò�Ѫ������Ԫ�صĺ�����ʵ�鲽�����£���

��ش��������⣺
��1��������м�������NaOH��������Ҫ��Ӧ�����ӷ���ʽΪ______________��������з�Ӧ�Ļ�ѧ����ʽΪ_____________________��
��2���������һϵ�д����IJ������裺___________��ϴ�ӡ�___________����ȴ��������
��3��ʵ��������98%Ũ����(�ܶ�1.84g/mL)����1mol/L��ϡ����480mL������ʱ�õ��IJ�����������Ͳ���ձ�����ͷ�ιܡ����������___________��������Ͳ��ȡŨ����________mL��
��4����ʵ������ģ���ÿƬ��Ѫ������Ԫ�ص�����___________g(�ú�a�Ĵ���ʽ��ʾ)
���𰸡�Fe2++2OH-=Fe(OH)2�� 4Fe(OH)2+O2+2H2O=4Fe(OH)3 ���� ���� 500mL����ƿ 27.2mL 0.07a
��������
��1��������м�������NaOH�������������������Ʒ�Ӧ���������������������������������е�������������������Ҫ��Ӧ�����ӷ���ʽΪFe2++2OH-=Fe(OH)2����4Fe(OH)2+O2+2H2O=4Fe(OH)3���ʴ�ΪFe2++2OH-=Fe(OH)2����4Fe(OH)2+O2+2H2O=4Fe(OH)3��
��2���������һϵ�д�������������������Һ����ת��Ϊ����������Ҫ���ˡ�ϴ�ӵ�����������Ȼ��������������������ȴ��������������������ʴ�Ϊ���ˣ����գ�
��3������480mL 1mol/L��ϡ���ᣬ����ʱ��Ҫ�������в������ձ�����ͷ�ιܡ�500mL����ƿ����Ͳ��Ũ��������ʵ���Ũ��=![]() =
=![]() =18.4mol/L������480mL 1mol/L��ϡ���ᣬ������Ͳ��ȡŨ��������=
=18.4mol/L������480mL 1mol/L��ϡ���ᣬ������Ͳ��ȡŨ��������=![]() =0.0272L=27.2mL���ʴ�Ϊ500mL����ƿ��27.2mL��
=0.0272L=27.2mL���ʴ�Ϊ500mL����ƿ��27.2mL��
��4��ag����������Ԫ�ص�������Ϊ10Ƭ��Ѫ������������������ÿƬ��Ѫ������Ԫ�ص�����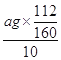 =0.07ag���ʴ�Ϊ0.07a��
=0.07ag���ʴ�Ϊ0.07a��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij����ャҺ��Al(OH)3��MnO2������Na2CrO4�����ǵ��������������ʹNa2CrO4������ȫ��ˮ������ij�о�С��������Ƶĵ�����װ�ã���ͼ2����ʹ��Һ����ɹ�������ͺ���Ԫ����Һ�����������á��ش��͢��е����⡣
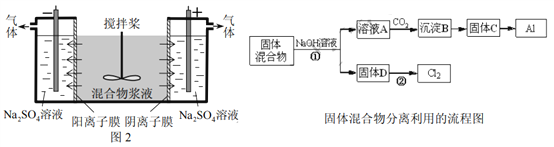
��������ķ�������ã�����ͼ�еIJ��ַ�������ͷ�Ӧ����δ������
��1����Ӧ�������Լ�NaOH�ĵ���ʽΪ_________��B��C�ķ�Ӧ����Ϊ__________��C��Al���Ʊ�������Ϊ______________��
��2����С��̽����Ӧ�ڷ�����������D��Ũ�����ϣ������ȣ��ޱ仯��������Cl2���ɣ�����Ӧֹͣ������ʣ�࣬��ʱ�μ����ᣬ�ֲ���Cl2���ɴ��ж�Ӱ��÷�Ӧ��Ч���е������У�����ţ�___________��
a���¶� b��Cl-��Ũ�� c����Һ�����
��3��0.1 mol Cl2�뽹̿��TiO2��ȫ��Ӧ������һ�ֻ�ԭ�������һ����ˮ���TiO2��xH2O��Һ̬���������4.28 kJ���÷�Ӧ���Ȼ�ѧ����ʽΪ__________��
����Ԫ����Һ�ķ��������
��4���ö��Ե缫���ʱ��CrO42-�ܴӽ�Һ�з��������ԭ����__________�������Ԫ�ص�������_________�����������ɵ�����Ϊ___________��д��ѧʽ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����1��ָ������ͼʵ��װ���еĴ���֮��(����װ�����ձ��ײ��ѵ���ʯ����)
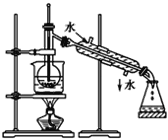
��_____________����_________��
��2��ͼ��ijѧ���Ĺ��˲���ʾ��ͼ����������淶����______

a ©���¿ڼ��δ�����ձ��� b ����������������
c ����ֽʪ��ʹ�����©���� d ��ֽ��Ե����©���ڱ�Ե
e �ò�������©������������Լӿ�����ٶ�
��.��������ȡ���������ͼ����֪�������̷�����Ӧ�Ļ�ѧ����ʽΪ��Cl2+2KI=2KCl+I2����ش��������⣺


��1��ָ����ȡ��Ĺ������й�ʵ������ٺ͢ڵ����ƣ�__________��________��
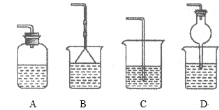
��2����3 mL�����ˮ��Һ�м���1mL���Ȼ�̼�����ú�۲쵽�Թ���ķֲ���������ͼ�е�_____(ע���Թ�����ɫ��Ϊ��ɫ��Һ)���ϲ���ɫ��Һ��������_____�²���ɫ��_____��
��3���Ӻ�����л���Һ����ȡ��ͻ����л��ܼ������辭���IJ�����_______��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����л�ѧ��Ӧ�����ӷ���ʽ��ȷ����( )
A��0.01mol/L NH4Al(SO4)2��Һ��0.02mol/L Ba(OH)2��Һ��������NH4++Al3++2SO42��+2Ba2++4OH��=2BaSO4��+Al(OH)3��+NH3H2O
B��Na2O2����H218O����2Na2O2+2H218O=4Na++4OH��+18O2��
C��NH4HCO3��Һ�����NaOH��Һ������NH4++OH��![]() NH3��+H2O
NH3��+H2O
D��Ũ�����м���������۲�������Fe+3NO3��+6H+![]() Fe3++3NO2��+3H2O
Fe3++3NO2��+3H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ﮡ�ͭ����ȼ�ϵ���ǵͳɱ���Ч��ء��õ��ͨ��һ�ָ��ӵ�ͭ����ʴ������������ܣ����зŵ����Ϊ2Li��Cu2O��H2O===2Cu��2Li+��2OH��������˵������ȷ����
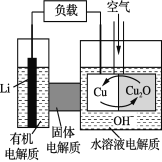
A. �ŵ�ʱ��Li+������������Cu���ƶ�
B. ͨ����ʱ��ͭ����ʴ������Cu2O
C. �ŵ�ʱ�������ĵ缫��ӦʽΪ:Cu2O��2H+ +2 e- ===2Cu��H2O
D. ������Ӧ�����У�������ΪO2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ʵ�����A��B�������2L���ܱ������У��������·�Ӧ��3A(g)+B(g)![]() xC(g)+2D(g)��5min����c(D)=0.5mol/L��c(A):c(B)=1:2��C�ķ�Ӧ������ 0.15 mol/(Lmin)��
xC(g)+2D(g)��5min����c(D)=0.5mol/L��c(A):c(B)=1:2��C�ķ�Ӧ������ 0.15 mol/(Lmin)��
��1��B�ķ�Ӧ����v(B)=_____X=___
��2��A��5minĩ��Ũ����___
��3����ʱ�����ڵ�ѹǿ�뿪ʼʱ֮��Ϊ��____��
��4�����Ȼ���(S2Cl2)��һ������ɫҺ�壬�Ǻϳ���Ⱦ�ϵ���Ҫԭ�ϡ�д�����ĵ���ʽ______��
��5������ԭ������Ϊ34�����ĵ��ʼ��仯������;�dz��㷺��
a.����Ԫ�����ڱ��е�λ����___��Se2Cl2�����������Լ�����ṹʽΪ___��
b.��������һ�ֿ�Ӧ����δ�������豸�����Ͱ뵼����ϡ���֪��(In)����ͬ���ұ������������Ӳ㡣����˵����ȷ����___������ĸ����
A��ԭ�Ӱ뾶��In>Se B��In�Ľ����Ա�Seǿ
C��In�Ľ����Ա�Al�� D���������Ļ�ѧʽΪInSe2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ڹ�ũҵ����������ҪӦ�á�
��1�����Ĵ������ǹ�ҵ��������Ļ�����д���û�ѧ����ʽ_________��
��2��ij��ѧʵ��С��ͬѧ��������װ���Ʊ�������̽���������ʣ�������������ȥ����
��ش�
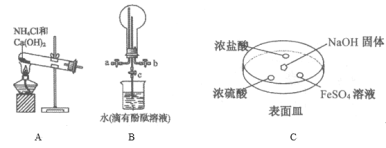
����װ��B�ռ���ʱ�����Ľ�������__��ѡ����a������b��������װ��B�еĻ���c�����۲쵽��ƿ�ڲ����˺�ɫ��Ȫ����˵�������е�������______��______��
����C��NaOH�����ϵμ���Ũ��ˮ��Ѹ�ٸ��ϸǣ��۲�����Ũ����Һ�θ�������� _____��������������Ӧ�Ļ�ѧ����ʽΪ_______��FeSO4Һ�����ȳ��ֻ���ɫ��������һ��ʱ����ɺ��ɫ�������ķ�Ӧ����Fe2++2NH3��H2O===Fe��OH��2��+2NH4+��_________��
��Ϊ��ֹ������Ⱦ������װ�ã�ʢ�ŵ�Һ���Ϊˮ�����������ն��ఱ��__������ţ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������в���ȱ�ٵ�Ԫ�أ�Ϊ��Ԥ����ȱ����ͨ���ھ���������һ����KIO3��ij�о�С��Ϊ�˼��ij�ӵ������Ƿ��е⣬�������й����ϣ���������ԭ���ǣ�KIO3 + 5KI + 3H2SO4 = 3I2 + 3K2SO4 + 3H2O
��1����˫���ű�ʾ�÷�Ӧ�е���ת�Ƶķ������Ŀ___________________________________���÷�Ӧ�л�ԭ�������������������֮����__________��0.2mol KIO3�μӷ�Ӧʱ��ת�Ƶĵ���Ϊ________mol��
��2������ʵ�����õ�һ�����ʵ���Ũ�ȵ�ϡ���ᣬ������1.0 mol/L��ϡ����500mL����������Ҫ�õ�����Ҫ����������___________����ѡ�������18.0mol/L Ũ����_________mL��
a.100mL��Ͳ b.������ c.100mL����ƿ d.50mL��Ͳ e.��ͷ�ι�
f.�ձ� g.500mL����ƿ
��3����������������ϡ������ҺŨ��ƫ�ߵ���____________����ѡ���
a.�ܽ����Һû����ȴ�����¾�ת�ƣ�b.ת��ʱû��ϴ���ձ�����������c.ת�ƹ�����������Һ��������d.������ƿ��ˮ����ʱ�۾�����Һ�棻e.ҡ�Ⱥ���Һ����ڿ̶��ߣ��ּ�����ˮ���̶���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ӦA(g) ![]() B(g) +C(g)���ݻ�Ϊ1.0L���ܱ������н��У�A�ij�ʼŨ��Ϊ0.050mol/L���¶�T1��T2��A��Ũ����ʱ���ϵ��ͼ��ʾ���ش��������⣺
B(g) +C(g)���ݻ�Ϊ1.0L���ܱ������н��У�A�ij�ʼŨ��Ϊ0.050mol/L���¶�T1��T2��A��Ũ����ʱ���ϵ��ͼ��ʾ���ش��������⣺

��1��������Ӧ���¶�T1____ T2��ƽ�ⳣ��K(T1)____K(T2)������������������С����������������
��2�����¶�T2ʱ��5min��Ӧ�ﵽƽ�⣬A��ת����Ϊ70%����
��ƽ��ʱ��ϵ�ܵ����ʵ���Ϊ________��
�ڷ�Ӧ��ƽ�ⳣ��K=_______��
�۷�Ӧ��0~5min�����ƽ����Ӧ����v(A)=________��
��3����֪1g FeS2��ȫȼ�շų�7.1kJ������FeS2ȼ�շ�Ӧ���Ȼ�ѧ����ʽΪ______��
��4������(t-BuNO)2���������ܼ��з������·�Ӧ��(t-BuNO)2 ![]() 2(t-BuNO) ��H = 50.5 kJ��mol-1���÷�Ӧ����S_____0(������������������������)����______�����ϸ��������ϵ���)�¶��������ڸ÷�Ӧ�Է����С�
2(t-BuNO) ��H = 50.5 kJ��mol-1���÷�Ӧ����S_____0(������������������������)����______�����ϸ��������ϵ���)�¶��������ڸ÷�Ӧ�Է����С�
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com