
【题目】(1)现有以下物质①熔融状态的NaCl ②NH3·H2O ③Na2O固体 ④铜 ⑤BaSO4固体 ⑥酒精 ⑦液态HCl ⑧KNO3溶液,其中属于电解质的是:___________;该状态下能导电的是_____________;属于非电解质的是_________________。(请用序号作答)
(2)以下A~D四个涉及H2O2的反应,请填空:
A. Na2O2+ 2HCl=H2O2+2NaCl B. Ag2O+H2O2=2Ag+O2↑+H2O
C. 2H2O2=2H2O+O2↑ D. □H2O2+□KMnO4+□H2SO4→□MnSO4+□K2SO4+□H2O+□O2↑
①配平D方程式,系数填在方框内____;该反应的还原剂是_________________;
②H2O2既体现氧化性,又体现还原性的反应是________,H2O2既不作氧化剂又不作还原剂的反应是__________。(请用代号作答)
③请用双线桥法表示B反应中电子转移的方向和数目:___________。
【答案】 ①②③⑤⑦ ①④⑧ ⑥ 2KMnO4+5H2O2+3H2SO4=K2SO4+2MnSO4+5O2↑+8H2O H2O2 C A 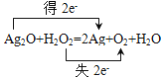
【解析】(1)水溶液中或熔化状态下能导电的化合物为电解质,则以上几种物质中,只有①②③⑤⑦为电解质,存在自由移动的离子或电子的物质能导电,则以上几种物质中只有①④⑧能导电,水溶液中和熔化状态下都不能导电的化合物为非电解质,则以上几种物质中,属于非电解质的有⑥,故答案为:①②③⑤⑦;①④⑧;⑥;
(2)①KMnO4中Mn的化合价为+7价,反应后变成了MnSO4,化合价变成+2,Mn元素化合价降低被还原,化合价降低了5价;H2O2中氧元素化合价为-1价,反应后变成了0价的O,化合价升高了1价,1分子双氧水反应,至少化合价升高2价,化合价变化的最小公倍数为10,所以KMnO4的计量数为2,双氧水的计量数为5,然后利用观察法配平其它物质,配平后的方程式为2KMnO4+5H2O2+3H2SO4=K2SO4+2MnSO4+5O2↑+8H2O,反应中双氧水中的O被氧化,双氧水为还原剂,故答案为:2KMnO4+5H2O2+3H2SO4= K2SO4+2MnSO4+5O2↑+ 8H2O;H2O2;
②A.Na2O2+2HCl=H2O2+2NaCl,是一个非氧化还原反应,双氧水既不是氧化剂,也不是还原剂;B.Ag2O+H2O2=2Ag+O2+H2O,Ag2O被还原成单质银,H2O2仅表现为还原性,其中氧元素转化为O2;C.2H2O2=2H2O+O2↑,过氧化氢的分解反应,是一个自身氧化还原反应,H2O2既表现了氧化性,又表现了还原性;D.H2O2+KMnO4+H2SO4→ MnSO4+K2SO4+H2O+O2↑,双氧水在反应中O元素的化合价由-1变成0,化合价升高被氧化,双氧水仅做还原剂;所以H2O2既体现氧化性,又体现还原性的反应是C;H2O2既不做氧化剂又不做还原剂的反应是A,故答案为:C;A;
③Ag2O+H2O2=2Ag+O2+H2O,Ag2O被还原成单质银,得2e-;H2O2仅表现为还原性,其中氧元素转化为O2;失2e-,反应中电子转移的方向和数目用双线桥法表示为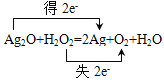 ,故答案为:
,故答案为: 。
。


科目:高中化学 来源: 题型:
【题目】某工厂废水中含游离态氮,通过下列实验测定其浓度
①取水样10.0mL于锥形瓶,加入10.0mLKI溶液(足量),滴入指示剂2﹣3滴.
②取一滴定管依次用自来水,蒸馏水洗净,然后注入0.01molL﹣1的Na2S2O3溶液,调整液面,记下读数.
③将锥形瓶置于滴定管下进行滴定,发生的反应为:I2+2Na2S2O3=2NaI+Na2S4O6 .
试回答下列问题:
(1)步骤①加入的指示剂是 .
(2)步骤②应使用式滴定管.
(3)试描述滴定终点的现象: .
(4)若耗去Na2S2O3溶液20.00mL,则废水中C12的物质的量浓度为 .
(5)请指出实验中的一处明显错误: .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定条件下,PbO2与Cr3+反应,产物是Cr2O72-和PbSO4,则参加反应的PbO2与Cr3+的物质的量之比为( )
A.3∶2B.3∶1C.1∶1D.3∶4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关的离子方程式书写正确的是
A. 向铜片中滴加浓硫酸并加热,有刺激性气味气体产生:Cu+4H++SO42-![]() Cu2++SO2↑+2H2O
Cu2++SO2↑+2H2O
B. 过量铁粉在加热条件下与浓硝酸反应:Fe+ NO3-+4H+ =Fe3++NO2↑+2H2O
C. 20mL1.0mol/L的明矾溶液与10mL3.5mol/LBa(OH)2溶液混合充分反应:3Ba2++6OH-+2Al3++3SO42-=3BaSO4+2Al(OH)3↓
D. 向Ca(HCO3)2溶液中加入过量NaOH溶液,有白色沉淀生成:Ca2++2HCO3- +2OH-== CaCO3↓+2H2O+CO32-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】 14C是一种放射性同位素,在高层大气中由宇宙射线产生的中子或核爆炸产生的中子轰击14N可使它转变为14C.下列说法正确的是( )
A.14C和14N互为同位素
B.14C和C60是同素异形体
C.![]() C核素中的中子数为8
C核素中的中子数为8
D.14CO2的摩尔质量为46
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铁粉和氧化亚铁粉末的混合物共9.2克,加入到150毫升的稀硫酸中,恰好完全反应,得到氢气2.24升(标准状况).求:
(1)混合物中铁和氧化亚铁的质量?
(2)原稀硫酸的物质的量浓度?
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上利用甲醇制备氢气常用的方法之一是甲醇蒸气重整法.此方法当中的一个主要反应为CH3OH(g)═CO(g)+2H2(g),说明该反应能自发进行的原因 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是
A.因为Al能导电,所以Al属于电解质
B.因为BaSO4难溶于水,所以BaSO4属于非电解质
C.虽然HCl在熔融时不导电,但HCl属于电解质
D.因为Na2SO4溶液能导电,所以Na2SO4溶液是电解质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】诺贝尔物理学奖曾授予“光纤之父”英国华裔科学家高锟以及两位美国科学家威拉德·博伊尔和乔治·史密斯。光导纤维的主要成分是二氧化硅,下列关于二氧化硅的说法正确的是( )
A. 二氧化硅是酸性氧化物,因此能与水反应生成硅酸
B. 用二氧化硅制取单质硅时,当生成2.24 L气体(标准状况)时,得到2.8 g硅
C. 二氧化硅制成的光导纤维,由于导电能力强而被用于制造光缆
D. 二氧化硅不能与碳酸钠溶液反应,但能与碳酸钠固体在高温时发生反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com