
【题目】已知有机物M的结构如图所示。关于M的描述正确的是

A.分子式为C11H7O2Cl
B.1molM与H2发生加成反应时,最多消耗5molH2
C.1molM与溴水发生加成反应时,最多消耗4molBr2
D.1 molNaOH溶液发生反应时,最多消耗2 molNaOH
科目:高中化学 来源: 题型:
【题目】某同学为探究元素周期表中元素性质的递变规律,设计了如下系列实验。
Ⅰ:(1)将钠、铁、镁、铝各1 mol分别投入到足量的同浓度的盐酸中,试预测实验结果:____________与盐酸反应最剧烈。
(2)向Na2S溶液中通入氯气出现黄色浑浊,可证明Cl的非金属性比S强,反应的离子方程式为____________________________。
Ⅱ:利用如图装置可验证同主族元素非金属性的变化规律。

(1)仪器B的名称为_____________,干燥管D的作用为防止______________________。
(2)若要证明非金属性:Cl>I-,则A中加浓盐酸,B中加KMnO4,KMnO4与浓盐酸常温下反应生成氯气,C中加淀粉-碘化钾混合溶液,观察到C中溶液__________________(填现象),即可证明。从环境保护的观点考虑,此装置缺少尾气处理装置,可用____________溶液吸收尾气。
(3)若要证明非金属性:![]() ,则在A中加盐酸、B中加
,则在A中加盐酸、B中加![]() 、C中加
、C中加![]() 溶液。观察到C中溶液_____________
溶液。观察到C中溶液_____________![]() 填现象
填现象![]() ,即可证明。但有的同学认为盐酸具有挥发性,可进入C中干扰实验,应在两装置间添加装有____________溶液的洗气瓶除去。
,即可证明。但有的同学认为盐酸具有挥发性,可进入C中干扰实验,应在两装置间添加装有____________溶液的洗气瓶除去。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种新型的“锂-呼吸CO2电化学装置”的结构如下图所示,下列说法正确的是( )
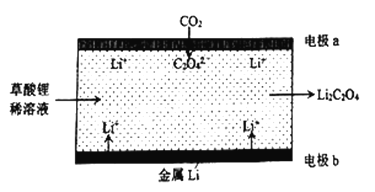
A. 该装置可由电能转变为化学能
B. 每生成20.4gLi2C2O4,有0.4molLi+从正极迁移至负极
C. 正极的电极反应为:C2O42--2e-=2CO2
D. 利用该技术可减少温室气体CO2的排放
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是元素周期表的一部分,用化学用语回答下列问题:
ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
二 | ① | ② | ③ | ||||
三 | ④ | ⑤ | ⑥ | ⑦ | ⑧ |
(1)③的元素符号为___,元素④与⑦形成化合物的电子式为___。
(2)比较元素①和⑥的原子半径大小:①___(填“>”或“<”)⑥
(3)元素⑥的离子结构示意图为___。
(4)元素①和⑧形成的化合物中含有的化学键为___。
(5)元素②、⑤的最高价氧化物对应的水化物之间反应的离子方程式为___。
(6)工业上冶炼元素⑥的单质的化学方程式为___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关离子共存的说法或离子方程式的书写中,正确的一组是( )
①加入NaOH溶液后的溶液中能大量共存的离子:NH4+、Al3+、SO42-
②pH=1的溶液中能大量共存的离子:Fe3+、Mg2+、Cl-、SO42-
③能使酚酞溶液变红的溶液中能大量共存的离子:K+、CO32-、Na+、S2-
④向 NH4HCO3溶液中加入足量NaOH溶液并共热:NH4++OH-=NH3↑+H2O
⑤用食醋溶解水垢:CaCO3+2H+=Ca2+ + CO2↑ + H2O
⑥向硫酸氢钠溶液中滴入氢氧化钡溶液至pH=7:Ba2++2OH-+2H++SO42-=BaSO4↓+2H2O
⑦用FeCl3溶液腐蚀铜电路板:2Fe3++Cu=2Fe2++Cu2+
A.①③⑤⑦B.②③⑥⑦C.②④⑤⑦D.③④⑥⑦
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定条件下,向1 L密闭容器中充入3 mol X 气体和1 mol Y气体,发生反应2X(g)+2Y(g)![]() 3Z(g)+2W(g),达到化学平衡时,测出的下列各生成物浓度的数据中肯定错误的是( )
3Z(g)+2W(g),达到化学平衡时,测出的下列各生成物浓度的数据中肯定错误的是( )
A.c(Z)=0.75 mol/LB.c(Z)=1.2 mol/L
C.c(W)=0.8 mol/LD.c(W)=1 mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】异戊二烯是重要的有机化工原料,其结构简式为: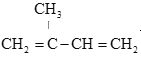 异戊二烯的一种制备方法如图所示:
异戊二烯的一种制备方法如图所示:
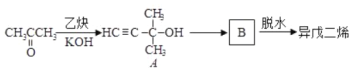
回答下列问题:
(1)A中含氧官能团发生的反应有____。(填反应类型)
(2)B的结构简式为___。B的同分异构体Y能发生银镜反应,则Y可能的结构有____种。
(3)设计由异戊二烯制得![]() 的路线。____。
的路线。____。
合成路线常用的表示方式为:A![]() B……
B……![]() 目标产物
目标产物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应的离子方程式书写正确的是( )
A.![]() 与水反应:
与水反应:![]() +
+![]() =
=![]()
B.铁与稀硫酸反应:2Fe+6![]() =2
=2![]() +3
+3![]() ↑
↑
C.![]() 溶液和
溶液和![]() 溶液反应:
溶液反应:![]() ↓
↓
D.CaCO3和稀硝酸反应:CaCO3+![]() =Ca2++
=Ca2++![]() ↑+
↑+![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】全钒氧化还原电池是一种新型可充电池,不同价态的含钒离子作为正极和负极的活性物质,分别储存在各自的酸性电解液储罐中。其结构原理如图所示,该电池放电时,右槽中的电极反应为:V2+-e-=V3+,下列说法不正确的是( )
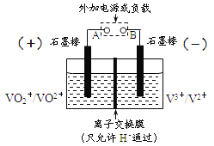
A. 充电时,每转移1mol电子,电解液中n(H+)的变化量为2mol
B. 充电时,阴极电解液pH升高
C. 放电时,右槽发生氧化反应
D. 放电时,左槽的电极反应式:VO2++2H++e-=VO2++H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com