
”¾ĢāÄæ”æÉčNAĪŖ°¢·ü¼ÓµĀĀŽ³£ŹżµÄÖµ,ĻĀĮŠŠšŹöÕżČ·µÄŹĒ£Ø £©
A. 2.24LŅŅĶéÖŠŗ¬ÓŠµÄ¹²¼Ū¼üŹżĪŖ0.7NA
B. 23 gÄĘŌŚæÕĘųÖŠ³ä·ÖČ¼ÉÕÉś³É¹żŃõ»ÆÄĘŹ±ŃõĘųµĆµē×ÓŹżĪŖ2NA
C. 11g³¬ÖŲĖ®(3H216O)ÖŠŗ¬ÓŠµÄÖŠ×ÓŹżĪŖ6NA
D. 0.1molN2Óė0.3molH2ŌŚŅ»¶ØĢõ¼žĻĀ³ä·Ö·“Ó¦ŗó£¬Éś³ÉNH3·Ö×ÓŹżĪŖ0.2NA
”¾“š°ø”æC
”¾½āĪö”æA”¢ĘųĢåƻӊÖøĆ÷ŹĒ±ź×¼×“æö£¬¹ŹA“ķĪó£»B”¢23 gÄĘŌŚæÕĘųÖŠ³ä·ÖČ¼ÉÕÉś³É¹żŃõ»ÆÄĘŹ±ŃõĘųµĆµē×ÓŹżĪŖ1NA£¬¹ŹB“ķĪó£»C”¢11g³¬ÖŲĖ®(3H216O)ÖŠŗ¬ÓŠµÄÖŠ×ÓŹżĪŖ![]() NA=6NA£¬ ¹ŹCÕżČ·£»D. ŗĻ³É°±·“Ó¦ŹĒæÉÄę·“Ó¦£¬0.1molN2Óė0.3molH2ŌŚŅ»¶ØĢõ¼žĻĀ³ä·Ö·“Ó¦“ļµ½Ę½ŗāŗó£¬Éś³ÉNH3·Ö×ÓŹżŠ”ÓŚ0.2NA£¬¹ŹD“ķĪó£»¹ŹŃ”C”£
NA=6NA£¬ ¹ŹCÕżČ·£»D. ŗĻ³É°±·“Ó¦ŹĒæÉÄę·“Ó¦£¬0.1molN2Óė0.3molH2ŌŚŅ»¶ØĢõ¼žĻĀ³ä·Ö·“Ó¦“ļµ½Ę½ŗāŗó£¬Éś³ÉNH3·Ö×ÓŹżŠ”ÓŚ0.2NA£¬¹ŹD“ķĪó£»¹ŹŃ”C”£



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æÄ³ŃŠ¾æŠ”×é“Ó¼×±½³ö·¢£¬°“ĻĀĮŠĀ·ĻßŗĻ³ÉČ¾ĮĻÖŠ¼äĢåXŗĶŅ½Ņ©ÖŠ¼äĢåY”£

ŅŃÖŖ£ŗ¢Ł»ÆŗĻĪļA”¢E”¢F»„ĪŖĶ¬·ÖŅģ¹¹Ģ唣

Ēė»Ų“š£ŗ
(1)ĻĀĮŠĖµ·Ø²»ÕżČ·µÄŹĒ_____________”£
A£®»ÆŗĻĪļCÄÜ·¢ÉśŃõ»Æ·“Ó¦£¬²»·¢Éś»¹Ō·“Ó¦ B£®»ÆŗĻĪļDÄÜ·¢ÉśĖ®½ā·“Ó¦
C£®»ÆŗĻĪļEÄÜ·¢ÉśČ”“ś·“Ó¦ D£®»ÆŗĻĪļFÄÜŠĪ³ÉÄŚŃĪ
(2)B+C”śDµÄ»Æѧ·½³ĢŹ½ŹĒ____________________________________________”£
(3)»ÆŗĻĪļGµÄ½į¹¹¼ņŹ½ŹĒ___________________”£
(4)Š“³öĶ¬Ź±·ūŗĻĻĀĮŠĢõ¼žµÄAµÄĖłÓŠĶ¬·ÖŅģ¹¹ĢåµÄ½į¹¹Ķ²Ź½___________”£
¢ŁŗģĶā¹āĘ×¼ģ²ā±ķĆ÷·Ö×ÓÖŠŗ¬ÓŠČ©»ł£¬¢Ś1H-NMRĘ×ĻŌŹ¾·Ö×ÓÖŠŗ¬ÓŠ±½»·£¬Äæ±½»·ÉĻÓŠĮ½ÖÖ²»Ķ¬»Æѧ»·¾³µÄĒāŌ×Ó”£
(5)ĪŖĢ½Ė÷ŠĀµÄŗĻ³ÉĀ·Ļߣ¬²ÉÓƱ½ŗĶŅŅĻ©ĪŖŌĮĻÖʱø»ÆĢØĪļF£¬ĒėÉč¼ĘøĆŗĻ³ÉĀ·Ļß(ÓĆĮ÷³ĢĶ¼±ķŹ¾£¬ĪŽ»śŹŌ¼ĮČĪŃ”)___________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æµŖ(N)”¢Į×(P)”¢Éé(As)µČVA×åŌŖĖŲ»ÆŗĻĪļŌŚŃŠ¾æŗĶÉś²śÖŠÓŠÖŲŅŖÓĆĶ¾”£ČēĪŅ¹śæĘŃŠČĖŌ±ŃŠ¾æ·¢ĻÖAs2O3(»ņŠ“³ÉAs4O6£¬Ė׳ĘÅųĖŖ)¶Ō°×ŃŖ²”ÓŠĆ÷ĻŌµÄÖĪĮĘ×÷ÓĆ»Ų“šĻĀĮŠĪŹĢā£ŗ
£Ø1£©AsŌ×ÓµÄŗĖĶāµē×ÓÅŲ¼Ź½ĪŖ_________________£»PµÄµŚŅ»µēĄėÄܱČS“óµÄŌŅņĪŖ_______________
£Ø2£©Š“³öŅ»ÖÖÓėCN”„»„ĪŖµČµē×ÓĢåµÄĮ£×Ó________(ÓĆ»ÆѧŹ½±ķŹ¾)£»(SCN)2·Ö×ÓÖŠ¦Ņ¼üŗĶ¦Š¼üøöŹż±ČĪŖ___________
£Ø3£©ÅųĖŖ¾ē¶¾£¬æÉÓĆŹÆ»ŅĻū¶¾Éś³ÉAsO33-ŗĶÉŁĮæAsO43-£¬ĘäÖŠAsO33-ÖŠAsµÄŌӻƷ½Ź½ĪŖ__________£¬AsO43-µÄæռ乹ŠĶĪŖ___________
£Ø4£©NH4+ÖŠHŅ»NŅ»HµÄ¼ü½Ē±ČNH3ÖŠH Ņ»NŅ»HµÄ¼ü½Ē“óµÄŌŅņŹĒ__________£»NH3ŗĶĖ®·Ö×ÓÓėĶĄė×ÓŠĪ³ÉµÄ»ÆŗĻĪļÖŠŃōĄė×Ó³ŹÖįĻņĻĮ³¤µÄ°ĖĆęĢå½į¹¹(ČēĻĀĶ¼I)£¬øĆ»ÆŗĻĪļ¼ÓČČŹ±Ź×ĻČŹ§Č„Ė®£¬Ēė“ÓŌ×Ó½į¹¹½Ē¶Č¼ÓŅŌ·ÖĪö£ŗ__________
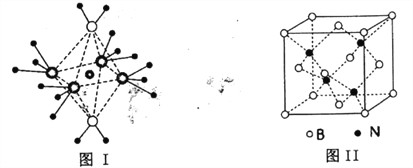
£Ø5£©BNµÄČŪµćĪŖ3000”ę£¬ĆܶČĪŖ2.25g”¤cm-3£¬Ę侧°ū½į¹¹ČēÉĻĶ¼¢ņĖłŹ¾£¬¾§ĢåÖŠŅ»øöBŌ×ÓÖÜĪ§¾ąĄė×ī½üµÄNŌ×ÓÓŠ__________øö£»ČōŌ×Ó°ė¾¶·Ö±šĪŖrNpmŗĶrBpm£¬°¢·ü¼ÓµĀĀŽ³£ŹżÖµĪŖNA£¬ŌņBN¾§°ūÖŠŌ×ÓµÄĢå»żÕ¼¾§°ūĢå»żµÄ°Ł·ÖĀŹĪŖ__________
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĶ¼ŹĒŅ»Ģ×ÖĘČ”²¢ŃéÖ¤ĀČĘų²æ·Ö»ÆѧŠŌÖŹµÄŹµŃé×°ÖĆ”£»Ų“šĻĀĮŠĪŹĢā£ŗ

(1)×°ÖĆAÖŠ£¬ŅĒĘ÷aµÄĆū³Ę____________£¬øĆŅĒĘ÷ÖŠŹ¢ÓŠµÄŹŌ¼ĮĪŖ_________£»
(2)µ±Cl2ĘųĮ÷ĶعżŅ»¶ĪŹ±¼äŗó£¬×°ÖĆBÖŠČÜŅŗµÄpH ________7(Ģī”°£¾”±”°£¼”±»ņ”°£½”±)£¬×°ÖĆBÖŠ·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ_________________________________£»
(3)µ±Cl2ĘųĮ÷³ÖŠųĶعżŹ±£¬×°ÖĆDÖŠøÉŌļµÄÓŠÉ«²¼ĢõÄÜĶŹÉ«£¬ŌŅņŹĒ_______________£»
(4)×°ÖĆCÖŠµÄČÜŅŗŃÕÉ«ÓÉĪŽÉ«±äĪŖ______________£»×°ÖĆEµÄ×÷ÓĆŹĒ____________________________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ[ŹµŃé»Æѧ]
½¹ŃĒĮņĖįÄĘ£ØNa2S2O5£©ŹĒ³£ÓƵÄæ¹Ńõ»Æ¼Į£¬ŌŚæÕĘųÖŠ”¢ŹÜČČŹ±¾łŅ×·Ö½ā”£ŹµŃéŹŅÖʱøÉŁĮæNa2S2O5µÄ·½·Ø£ŗŌŚ²»¶Ļ½Į°čĻĀ£¬æŲÖĘ·“Ó¦ĪĀ¶ČŌŚ40”ę×óÓŅ£¬ĻņNa2CO3¹ż±„ŗĶČÜŅŗÖŠĶØČėSO2£¬ŹµŃé×°ÖĆČēĻĀĶ¼ĖłŹ¾”£

µ±ČÜŅŗpHŌ¼ĪŖ4Ź±£¬Ķ£Ö¹·“Ó¦£¬ŌŚ20”ę×óÓŅ¾²ÖĆ½į¾§”£Éś³ÉNa2S2O5µÄ»Æѧ·½³ĢŹ½ĪŖ
2NaHSO3===Na2S2O5+H2O
£Ø1£©SO2ÓėNa2CO3ČÜŅŗ·“Ӧɜ³ÉNaHSO3ŗĶCO2£¬ĘäĄė×Ó·½³ĢŹ½ĪŖ____________________”£
£Ø2£©×°ÖĆYµÄ×÷ÓĆŹĒ______________________________”£
£Ø3£©Īö³ö¹ĢĢåµÄ·“Ó¦Ņŗ¾¼õŃ¹³éĀĖ”¢Ļ“µÓ”¢25”ꔫ30”ęøÉŌļ£¬æÉ»ńµĆNa2S2O5¹ĢĢ唣
¢Ł×é³É¼õŃ¹³éĀĖ×°ÖƵÄÖ÷ŅŖŅĒĘ÷ŹĒ²¼ŹĻĀ©¶·”¢________________ŗĶ³éĘų±Ć”£
¢ŚŅĄ“ĪÓƱ„ŗĶSO2Ė®ČÜŅŗ”¢ĪŽĖ®ŅŅ“¼Ļ“µÓNa2S2O5¹ĢĢ唣ÓƱ„ŗĶSO2Ė®ČÜŅŗĻ“µÓµÄÄæµÄŹĒ______”£
£Ø4£©ŹµŃéÖʵƵÄNa2S2O5¹ĢĢåÖŠŗ¬ÓŠŅ»¶ØĮæµÄNa2SO3ŗĶNa2SO4£¬ĘäæÉÄܵÄŌŅņŹĒ______”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĪŁ£Ø74W£©ŹĒČŪµć×īøߵĽšŹō£¬ŹĒÖŲŅŖµÄÕ½ĀŌĪļ׏”£×ŌČ»½ēÖŠĪŁæóŹÆµÄÖ÷ŅŖ³É·ÖŹĒĢśŗĶĆĢµÄĪŁĖįŃĪ(FeWO4”¢MnWO4)£¬»¹ŗ¬ÉŁĮæSi”¢P”¢AsµÄ»ÆŗĻĪļ”£ÓÉŗŚĪŁæóŅ±Į¶ĪŁµÄ¹¤ŅÕĮ÷³ĢČēĻĀ£ŗ

ŅŃÖŖ£ŗ¢ŁĀĖŌüIµÄÖ÷ŅŖ³É·ŻŹĒFe2O3”¢MnO2”£¢ŚÉĻŹöĮ÷³ĢÖŠ£¬³ż×īŗóŅ»²½Ķā£¬ĘäÓą²½ÖčĪŁµÄ»ÆŗĻ¼ŪĪ“±ä”£¢Ū³£ĪĀĻĀĪŁĖįÄŃČÜÓŚĖ®”£ »Ų“šĻĀĮŠĪŹĢā£ŗ
£Ø1£©ĪŁĖįÖŠĪŁŌŖĖŲµÄ»ÆŗĻ¼ŪĪŖ_________£¬Š“³öMnWO4ŌŚČŪČŚĢõ¼žĻĀ·¢Éś¼ī·Ö½ā·“Ӧɜ³ÉMnO2µÄ»Æѧ·½³ĢŹ½___________________________________________”£
£Ø2£©ÉĻŹöĮ÷³ĢÖŠĻņ“ÖĪŁĖįÄĘČÜŅŗÖŠ¼ÓĮņĖįµ÷pH=10ŗó£¬ČÜŅŗÖŠµÄŌÓÖŹŅõĄė×ÓĪŖSiO32-”¢HAsO32-”¢HAsO42-”¢HPO42-µČ£¬Ōņ”°¾»»Æ”±¹ż³ĢÖŠ£¬¼ÓČėH2O2Ź±·¢Éś·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖ_______________________________£¬ĀĖŌü¢ņµÄÖ÷ŅŖ³É·ÖŹĒ_________”£
£Ø3£©ŅŃÖŖĒāŃõ»ÆøĘŗĶĪŁĖįøĘ(CaWO4)¶¼ŹĒĪ¢Čܵē½āÖŹ£¬Į½ÕßµÄČܽā¶Č¾łĖęĪĀ¶ČÉżø߶ų¼õŠ””£Ķ¼ĪŖ²»Ķ¬ĪĀ¶ČĻĀCa(OH)2”¢CaWO4µÄ³ĮµķČܽāĘ½ŗāĒśĻß”£ŌņT1_________T2(Ģī”°>”±»ņ”°<”±)”£

½«ĪŁĖįÄĘČÜŅŗ¼ÓČėŹÆ»ŅČéµĆµ½“óĮæĪŁĖįøĘ£¬·¢Éś·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖ_________________£¬T2Ź±øĆ·“Ó¦µÄĘ½ŗā³£ŹżĪŖ_________________”£
£Ø4£©Ó²ÖŹŗĻ½šµ¶¾ßÖŠŗ¬Ģ¼»ÆĪŁ(WC)£¬ĄūÓƵē½ā·ØæÉŅŌ“ÓĢ¼»ÆĪŁ·ĻĮĻÖŠ»ŲŹÕĪŁ”£µē½āŹ±£¬ÓĆĢ¼»ÆĪŁ×öŃō¼«£¬²»ŠāøÖ×öŅõ¼«£¬HClČÜŅŗĪŖµē½āŅŗ£¬Ńō¼«Īö³öĪŁĖį²¢·Å³öCO2”£øĆŃō¼«·“Ó¦Ź½ĪŖ_________________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æij¹¤³§µÄ¹¤Ņµ·ĻĖ®ÖŠŗ¬ÓŠ“óĮæµÄFeSO4£¬½Ļ¶ąµÄCuSO4ŗĶÉŁĮæNa2SO4”£ĪŖĮĖ¼õÉŁĪŪČ¾²¢±ä·ĻĪŖ±¦£¬¹¤³§¼Ę»®“ÓøĆ·ĻĖ®ÖŠ»ŲŹÕĮņĖįŃĒĢśŗĶ½šŹōĶ£®Ēėøł¾ŻĻĀĮŠĮ÷³ĢĶ¼£¬Ķź³É»ŲŹÕĮņĖįŃĒĢśŗĶĶµÄŹµŃé·½°ø£®£Øæɹ©Ń”ŌńµÄŹŌ¼ĮĪŖĢś·Ū”¢Ļ”H2SO4”¢NaOHČÜŅŗµČŹŌ¼Į£©

£Ø1£©²Ł×÷aµÄĆū³ĘĪŖ £¬ĖłŠčŅŖµÄ²£Į§ŅĒĘ÷ĪŖ ”£
£Ø2£©¹ĢĢåEµÄ³É·ÖĪŖ £¬¼ÓČėµÄŹŌ¼Į¢ÜĪŖĻ”ĮņĖį£¬·¢ÉśµÄ»Æѧ·½³ĢŹ½ĪŖ ”£
£Ø3£©¼ÓČėŹŌ¼Į¢ŁµÄÄæµÄŹĒ ”£
£Ø4£©“ÓČÜŅŗDŗĶČÜŅŗGÖŠµĆµ½FeSO47H2O¾§ĢåµÄ²Ł×÷ĪŖ ”¢ĄäČ“½į¾§”¢¹żĀĖ”¢ ”¢øÉŌļ”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æijÖĘ¼ī³§µÄÉś²śĮ÷³ĢŹ¾ŅāĶ¼ČēĻĀ£ŗ

ĻĀĮŠ·ÖĪöÕżČ·µÄŹĒ£Ø £©
A. øĆÖĘ¼ī·ØŹĒŗīŹĻÖĘ¼ī·Ø B. ·“Ó¦¢ŁÖŠ°üŗ¬ø“·Ö½ā·“Ó¦
C. XÖŠÖ»ŗ¬ÓŠCa2+ŗĶCl”Ŗ D. ĄķĀŪÉĻ£¬Éś²ś¹ż³ĢÖŠĪŽŠč²¹³äCO2
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ(1)ŌŚŅ»¶ØĢõ¼žĻĀN2ÓėH2·“Ӧɜ³ÉNH3£¬Ēė»Ų“š£ŗ
¢ŁČō·“Ó¦ĪļµÄ×ÜÄÜĮæĪŖE1£¬Éś³ÉĪļµÄ×ÜÄÜĮæĪŖE2£¬ĒŅE1£¾E2£¬ŌņøĆ·“Ó¦ĪŖ________(Ģī”°ĪüČČ”±»ņ”°·ÅČČ”±)·“Ó¦”£
¢ŚŅŃÖŖ²šæŖ1 mol H”ŖH¼ü”¢1 mol N”ŖH¼ü”¢1 mol N”ŌN¼ü·Ö±šŠčŅŖµÄÄÜĮæŹĒ436 kJ”¢391 kJ”¢946 kJ£¬ŌņN2ÓėH2·“Ӧɜ³ÉNH3µÄČČ»Æѧ·½³ĢŹ½ĪŖ________________”£
(2) N2H4ŗĶH2O2»ģŗĻæÉ×÷»š¼żĶĘ½ų¼Į£¬ŅŃÖŖ£ŗ16 gŅŗĢ¬N2H4ŗĶ×ćĮæŃõĘų·“Ӧɜ³ÉN2(g)ŗĶH2O(l)£¬·Å³ö310.6 kJµÄČČĮ棻2H2O2(l)===O2(g)£«2H2O(l)””¦¤H£½£196.4 kJ”¤mol£1”£·“Ó¦N2H4(g)£«O2(g)===N2(g)£«2H2O(l)µÄ¦¤H£½____________kJ”¤mol£1”£N2H4ŗĶH2O2·“Ӧɜ³ÉN2(g)ŗĶH2O(l)µÄČČ»Æѧ·½³ĢŹ½ĪŖ_______________________________________”£
(3)ŹµŃéŹŅÓĆ50 mL 0.50 mol”¤L£1ŃĪĖįÓė50 mLijÅØ¶ČµÄNaOHČÜŅŗŌŚČēĶ¼ĖłŹ¾×°ÖĆÖŠ·“Ó¦£¬Ķعż²ā¶Ø·“Ó¦¹ż³ĢÖŠĖł·Å³öµÄČČĮææɼĘĖćÖŠŗĶČČ”£øĆ×°ÖĆÓŠĮ½“¦Ć÷ĻŌµÄ“ķĪó£¬ĘäÖŠŅ»“¦ŹĒȱɣŅ»ÖÖ²£Į§ŅĒĘ÷£¬øĆŅĒĘ÷µÄĆū³ĘĪŖ____________£»ŹµŃéŹŅĢį¹©ĮĖ0.50 mol”¤L£1ŗĶ0.55 mol”¤L£1Į½ÖÖÅØ¶ČµÄNaOHČÜŅŗ£¬Ó¦Ń”Ōń_____________mol”¤L£1µÄNaOHČÜŅŗ½ųŠŠŹµŃ锣

²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com