
(12分)某课外活动小组为了测定某氯化锶(SrCl2)样品的纯度,设计了如下方案:
称取1.0g样品溶解于适量水中,向其中加入含AgNO32.38g的AgNO3溶液(溶液中除Cl―外,不含其它与Ag+反应生成沉淀的离子),Cl―即被全部沉淀。然后用含Fe3+的溶液作指示剂,用0.2mol/L的NH4SCN标准溶液滴定剩余的AgNO3,使剩余的Ag+以AgSCN白色沉淀的形式析出,以测定氯化锶样品的纯度。请回答下列问题:
(1)滴定反应达到终点的现象是 ;
(2)实施滴定的溶液以呈 (选填“酸性”、“中性”或“碱性”)为宜,加
(填化学式)试剂可达到这一目的;
(3)在终点到达之前的滴定过程中,两种沉淀表面会吸附部分Ag+,需不断剧烈摇动锥形瓶,否则会使n (Clˉ)的测定结果 (选填“偏高”、“偏低”或“无影响”);
(4)到达终点后,则必须轻轻摇动锥形瓶,(此时不得剧烈摇动)以减少误差,否则这种误差会使n (Clˉ)测定值偏低,这说明两者的溶解度:AgCl AgSCN(填“>”或“<”);
(5)若以Fe3+的溶液作指示剂,用NH4SCN标准溶液滴定剩余的AgNO3时,用去上述浓度的NH4SCN溶液20.0mL,则原氯化锶样品的纯度为 。
科目:高中化学 来源: 题型:
 Ⅰ.研究NO2、SO2、CO等大气污染气体的处理具有重要意义.
Ⅰ.研究NO2、SO2、CO等大气污染气体的处理具有重要意义.| Q2-Q1 |
| 2 |
| Q2-Q1 |
| 2 |
查看答案和解析>>
科目:高中化学 来源:2015届广东省肇庆市高二上学期末考试化学试卷(解析版) 题型:实验题
(1)某学习小组用0.80mol/L标准浓度的烧碱溶液测定未知浓度的盐酸。
①滴定管如图所示,用 滴定管盛装标准浓度的氢氧化钠溶液(填“甲”或“乙”)。

②用滴定的方法来测定盐酸的浓度,实验数据如下所示:
|
实验编号 |
待测HCl溶液的体积(mL) |
滴入NaOH溶液的体积(mL) |
|
1 |
20.00 |
23.00 |
|
2 |
20.00 |
23.10 |
|
3 |
20.00 |
22.90 |
该未知盐酸的浓度为(保留两位有效数字)_______________。
③下列操作会使所测得的盐酸的浓度偏低的是__________:
A.盛装待测液的锥形瓶用水洗后未干燥
B.滴定前,碱式滴定管尖端有气泡,滴定后气泡消失
C.碱式滴定管用蒸馏水洗净后,未用标准氢氧化钠溶液润洗
D.读碱式滴定管的刻度时,滴定前仰视凹液面最低处,滴定后俯视读数
(2)某课外活动小组为了测定某氯化锶(SrCl2)样品的纯度,设计了如下方案:称取1.0 g样品溶解于适量水中,向其中加入含AgNO3 2.38 g的AgNO3溶液(溶液中除Cl-外,不含其他与Ag+反应生成沉淀的离子),Cl-即被全部沉淀。然后用含Fe3+的溶液作指示剂,用0.2 mol·L-1的NH4SCN标准溶液滴定剩余的AgNO3,使剩余的Ag+以AgSCN白色沉淀的形式析出,以测定氯化锶样品的纯度。
请回答下列问题:
①判断滴定达到终点的现象是_______________________________________________。
②考虑Ag+和Fe3+在酸或碱性溶液中的存在形式,在实施滴定的溶液以呈_____(选填“酸性”、“中性”或“碱性”)为宜。
③在终点到达之前的滴定过程中,两种沉淀表面会吸附部分Ag+,需不断剧烈摇动锥形瓶,否则会使n(Cl-)的测定结果________(选填“偏高”、“偏低”或“无影响”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
某课外活动小组为了探索乙二酸的酸性强弱及乙二酸受热分解产物,设计了如下实验。
(1)用pH试纸测定等物质的量浓度的硫酸、乙二酸、醋酸溶液的pH,测得溶液的pH分别为a、b、c,且a<b<c。
①测定上述溶液pH的方法是________________________________________________。
②上述三种酸的酸性由强到弱的顺序是__________________________________________。
(2)将一定量的乙二酸放于试管中,按下图装置进行实验。

充分加热一段时间后,发现乙装置中U形管里出现少量液体,丙装置中澄清石灰水变浑浊。待反应完成后,向乙装置中U形管里加入少量无水硫酸铜,无水硫酸铜变蓝。
①根据上述实验事实,推测乙二酸分解产物中一定有__________________________________。
②乙装置的作用是________________________________________________________。
(3)根据丁装置推测,乙二酸分解的产物中还可能有___________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
Ⅰ.研究NO2、SO2、CO等大气污染气体的处理具有重要意义。
(1)已知:2SO2(g) + O2(g)![]() 2SO3(g) ΔH= —Q1 kJ·mol-1
2SO3(g) ΔH= —Q1 kJ·mol-1
2NO(g) + O2(g)![]() 2NO2(g) ΔH= —Q2kJ·mol-1
2NO2(g) ΔH= —Q2kJ·mol-1
则反应NO2(g) + SO2(g)![]() SO3(g) + NO(g) 的ΔH= kJ·mol-1。
SO3(g) + NO(g) 的ΔH= kJ·mol-1。
 (2)一定条件下,将NO2与SO2以体积比1:2置于密闭容器中发生
(2)一定条件下,将NO2与SO2以体积比1:2置于密闭容器中发生
上述反应, 当测得上述反应平衡时NO2与NO体积比为1:3,
则平衡常数K= 。
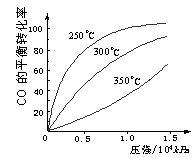
(3)CO可用于合成甲醇,反应方程式为:
CO(g)+2H2(g)![]() CH3OH(g)。CO在不同温度下的
CH3OH(g)。CO在不同温度下的
平衡转化率与压强的关系如下图所示。该反应ΔH 0
(填“>”或“ <”)。
Ⅱ.已知草酸是一种二元弱酸,草酸氢钠(NaHC2O4)溶液显酸性。
(1)用离子方程式解释Na2C2O4溶液显碱性的原因 ;
(2)常温下,比较0.1 mol·L-1NaHC2O4溶液中各种离子浓度的大小关系 ;
Ⅲ.某课外活动小组为了探究的BaSO4溶解度,分别将足量BaSO4放入:a. 5ml 水;b. 40 ml 0.2 mol·L-1的Ba(OH)2溶液;c. 20ml 0.5 mol·L-1的Na2SO4溶液;d. 40ml 0.1 mol·L-1的H2SO4溶液中,溶解至饱和。
(1)以上各溶液中,的浓度由大到小的顺序为 ;
A.b>a>c>d B.b>a>d>c C.a>d>c>b D.a>b>d>c
(2)某同学取同样的溶液b和溶液d直接混合,则混合溶液的pH值为 (设混合溶液的体积为混合前两溶液的体积之和)。
查看答案和解析>>
科目:高中化学 来源:2012-2013学年云南省玉溪一中高三(上)月考化学试卷(10月份)(解析版) 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com