
用碳棒作电极,在Na+、Cu2+、Cl-、SO42-等离子中选出适当离子组成电解质,电解其溶液,写出符合条件的一种电解质的化学式:
(1)当阴极放出H2,阳极放出O2时,电解质是___________________;
(2)当阴极析出金属,阳极放出O2时,电解质是________________;
(3)当阴极放出H2,阳极放出Cl2时,电解质是_________________;
(4)通过电子的物质的量与阴极析出的金属的物质的量、阳极析出的气体的物质的量之比为4:2:1时,电解质的化学式是______________________。
科目:高中化学 来源: 题型:
在10-9 m~10-7 m范围内,对原子、分子进行操纵的纳米超分子技术往往能实现意想不到的变化。如纳米铜颗粒一遇到空气就会剧烈燃烧,甚至发生爆炸。下列说法正确的是
A.纳米铜是一种新型化合物
B.纳米铜颗粒比普通铜更易与氧气发生反应
C.纳米铜与普通铜所含铜原子的种类不同
D.纳米铜无需密封保存
查看答案和解析>>
科目:高中化学 来源: 题型:
使反应4NH3(g)+3O2(g)===2N2(g)+6H2O(g)在2 L的密闭容器中进行,半分钟后N2的物质的量增加了0.6 mol。此反应的平均速率v( X)为 ( )
X)为 ( )
A.v(NH3)=0.02 mol·L-1·s-1
B.v(O2)=0.01 mol·L-1·s-1
C.v(N2)=0.02 mol·L-1·s-1
D.v(H2O)=0.02 mol·L-1·s-1
查看答案和解析>>
科目:高中化学 来源: 题型:
已知硫酸的第一步电离(H2SO4 = H++HSO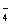 )是完全的,但第二步电离(HSO
)是完全的,但第二步电离(HSO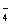
 H+ + SO
H+ + SO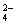 )并不完全。如果25℃时,01 mol·L-1 H2SO4溶液中c(SO
)并不完全。如果25℃时,01 mol·L-1 H2SO4溶液中c(SO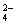 ) = 0.010 mol·L-1,01 mol·L-1 NaHSO4溶液中c(SO
) = 0.010 mol·L-1,01 mol·L-1 NaHSO4溶液中c(SO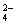 ) = 0.029 mol·L-1,试回答:
) = 0.029 mol·L-1,试回答:
(1)25℃时,01 mol·L-1 H2SO4溶液中pH = ;(可用对数表示)
(2)为何01 mol·L-1 的H2SO4 溶液中的c(SO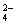 )比01 mol·L-1 的NaHSO4 溶液中c(SO
)比01 mol·L-1 的NaHSO4 溶液中c(SO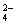 ) 小?
) 小?
(3)0.1 mol·L-1 Na2SO4溶液的pH值 7(填大于、小于或等于)
(4)固体NaHSO4与固体食盐混和共热至600℃,能否得到HCl气体?为什么?
(5)常温下测得0.25 mol·L-1的CuSO4溶液的pH值为5,025 mol·L-1 Cu(ClO4)2溶液的pH值为45,其原因是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
能够使反应Cu+2H2O====Cu(OH)2+H2↑发生的是( )
A.用铜片作阴、阳极,电解氯化铜溶液
B.用铜片作阴、阳极,电解硫酸钾溶液
C.铜锌合金在潮湿空气中发生电化学腐蚀
D.铜片作原电池的负极,碳棒作原电池的正极,氯化钠作电解质溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
已知同温同压下,气体的密度与它的摩尔质量成正比.一只气球若放在空气(空气平均摩尔质量为29g/mol)中可静止不动,那么在相同条件下该气球放在下列气体中会下沉的是( )
|
| A. | O2 | B. | Cl2 | C. | CO2 | D. | CH4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
将9.60×10﹣4 mol 的XO4﹣在溶液中还原到较低价态,需用24mL 0.100mol/L 的H2O2溶液,则X元素的化合价变为( )
|
| A. | +1 | B. | +2 | C. | +3 | D. | +4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
I2(g)+H2(g) 2HI(g) △H<0,在其他条件不变的情况下正确说法是 ( )
2HI(g) △H<0,在其他条件不变的情况下正确说法是 ( )
A.加入催化剂,改变了反应的途径,反应的△H也随之改变
B.改变压强,平衡不发生移动,反应放出的热量不变
C.升高温度,反应速率加快,反应放出的热量不变
D.若在原电池中进行,反应放出的热量不变
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是
A.SO2和NO2都是酸性氧化物,都能与水反应生成酸
B.Na2O和Na2O2组成元素相同,与CO2反应产物也完全相同
C.Al2O3和Na2O按物质的量比1:1投人水中可得到澄清溶液
D.金属铝排在金属活动性顺序表中氢元素的前面,铝与强酸反应一定放出氢气
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com