
| A. | 有单质参加或有单质生成的反应一定是氧化还原反应 | |
| B. | 氧化还原的本质是元素化合价的升降 | |
| C. | 失电子越多,该物质的还原性就越强 | |
| D. | 金属单质在化学反应中一定作还原剂 |
分析 A.同素异形体的转化中没有元素的化合价变化;
B.氧化还原反应的本质为电子的转移;
C.还原性与失去电子多少无关;
D.金属单质在反应中只能失去电子.
解答 解:A.同素异形体的转化中,有单质参加也有单质生成,没有元素的化合价变化,不属于氧化还原反应,故A错误;
B.氧化还原反应的本质为电子的转移,其特征为化合价的升降,故B错误;
C.还原性与失去电子多少无关,与失去电子的难易程度有关,故C错误;
D.金属单质在反应中只能失去电子,则只作还原剂,故D正确;
故选D.
点评 本题考查氧化还原反应,为高频考点,把握反应中元素的化合价变化为解答的关键,侧重氧化还原反应基本概念及转移电子的考查,题目难度不大.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 已知2H2(g)+O2(g)═2H2O(g)△H=-483.6kJ•mol-1,则氢气的燃烧热为241.8kJ•mol-1 | |
| B. | 已知C(石墨,s)═C(金刚石,s)△H>0,则金刚石比石墨稳定 | |
| C. | 已知2C(s)+2O2(g)═2CO2 (g)△H1;2C(s)+O2(g)=2CO(g)△H2,则△H1>△H2 | |
| D. | 已知Ni(CO)4(s)═Ni(s)+4CO(g)△H=Q kJ•mol-1,则Ni(s)+4CO(g)═Ni(CO)4(s)△H=-QkJ•mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 原混合物中Cu为12.8g | B. | 原溶液中c(SO42-)=0.15mol•L-1 | ||
| C. | 反应后溶液中Cu2+为0.3mol | D. | 反应后溶液中c(SO42-)为0.8mol•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
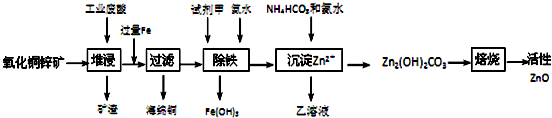
| 离子 | 开始沉淀时的pH | 完全沉淀时的pH |
| Fe2+ | 6.34 | 9.7 |
| Fe3+ | 1.48 | 3.2 |
| Zn2+ | 6.2 | 8.0 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氢化物的稳定性:HF>HCl>H2S>PH3>SiH4 | |
| B. | 离子的还原性:S2->Cl->Br->I- | |
| C. | 酸性:H2SO4>H3PO4>H2CO3>HClO | |
| D. | 金属性:Be<Mg<Ca<K |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com