
 化学实验有助于理解化学知识,形成化学观念,提高探究与创新能力,提升科学素养.
化学实验有助于理解化学知识,形成化学观念,提高探究与创新能力,提升科学素养.分析 (1)①依据原电池原理和盐桥的作用,在同一烧杯中,电极与溶液含相同的金属元素,设计不同的电极为铜和锌,电解质溶液为硫酸铜和硫酸锌溶液;
②以铜片为电极之一,CuSO4(aq)为电解质溶液,只在一个烧杯中组装原电池乙,则另一电极应比铜活泼做负极;
③从电硫稳定,能量转化彻底,反应速率快等分析判断;
(2)牲阳极的阴极保护法原理是原电池中把被保护的金属设计成正极,另一活泼的金属做负极.
解答 解:(1)①在同一烧杯中,电极与溶液含相同的金属元素,如图示设计原电池,锌做负极,铜做正极,原电池的甲装置示意图为: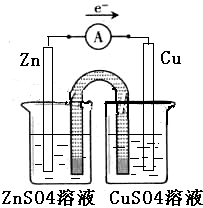 ,故答案为:
,故答案为: ;
;
②以铜片为电极之一,CuSO4(aq)为电解质溶液,只在一个烧杯中组装原电池乙,依据原电池反应的原理,需要选用比铜活泼的锌做负极,下层原电池,负极发生氧化反应,Zn-2e-=Zn2+,锌溶解,故答案为:电极逐渐溶解;
③甲乙两种原电池中可更有效地将化学能转化为电能的是甲,因为甲可以保持电流稳定,化学能基本都转化为电能.而乙中的活泼金属还可以与CuSO4溶液发生置换反应,部分能量转化为热能,
故答案为:甲;甲可以保持电流稳定,化学能基本都转化为电能.而乙中的活泼金属还可以与CuSO4溶液发生置换反应,部分能量转化为热能;
(2)根据牺牲阳极的阴极保护法原理,是原电池原理的应用,利用被保护的金属做正极被保护选择,为减缓电解质溶液中铁片的腐蚀,应选择比铁活泼的金属做负极,在电池内电路为阳极,称为牺牲阳极的阴极保护法,材料中 选择锌做阳极,
故答案为:锌片.
点评 本题考查了原电池装置设计,盐桥的作用分析应用,金属保护的方法和名称,题目难度中等.


科目:高中化学 来源: 题型:选择题
| A. | 已知:H2(g)+$\frac{1}{2}$O2(g)═H2O(l)△H=-285.8 kJ•mol-1,则H2的燃烧热为-285.8 kJ•mol-1 | |
| B. | 已知:S(g)+O2(g)═SO2(g)△H1=-Q1;S(s)+O2(g)═SO2(g)△H2=-Q2,则Q1<Q2 | |
| C. | 已知:$\frac{1}{2}$H2SO4(浓)+NaOH(aq)═$\frac{1}{2}$Na2SO4(aq)+H2O(l)△H1;CH3COOH(aq)+NH3•H2O(aq)═CH3COONH4(aq)+H2O(l)△H2,则有|△H1|<|△H2| | |
| D. | 已知:Fe2O3(s)+3C(石墨)═2Fe(s)+3CO(g)△H=+489.0 kJ•mol-1 CO(g)+$\frac{1}{2}$O2(g)═CO2(g)△H=-283.0 kJ•mol-1 C(石墨)+O2(g)═CO2(g)△H=-393.5 kJ•mol-1 则4Fe(s)+3O2(g)═2Fe2O3(s)△H=-1 641.0 kJ•mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1L溶液中Cl-离子浓度为0.2mol•L-1 | |
| B. | 1L溶液中Cl-离子总数为0.2NA | |
| C. | 1L溶液中Ba2+离子浓度为0.2mol•L-1 | |
| D. | 1L溶液中Ba2+和Cl-离子总数为0.4NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 已知25℃时部分弱电解质的电离平衡常数数据如表所示:
已知25℃时部分弱电解质的电离平衡常数数据如表所示:| 化学式 | CH3COOH | H2CO3 | HClO | |
| 电离平 衡常数 | Ka=1.8×10-5 | Ka1=4.3×10-7 | Ka2=5.6×10-11 | Ka=3.0×10-8 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 放入0.2mol SO2、0.1molO2、0.1mol SO3,达到平衡时SO3必小于amol | |
| B. | 放入0.2mol SO2、0.1molO2、0.2mol SO3,达到平衡时SO3必大于amol | |
| C. | 放入0.4mol SO2、0.1molO2,达到平衡时SO3会等于0.4amol | |
| D. | 放入0.2mol SO2、0.1molO2,达到平衡时SO3必小于amol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将碳块磨成粉末可以加快反应速率 | |
| B. | 升高温度一般可以加快反应速率 | |
| C. | 容器体积不变时,向其中充入N2,反应速率不变 | |
| D. | 增加碳的量可以加快反应速率 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 已知热化学方程式H+(aq)+OH-(aq)═H2O(l)△H=-57.3kJ/mol,
已知热化学方程式H+(aq)+OH-(aq)═H2O(l)△H=-57.3kJ/mol,查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com