
【题目】二氧化硫的催化氧化原理为2SO2(g)+O2(g)![]() 2SO3(g)。在一定压强下,反应混合体系在平衡状态时SO3的百分含量与温度的关系如图所示。下列说法不正确的是
2SO3(g)。在一定压强下,反应混合体系在平衡状态时SO3的百分含量与温度的关系如图所示。下列说法不正确的是
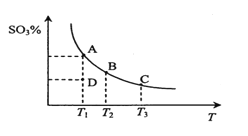
A. 反应2SO2(g)+O2(g)![]() 2SO3(g)的△H<0
2SO3(g)的△H<0
B. 在D点时v(正)<v(逆)
C. 若B、C点的平衡常数分别为KB、KC,则KB>KC
D. 恒温恒压下向平衡体系中通入氦气,平衡向左移动
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】(1)微生物燃料电池是指在微生物的作用下将化学能转化为电能的装置。某微生物燃料电池的工作原理如图所示:
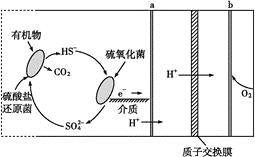
HS-在硫氧化菌作用下转化为SO![]() 的反应式是__。
的反应式是__。
(2)PbSO4热激活电池可用作火箭、导弹的工作电源,基本结构如图所示,其中作为电解质的无水LiCl—KCl受热熔融后,电池即可瞬间输出电能。该电池总反应为PbSO4+2LiCl+Ca=CaCl2+Li2SO4+Pb。
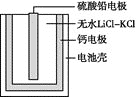
①放电过程中,Li+向__(填“负极”或“正极”)移动。
②负极反应式为__。
③电路中每转移0.2mol电子,理论上生成__gPb。
(3)氨氧燃料电池具有很大的发展潜力。氨氧燃料电池工作原理如图所示。
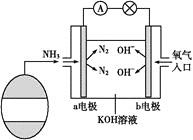
①a电极的电极反应式是__。
②一段时间后,需向装置中补充KOH,请依据反应原理解释原因:__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用下列装置完成相关实验,不合理的是( )
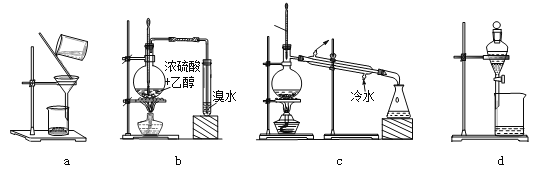
A. 用a趁热过滤提纯苯甲酸B. 用b制备并检验乙烯
C. 用c除去溴苯中的苯D. 用d分离硝基苯与水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】苏合香醇可以用作食用香精,其结构简式如图所示。

(1)苏合香醇的分子式为_____________,它不能发生的有机反应类型有(填数字序号)_____________。
①取代反应 ②加成反应 ③消去反应 ④加聚反应 ⑤氧化反应 ⑥水解反应
(2)有机物丙是一种香料,其合成路线如图。其中A为烃,相对分子质量为56;甲的相对分子质量通过质谱法测得为88,它的核磁共振氢谱显示只有三组峰;乙与苏合香醇互为同系物。

已知:R-CH=CH2  R-CH2CH2OH
R-CH2CH2OH
①A的结构简式是_____________。
②写出由B到C的化学反应方程式_____________。
③写出C与新制氢氧化铜悬浊液反应的化学反应方程式_____________。
④B的同分异构体能与钠反应生成氢气,不能发生催化氧化反应,其结构简式_____________。
⑤丙中含有两个—CH3,则甲与乙反应的化学方程式为__________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物H是一种有机光电材料中间体。实验室由芳香化合物A制备H的一种合成路线如下:
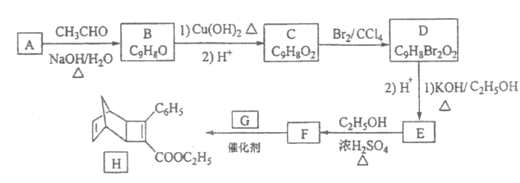
已知:①![]()
![]()
![]()
②
回答下列问题:
(1)A物质所含官能团的名称和结构简式为_____________。
(2)E的结构简式为_____________。
(3)G为甲苯的同分异构体,由F生成H的化学方程式为_____________。
(4)芳香化合物X是F的同分异构体,X能与饱和碳酸氢钠溶液反应放出CO2,其核磁共振氢谱显示有4种不同化学环境的氢,峰面积比为6:2:1:1,写出一种符合要求的X的结构简式_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I.金属矿物资源以及海水资源的利用有着非常重要的意义。
Ⅰ(1)金属铁常用的冶炼方法是____________(填序号);
A.热分解法 B.热还原法 C.电解法 D.湿法冶金
(2)利用冶炼得到的铁屑和海带中提取的碘可以用于生产KI,其工艺流程如图所示:
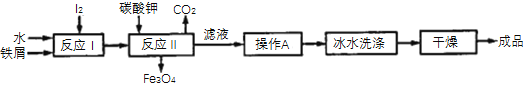
①操作A包括________________、_____________、过滤。
②用冰水洗涤的目的是:a除去附着在KI表面的可溶性杂质:b._________________。
③反应Ⅰ生成了铁与碘的化合物X,若X中铁元素与碘元素的质量比为21∶127,则X的化学式为__________________;反应Ⅱ中1molX完全反应生成89.6L(标准状况)CO2,写出反应Ⅱ的化学方程式:______________________________________________。
Ⅱ.工业上由黄铜矿(主要成分CuFeS2)冶炼铜的主要流程如下:
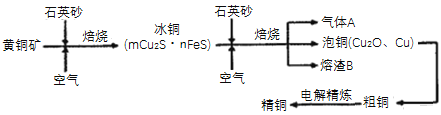
(3)气体A中的大气污染物可选用下列试剂中的____________吸收。
a.浓HSO4 b.稀HNO3 c.NaOH溶液 d.氨水
(4)用稀H2SO4浸泡熔渣B,取少量所得溶液,滴加KSCN溶液后呈红色,说明溶液中存在_____(填离子符号),检验溶液中还存在Fe2+的方案是:____________________________。
(5)在一定量的精铜中加入足量的稀HNO3溶液,该反应的离子方程式为________________。
(6)由泡铜冶炼粗铜的化学反应方程式为______________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA为阿伏伽德罗常数,下列叙述中正确的是:
A.标准状况下,2.24 L CHCl3中含有Cl原子的个数为0.3NA
B.1molCH4分子中共用电子个数为10NA
C.1molC2H6O分子中含有的C-H键的数目一定为5NA
D.14g乙烯和丙烯的混合物,完全燃烧后所生成的CO2分子数为NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】溴、碘主要存在于海水中,有“海洋元素”的美称。海水中的碘主要富集在海带中,我国海带产量居世界第一位,除供食用外,大量用于制碘。提取碘的途径如下图所示,下列有关叙述正确的是

A. 此装置进行操作①
此装置进行操作①
B.②③操作中所用到的玻璃仪器有:玻璃棒、烧杯、分液漏斗
C.④中当1molH2O2氧化I-时,转移电子数为2NA
D.溶剂X可选用酒精或苯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式表达正确的是( )
A.向硫酸铁溶液中加入过量铁粉:Fe+2Fe3+=3Fe2+
B.向Na2CO3溶液中滴加稀盐酸:Na2CO3+2H+=2Na++CO2↑+H2O
C.向铜粉中加入稀硫酸:Cu+2H+=Cu2++H2↑
D.向铝粉中加入足量NaOH溶液:2Al+2OH-=2AlO![]() +H2↑
+H2↑
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com