
 工业上一般以CO和H2为原料合成甲醇,该反应的热化学方程式为:CO (g)+2H2 (g)?CH3OH (g)△H=-116kJ/mol
工业上一般以CO和H2为原料合成甲醇,该反应的热化学方程式为:CO (g)+2H2 (g)?CH3OH (g)△H=-116kJ/mol分析 (1)化学平衡常数是指:一定温度下,可逆反应到达平衡时,生成物的浓度系数次幂之积与反应物的浓度系数次幂之积的比,固体、纯液体不需要在化学平衡常数中写出;
正反应为放热反应,升高温度平衡逆向移动,平衡常数减小;
(2)升高温度、增大物质浓度、增大压强、使用催化剂等可以加快反应速率,要提高转化率,应使平衡正向移动;
(3)a.体积压缩,平衡时各组分的浓度均增大;
b.体积压缩,压强增大,正逆反应速率都增大;
c.体积压缩,压强增大,平衡正向移动;
d.体积压缩,压强增大,平衡正向移动,氢气物质的量减小,甲醇物质的量增大;
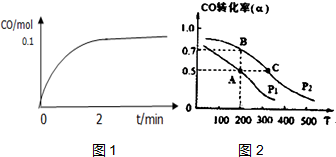
(4)2min到达平衡,生成CO为0.1mol,根据方程式可知生成氢气为0.2mol,再根据v=$\frac{△c}{△t}$计算v(H2);
(5)①温度越高,反应速率越快,到达平衡时间越短;
②A点时容器的体积为1L,CO转化率为0.5,消耗CO为0.5mol,则:
CO (g)+2H2 (g)?CH3OH (g)
起始浓度(mol/L):1 2 0
变化浓度(mol/L):0.5 1 0.5
平衡浓度(mol/L):0.5 1 0.5
再根据K=$\frac{c(C{H}_{3}OH)}{c(CO)×{c}^{2}({H}_{2})}$计算平衡常数.
解答 解:(1)CO (g)+2H2 (g)?CH3OH (g)的化学平衡常数表达式K=$\frac{c(C{H}_{3}OH)}{c(CO)×{c}^{2}({H}_{2})}$,
正反应为放热反应,升高温度平衡逆向移动,平衡常数减小;
故答案为:K=$\frac{c(C{H}_{3}OH)}{c(CO)×{c}^{2}({H}_{2})}$;减小;
(2)a.随时将CH3OH与反应混合物分离,平衡正向移动,转化率增大,但反应速率减慢,故a错误;
b.降低反应温度,平衡正向移动,转化率增大,但反应速率减慢,故b错误;
c.使用高效催化剂,加快反应速率,但不影响平衡移动,转化率不变,故c错误;
d.增大体系压强,反应速率加快,正反应为气体体积减小的反应,平衡正向移动,转化率增大,故d正确,
故选:d;
(3)a.体积压缩,压强增大,平衡正向移动,平衡常数不变,则平衡时各组分的浓度均增大,故a错误;
b.体积压缩,压强增大,正逆反应速率都增大,平衡正向移动,正反应速率增大更多,故b错误;
c.体积压缩,压强增大,平衡正向移动,CH3OH 的物质的量增加,故c正确;
d.体积压缩,压强增大,平衡正向移动,氢气物质的量减小,甲醇物质的量增大,重新平衡$\frac{c({H}_{2})}{c(C{H}_{3}OH)}$减小
,故d正确,
故选:cd;
(4)2min到达平衡,生成CO为0.1mol,根据方程式可知生成氢气为0.2mol,则v(H2)=$\frac{\frac{0.2mol}{1L}}{2min}$=0.1mol/(L.min),
故答案为:0.1mol/(L.min);
(5)①温度A<C,温度越高,反应速率越快,到达平衡时间越短,到平衡状态所需要的时间tA>tC,
故答案为:大于;
②A点时容器的体积为1L,CO转化率为0.5,消耗CO为0.5mol,则:
CO (g)+2H2 (g)?CH3OH (g)
起始浓度(mol/L):1 2 0
变化浓度(mol/L):0.5 1 0.5
平衡浓度(mol/L):0.5 1 0.5
故平衡常数K=$\frac{c(C{H}_{3}OH)}{c(CO)×{c}^{2}({H}_{2})}$=$\frac{0.5mol/L}{0.5mol/L×(1mol/L)^{2}}$=1 L2•mol-2,
故答案为:1 L2•mol-2.
点评 本题考查化学平衡计算与影响因素、平衡常数、化学反应速率计算及影响因素、化学平衡图象等,理解掌握平衡移动原理.


 天天练口算系列答案
天天练口算系列答案科目:高中化学 来源: 题型:解答题
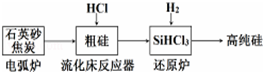
| 发生的主要反应 | |
| 电弧炉 | SiO2+2C$\frac{\underline{\;1600-1800℃\;}}{\;}$si+2CO |
| 流化床反应器 | Si+3HCl$\frac{\underline{\;250-300\;}}{\;}$SiHCl3+H2 |
| 还原炉 |
| 物质 | Si | SiCl4 | SiHCl3 | SiH2Cl2 | SiH3Cl | HCl | SiH4 |
| 沸点/°C | 2355 | 57.6 | 31.8 | 8.2 | -30.4 | -84.9 | -111.9 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温下,50g SO2和CO2的混合气体中可能含有2NA个氧原子 | |
| B. | I mol Cl2与足量的铁反应,转移的电子数为3NA | |
| C. | 1 L0.1 mol•L-1氨水含有0.l NA个OH- | |
| D. | I mol乙醇中含有C-H键的数目为6NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 前者小于后者 | B. | 前者大于后者 | C. | 前者等于后者 | D. | 不能确定 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | NH3•H2O | B. | Mg(OH)2 | C. | Na2CO3 | D. | MgCO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com