
下列实验操作中这确的是( )
A.进行蒸发操作时,应使混合物中的水分完全蒸干后,才能停止加热
B.进行蒸馏操作时,应使温度计水银球应该插入液面下
C.进行分液操作时,分液漏斗中下层液体从下口放出,上层液体从上口倒出
D.进行萃取操作时,应选择有机萃取剂,且萃取剂的密度必须比水大
科目:高中化学 来源: 题型:
某研究性学习小组利用所学知识进行下列实验研究。请回答下列问题:
(1) 利用高锰酸钾分解制氧气,并测定高锰酸钾的质量分数。实验停止加热如图I所示(导管出口高于液面)。
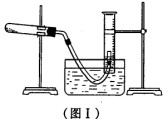
①测量收集到气体体积必须包括的几个步骤:a.调整量筒内外液面高度使之相同;
b.使试管和量筒内的气体都冷却至室温;c.读取量筒内气体的体积。这三步操作的正
确顺序是:___________(请填写步骤代号)。
②测量收集到气体体积时,如何使量筒内外液面的高度相同?____________。
(2) 为了得到二氧化锰,实验完毕将图I中的试管冷却后,把剩余的药品倒入烧
杯中加水溶解,再经过滤、洗涤和干燥得到纯净的二氧化锰。“过滤”中使用的玻璃仪
器是_____________________。
(3) 图Ⅱ是实验室制取TiCl4。的装置。四氯化钛是无色液体,沸点为1360C。它极
易水解,遇空气中的水蒸气即产生“白烟”(TiCl4+H2O=TiOCl2+2HCl↑)。在
6500C~8500C下,将氯气通过二氧化钛和炭粉的混合物可得到四氯化钛和CO气体。
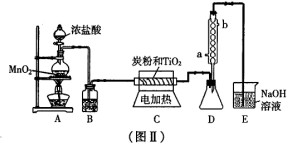
①A装置中反应的离子方程式______________________________
②B装置中的试剂及其作用是______________________________
③D装置中冷凝水的方向为_______________进_______________出。
④请指出此装置的缺陷和不妥之处

查看答案和解析>>
科目:高中化学 来源: 题型:
某研究性学习小组利用所学知识进行下列实验研究。请回答下列问题:
(1) 利用高锰酸钾分解制氧气,并测定高锰酸钾的质量分数。实验停止加热如图I所示(导管出口高于液面)。
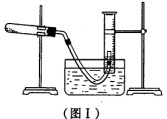
①测量收集到气体体积必须包括的几个步骤:a.调整量筒内外液面高度使之相同;
b.使试管和量筒内的气体都冷却至室温;c.读取量筒内气体的体积。这三步操作的正
确顺序是:___________(请填写步骤代号)。
②测量收集到气体体积时,如何使量筒内外液面的高度相同?____________。
(2) 为了得到二氧化锰,实验完毕将图I中的试管冷却后,把剩余的药品倒入烧
杯中加水溶解,再经过滤、洗涤和干燥得到纯净的二氧化锰。“过滤”中使用的玻璃仪
器是_____________________。
(3) 图Ⅱ是实验室制取TiCl4。的装置。四氯化钛是无色液体,沸点为1360C。它极
易水解,遇空气中的水蒸气即产生“白烟”(TiCl4+H2O=TiOCl2+2HCl↑)。在
6500C~8500C下,将氯气通过二氧化钛和炭粉的混合物可得到四氯化钛和CO气体。
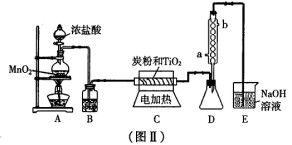
①A装置中反应的离子方程式______________________________
②B装置中的试剂及其作用是______________________________
③D装置中冷凝水的方向为_______________进_______________出。
④请指出此装置的缺陷和不妥之处

查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
(14分)欲用浓硝酸法(测定反应后生成气体的量)测定某铜银合金中铜的质量分数。资料表明:①反应中除生成NO2气体外还有少量的NO生成;②常温下N02与N2O4混合存在,在低于0℃时几乎只有无色N2O4液体或晶体存在。为完成测定并验证有NO生成,有人设计下图实验装置。
(1)实验开始前要先打开A部分的活塞K1,持续通一段时间的氮气再关闭K1,这样做的目的是________________________________________________。
(2)装置B瓶的作用是___________________________________________。
(3)A中反应停止后,打开D中的活塞K2并通人氧气,若反应中确有NO产生,则D中应出现的现象是________________;实验发现,通人氧气温度的高低对实验现象有较大影响,则为了便于观察应通人_______________(填“冷”或“热”)的氧气。
(4)为了减少测量误差,在A中反应完成和D中出现现象后,还应继续进行的操作是:___________________________________________________。
(5)实验测得下列数据:所用铜银合金质量为15.0 g,浓硝酸的体积为40 mL,浓度为13.5mol·L-1。实验后:A中溶液体积为40mL,H+浓度为1.0mol·L-1。若设反应中硝酸既无挥发也无分解,则:
①参加反应的硝酸的物质的量为______________;
②若已测出反应后E装置的生成物含氮元素的质量,则为确定合金中铜的质量分数,还需要测定的数据是__________。
(6)实验中只测定铜的质量分数,不验证NO的产生,则在铜银合金与硝酸反应后,只需简单的实验操作就可以达到目的,请简述实验过程_______________ ____。
【解析】本实验的目的有两个。一是验证反应中除生成NO2气体外还有少量的NO生成,二是测定某铜银合金中铜的质量分数,解题时我们始终围绕这两个目的。要验证有NO生成,就必须要保证整个装置中没有氧气存在,否则即使生成NO,也会转变成NO2,所以实验开始前要先打开A部分的活塞K1,持续通一段时间的氮气再关闭K1,这样做的目的是排尽装置中的空气。检验NO的方法是将NO与O2反应生成红棕色的NO2,由于反应中本来就生成NO2,所以必须将NO2与NO分离,结合题目不难得到装置C的作用就是将NO2转变成无色N2O4液体或晶体。如果温度过低NO2会转变成无色N2O4液体或晶体,所以为了便于观察应通人热的氧气。要测定某铜银合金中铜的质量分数除知道铜银合金的质量外,还必须测得与铜银合金相关的另外一个量,方可列方程组求解。结合题意,可知方法为测出氮的氧化物的质量。由于氮的氧化物存在于C、E两个装置中,所以必须测出两个装置的质量变化。另为保证测定准确,在A中反应完成和D中出现现象后,还应打开K1、K2,持续一段时间的N2和O2,以保证氮的氧化物被充分吸收。计算参加反应的硝酸的物质的量可以利用原子守恒进行计算,反应后剩余硝酸是0.04mol,反应前硝酸是0.04L×13.5mol/L=0.54mol,剩余参加反应的硝酸是0.5mol。因为溶液中含有银离子,剩余可以通过沉淀法来测定银的物质的量。
查看答案和解析>>
科目:高中化学 来源:2014届河北省高一下学期期中考试化学试卷(解析版) 题型:实验题
(14分)欲用浓硝酸法(测定反应后生成气体的量)测定某铜银合金中铜的质量分数。资料表明:①反应中除生成NO2气体外还有少量的NO生成;②常温下N02与N2O4混合存在,在低于0℃时几乎只有无色N2O4液体或晶体存在。为完成测定并验证有NO生成,有人设计下图实验装置。
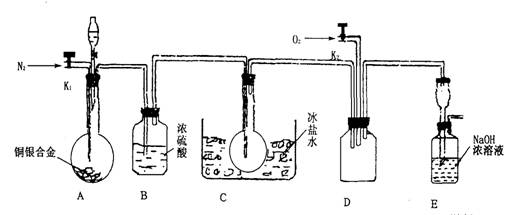
(1)实验开始前要先打开A部分的活塞K1,持续通一段时间的氮气再关闭K1,这样做的目的是________________________________________________。
(2)装置B瓶的作用是___________________________________________。
(3)A中反应停止后,打开D中的活塞K2并通人氧气,若反应中确有NO产生,则D中应出现的现象是________________;实验发现,通人氧气温度的高低对实验现象有较大影响,则为了便于观察应通人_______________(填“冷”或“热”)的氧气。
(4)为了减少测量误差,在A中反应完成和D中出现现象后,还应继续进行的操作是: ___________________________________________________。
(5)实验测得下列数据:所用铜银合金质量为15.0 g,浓硝酸的体积为40 mL,浓度为13.5mol·L-1。实验后:A中溶液体积为40mL,H+浓度为1.0mol·L-1。若设反应中硝酸既无挥发也无分解,则:
①参加反应的硝酸的物质的量为______________;
②若已测出反应后E装置的生成物含氮元素的质量,则为确定合金中铜的质量分数,还需要测定的数据是__________。
(6)实验中只测定铜的质量分数,不验证NO的产生,则在铜银合金与硝酸反应后,只需简单的实验操作就可以达到目的,请简述实验过程_______________ ____。
【解析】本实验的目的有两个。一是验证反应中除生成NO2气体外还有少量的NO生成,二是测定某铜银合金中铜的质量分数,解题时我们始终围绕这两个目的。要验证有NO生成,就必须要保证整个装置中没有氧气存在,否则即使生成NO,也会转变成NO2,所以实验开始前要先打开A部分的活塞K1,持续通一段时间的氮气再关闭K1,这样做的目的是排尽装置中的空气。检验NO的方法是将NO与O2反应生成红棕色的NO2,由于反应中本来就生成NO2,所以必须将NO2与NO分离,结合题目不难得到装置C的作用就是将NO2转变成无色N2O4液体或晶体。如果温度过低NO2会转变成无色N2O4液体或晶体,所以为了便于观察应通人热的氧气。要测定某铜银合金中铜的质量分数除知道铜银合金的质量外,还必须测得与铜银合金相关的另外一个量,方可列方程组求解。结合题意,可知方法为测出氮的氧化物的质量。由于氮的氧化物存在于C、E两个装置中,所以必须测出两个装置的质量变化。另为保证测定准确,在A中反应完成和D中出现现象后,还应打开K1、K2,持续一段时间的N2和O2,以保证氮的氧化物被充分吸收。计算参加反应的硝酸的物质的量可以利用原子守恒进行计算,反应后剩余硝酸是0.04mol,反应前硝酸是0.04L×13.5mol/L=0.54mol,剩余参加反应的硝酸是0.5mol。因为溶液中含有银离子,剩余可以通过沉淀法来测定银的物质的量。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com