
| A. | ①电子流动方向 | B. | ②电流方向 | ||
| C. | ③电极反应 | D. | ④溶液中离子移动方向 |
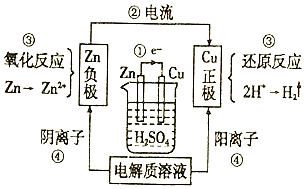
分析 该装置是锌铜稀硫酸原电池,锌作负极,铜作正极,负极上锌失电子发生氧化反应,正极上氢离子得电子发生还原反应,电子从负极沿导线流向正极,电流的方向与电子方向相反,在内电路中,阴离子移向负极,阳离子移向正极,以此解答.
解答 解:A.锌为负极,铜为正极,电子由锌片流向铜片,故A正确;
B.电流与电子运动方向相反,则电流由铜片经导线流向锌片,故B错误;
C.H+在铜片上得电子被还原生成H2逸出,故C正确;
D.原电池工作时,阴离子移向负极,阳离子移向正极,故D正确;
故选B.
点评 本题考查原电池知识,为高考高频考点,注意把握原电池的组成以及工作原理,能正确书写电极方程式,注意相关基础知识的积累,难度不大.


 应用题作业本系列答案
应用题作业本系列答案科目:高中化学 来源: 题型:选择题
| A. | 微电池的负极是Mg | B. | 微电池的负极是Al | ||
| C. | 铝的电极反应式为2H++2e-═H2↑ | D. | 镁的电极反应式为Mg-2e-═Mg2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将一块带有氧化膜的铝片与过量的浓NaOH溶液完全反应后,取澄清溶液将其蒸干,得纯净的NaAlO2固体 | |
| B. | 向NaAlO2溶液中加入过量的A1C13溶液,将所得沉淀过滤洗涤,加热灼烧去掉水分,可得纯净的A1(OH)3固体 | |
| C. | 把铝块与适量的稀盐酸完全反应,将所得溶液蒸干,可得AlCl3固体 | |
| D. | AlC3溶液与足量氨水反应,将沉淀过滤、洗涤、灼烧去掉水分可得Al2O3固体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 根据元素在周期表中的位置,推测元素的原子结构 | |
| B. | 指导新元素的发现和合成,预测新元素的性质 | |
| C. | 在金属与非金属的分界线附近寻找半导体材料 | |
| D. | 在零族元素中寻找耐腐蚀的金属材料 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用溴水检验汽油中是否含有不饱和脂肪烃 | |
| B. | 除去苯中混有的苯酚,加入浓溴水,过滤 | |
| C. | 除去乙醇中混有的水,加入金属钠,蒸馏 | |
| D. | 乙烷气体中混有乙烯,通入酸性高锰酸钾溶液,洗气 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | v(A2)=0.4 mol•L-1•s-1 | B. | v(D)=6 mol•L-1•min-1 | ||
| C. | v(C)=0.6 mol•L-1•s-1 | D. | v(B2)=0.8 mol•L-1•s-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
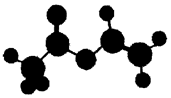 法国、美国、荷兰的三位科学家因研宄“分子机器的设计与合成”获得2016年诺贝尔化学奖.轮烷是一种分子机器的“轮子”,轮烷的一种合成原料由C、H、O三种元素组成,其球棍模型如图所示,下列说法正确的是( )
法国、美国、荷兰的三位科学家因研宄“分子机器的设计与合成”获得2016年诺贝尔化学奖.轮烷是一种分子机器的“轮子”,轮烷的一种合成原料由C、H、O三种元素组成,其球棍模型如图所示,下列说法正确的是( )| A. | 该化合物的名称为乙酸乙酯 | |
| B. | 该化合物与Br2的四氯化碳溶液不反应 | |
| C. | 该化合物既能发生水解反应,又能发生缩聚反应 | |
| D. | 该化合物的链状同分异构体中,能与NaHCO3反应放出CO2的只有3种 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
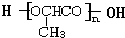 +(n-1)H2O.
+(n-1)H2O.
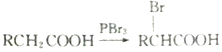
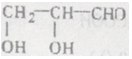 (己知同一个碳原子上不能连接2个羟基)
(己知同一个碳原子上不能连接2个羟基)查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com