
【题目】利用反应NO2(g)+SO2(g)![]() SO3(g)+NO(g)+Q(Q>0)可处理NO2、SO2等大气污染物,具有十分重要的意义。
SO3(g)+NO(g)+Q(Q>0)可处理NO2、SO2等大气污染物,具有十分重要的意义。
完成下列填空:
(1)该反应中被氧化的元素是__________;写出该反应的平衡常数表达式:K =_____________。
(2)若上述反应在一密闭容器中进行。下列能表明反应达到平衡状态的是_______(选填编号)。
a.混合气体颜色保持不变
b.NO2和NO的体积比保持不变
c.每消耗1mol SO2的同时生成1mol SO3
d.体系中气体密度保持不变
(3)一定温度下,在容积为V L的容器中发生上述反应,t min内,SO2的物质的量下降了a mol,则这段时间内v(NO) =__________(用相关字母表示并注明单位)。
(4)请写出两种能提高SO2转化率的措施:_____________、_____________。
(5)亚硫酸溶液久置,pH会变小,请用方程式表示其原因_______________
(6)将SO2持续通入NaOH溶液中,溶液中SO32—的浓度变化如图所示,请解释原因。

__________________
【答案】 SO2中+4价的S [SO3][NO]/[NO2][SO2] ab a/Vt mol/(L·min) 通入NO2 移走NO或SO3、降低温度、通入O2等(任写两种) 2H2SO3 + O2 → 2H2SO4 SO2与OH—反应生成SO32—,因此SO32—浓度增大;继续通入SO2时,SO2与SO32—反应生成HSO3—,导致SO32—浓度减小
【解析】(1)该反应中S元素化合价从+4价升高到+6价,被氧化的元素是S;根据方程式可知该反应的平衡常数表达式:K=[SO3][NO]/[NO2][SO2]。(2)a.混合气体颜色保持不变说明NO2浓度不再发生变化,说明反应达到平衡状态,a正确;b.NO2和NO的体积比保持不变说明正逆反应速率相等,达到平衡状态,b正确;c.每消耗1mol SO2的同时生成1mol SO3均表示正反应速率,不能说明反应达到平衡状态,c错误;d.密度是混合气的质量和容器容积的比值,在反应过程中质量和容积始终是不变的,因此体系中气体密度保持不变不能说明,d错误,答案选ab;(3)一定温度下,在容积为V L的容器中发生上述反应,t min内,SO2的物质的量下降了a mol,则这段时间内生成NO是amol,所以v(NO) = a/Vt mol/(L·min)。(4)正反应是放热反应,所以能提高SO2转化率的措施有通入NO2、移走NO或SO3、降低温度、通入O2等。(5)亚硫酸易被氧化为强酸硫酸,因此溶液久置,pH会变小,方程式为2H2SO3+O2→2H2SO4。(6)SO2是酸性氧化物,通入氢氧化钠溶液中,SO2与OH—反应生成SO32—,因此SO32—浓度增大;继续通入SO2时,SO2与SO32—反应生成HSO3—,导致SO32—浓度减小。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】合成光刻胶的一种路线如下:
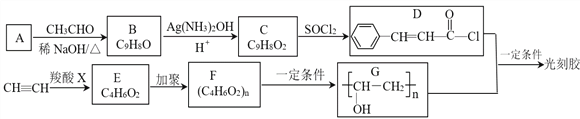
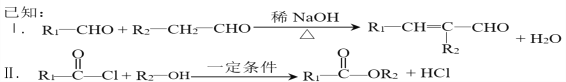
Ⅲ.RCOOH+CH![]() CH RCOOCH=CH2
CH RCOOCH=CH2
回答下列问题
(1)光刻胶中所含官能团的名称是______。
(2)D+G→光刻胶的化学方程式为______,该反应的反应类型是______。
(3)H是C的同分异构体,H具有下列性质或特征:①能发生水解反应和银镜反应;②能使溴水褪色;③属于芳香族化合物。则H的结构有______种。其中核磁共振氢谱为5组峰,且峰面积比为1∶1∶2∶2∶2的结构简式为______。
(4)根据已有知识并结合相关信息,写出以CH3CH2OH为原料制备CH3CH2CH2COOC2H5的合成路线流程图(无机试剂任选)。
(合成路线流程图示例如下:![]() )
)
______
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式正确的是
A. 甲酸与碳酸钠溶液反应 2H++CO32-=CO2↑+H2O
B. 醋酸溶液与Cu(OH)2 2H++Cu(OH)2=Cu2++2H2O
C. 苯酚钠溶液通足量CO2 2C6H5O-+CO2+H2O![]() 2C6H5OH+CO32-
2C6H5OH+CO32-
D. 甲醛溶液与足量的银氨溶液共热 ![]() +4Ag(NH3)2++4OH-
+4Ag(NH3)2++4OH-![]() CO32-+2NH4++4Ag↓+6NH3+2H2O
CO32-+2NH4++4Ag↓+6NH3+2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于有机反应的说法正确的是
A. 酸和醇发生取代反应一定生成酯B. 能发生银镜反应的有机物一定含有醛基
C. 卤代烃水解一定生成醇D. 醇脱水一定生成烯烃
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:酯能在碱性条件下发生如下反应:RCOOR′+NaOH―→RCOONa+R′OH,醛在一定条件下能被氧化成羧酸。某种烃的含氧衍生物A,其相对分子质量为88,分子内C、H、O 的原子个数之比为2∶4∶1,A与其它物质之间的转化关系如下:

请回答下列问题:
(1)写出 A、E 的结构简式:
A___________________,E_________________。
(2)写出 C 与 D 在一定条件下发生反应的化学方程式: ____________________。
(3)A的同分异构体中属于羧酸的有________种。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列事实不能用勒夏特列原理解释的是( )
①由NO2和N2O4组成的平衡体系加压后颜色先变深后变浅
②增大压强可加快SO2转化为SO3的速率
③黄绿色的氯水光照后颜色变浅
④在含有Fe(SCN)3的红色溶液中加铁粉,振荡静置,溶液颜色变浅或褪去
⑤对平衡体系H2(g)+I2(g) ![]() 2HI(g)加压后,混合气体的颜色加深
2HI(g)加压后,混合气体的颜色加深
A. ①③④ B. ②⑤ C. ①⑤ D. ①②④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质性质与应用对应关系不正确的是
A. 乙烯可以发生加成反应,常用作制取溴乙烷
B. 三硝基甲苯(TNT)难溶于水,可用作烈性炸药
C. 丙三醇具有很强的吸湿性,可用作配制化妆品
D. 乙炔可燃(氧炔焰温度可达3000℃以上),氧炔焰常用作焊接金属
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】离子方程式CO32-+ 2H+ = H2O + CO2↑中的CO32-代表的物质可以是
A.CaCO3 B.NaHCO3 C.Na2CO3 D.BaCO3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com