
| 80×35% |
| 14 |
| 80×50% |
| 40 |
| 80×(1-50%-35%) |
| 12 |
| 80×35% |
| 14 |
| 80×50% |
| 40 |
| 80×(1-50%-35%) |
| 12 |
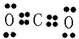 ,故答案为:CaCN2;
,故答案为:CaCN2;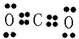 ;
;

 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
| A、非金属元素R所形成的含氧酸盐(NaROb)中的R元素必定呈现正价 |
| B、只有非金属能形成含氧酸或含氧酸盐 |
| C、除稀有气体外的非金属元素都能生成不同价态的含氧酸 |
| D、非金属的最高价含氧酸都具有强氧化性 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、常温常压下,7.0g乙烯与丙烯的混合物中含有氢原子的数目为NA |
| B、25℃时,pH=13的Ba(OH)2溶液中含有的OH-数目为0.1NA |
| C、50mL 18.4mol?L-1浓硫酸与足量铜微热反应,生成SO2分子的数目为0.46NA |
| D、常温下,1L 0.1mol?L-1的NH4NO3溶液中氧原子数为0.3NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
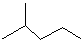 表示的分子式
表示的分子式 中含有的官能团的名称为
中含有的官能团的名称为查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1:2:3 |
| B、.1:1:1 |
| C、3:2:1 |
| D、2:1:1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com