

| 70 |
| 14 |
| 70 |
| 14 |
| 乙醇 |
| △ |
 ,
,| 乙醇 |
| △ |
 ;
;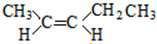 、
、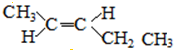 ,
,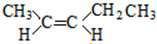 、
、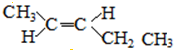 ;
; ,
, .
.


 金博士一点全通系列答案
金博士一点全通系列答案科目:高中化学 来源: 题型:
| A、加入硫酸铜粉末 |
| B、加入硝酸钠粉末 |
| C、加入醋酸钠晶体 |
| D、加入铅笔芯末 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、等体积、等物质的量浓度的Ba(OH)2溶液与NaHCO3溶液混合:Ba2++2OH-+2HCO3-═BaCO3↓+CO32-+H2O |
| B、次氯酸钙溶液中通入少量SO2气体:Ca2++2ClO-+SO2+H2O═CaSO3↓+2HClO |
| C、NH4HCO3溶液与足量NaOH溶液混合:NH4++HCO3-+2OH-═NH3?H2O+CO32-+H2O |
| D、明矾溶液中加过量的Ba(OH)2溶液:2Al3++3SO42-+3Ba2++6OH-═3BaSO4↓+2Al(OH)3↓ |
查看答案和解析>>
科目:高中化学 来源: 题型:
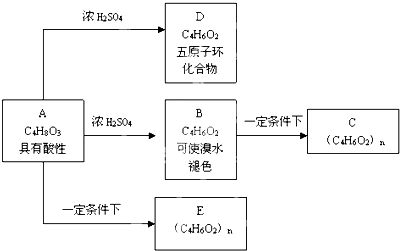
查看答案和解析>>
科目:高中化学 来源: 题型:
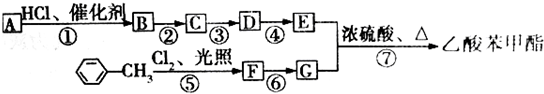
查看答案和解析>>
科目:高中化学 来源: 题型:
 某课外活动小组用题图探究铝镁合金的组成.
某课外活动小组用题图探究铝镁合金的组成.查看答案和解析>>
科目:高中化学 来源: 题型:
| A、CnH2n+2(n>1) |
| B、CnH2n(n>2) |
| C、CnH2n(n>1)和CmH2m(m>2) |
| D、CnH2n-2(n>1)与CmH2m-2(m,n>1) |
查看答案和解析>>
科目:高中化学 来源: 题型:
 据报道“全国数以万计的高校、中学化学实验室每天都排放着成分复杂的污染物”.为此我校某化学兴趣小组拟进行如下实验,以粗略测试刚做完实验的实验室(甲)空气中全部酸性气体的含量.
据报道“全国数以万计的高校、中学化学实验室每天都排放着成分复杂的污染物”.为此我校某化学兴趣小组拟进行如下实验,以粗略测试刚做完实验的实验室(甲)空气中全部酸性气体的含量.查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com