
 ,故答案为:
,故答案为: ;
; 2NaOH+Cl2↑+H2↑,
2NaOH+Cl2↑+H2↑, 2NaOH+Cl2↑+H2↑;
2NaOH+Cl2↑+H2↑;

科目:高中化学 来源: 题型:



查看答案和解析>>
科目:高中化学 来源: 题型:

| ||
| ||
| ||
| 溶解 |
| ||
| 过滤 |
| ||
| 洗涤 |
| 低温烘干、冷却、称量 |
m-
| ||
| m |
m-
| ||
| m |
查看答案和解析>>
科目:高中化学 来源:2012-2013学年河北省滦南一中高二下学期期末考试化学试卷(带解析) 题型:推断题
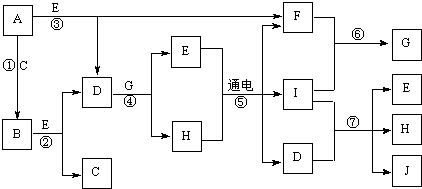
A—J均为中学化学中常见物质,C、D、G、H、I常温下均为气体,且G为单质,C常参加光合作用,其中H和I为大气污染物,E为常见的无色液体。F的焰色反应为黄色,反应①、②、③为工业反应。固体A是一种化肥,产物C、D、E的物质的量之比为1:1:1。它们之间的转化关系如下图:
(1)写出A的化学式 ,B的电子式为 ,B中含有的化学键类型是 。
(2)写出反应①的化学方程式 。
(3)少量J溶液加入F的水溶液中发生反应的离子方程式为 。
(4)氯气遇到D会产生大量白烟,常用D的浓溶液检验氯气管道是否漏气。其发生反应化学方程式为 。
(5)将G和I的混合气体60 mL通入水中,充分反应后余下气体10 mL(在相同条件下测定),则混合气体中G和I的体积比为 。
查看答案和解析>>
科目:高中化学 来源:2014届河北省高二下学期期末考试化学试卷(解析版) 题型:推断题
A—J均为中学化学中常见物质,C、D、G、H、I常温下均为气体,且G为单质,C常参加光合作用,其中H和I为大气污染物,E为常见的无色液体。F的焰色反应为黄色,反应①、②、③为工业反应。固体A是一种化肥,产物C、D、E的物质的量之比为1:1:1。它们之间的转化关系如下图:

(1)写出A的化学式 ,B的电子式为 ,B中含有的化学键类型是 。
(2)写出反应①的化学方程式 。
(3)少量J溶液加入F的水溶液中发生反应的离子方程式为 。
(4)氯气遇到D会产生大量白烟,常用D的浓溶液检验氯气管道是否漏气。其发生反应化学方程式为 。
(5)将G和I的混合气体60 mL通入水中,充分反应后余下气体10 mL(在相同条件下测定),则混合气体中G和I的体积比为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com