
| A. | 该传感器在工作过程中KOH的物质的量不变 | |
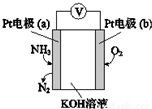
| B. | a极的电极反应式为2NH3+3O2--6e-═N2+3H2O | |
| C. | 反应消耗的NH3与O2的物质的量之比为4:5 | |
| D. | b极为负极 |
分析 该感器在工作过程中,负极上氨气失电子生成氮气,则a为负极,氧气在正极上得电子生成氢氧根离子,其电池的总反应为4NH3+3O2═4N2+6H2O,据此分析.
解答 解:A.该传感器在工作过程中总反应为4NH3+3O2═4N2+6H2O,所以KOH的物质的量不变,故A正确;
B.碱性条件下,氨气失电子生成氮气和水,则a极的电极反应式为2NH3+6OH--6e-═N2+6H2O,故B错误;
C.电池的总反应为4NH3+3O2═4N2+6H2O,则反应消耗的NH3与O2的物质的量之比为4:3,故C错误;
D.该感器在工作过程中,负极上氨气失电子生成氮气,则a为负极,故D错误;
故选A.
点评 本题考查了原电池原理,明确正负极上发生的电极反应即可解答,难点是电极反应式的书写,难度中等,侧重于考查学生的分析能力.


 学而优衔接教材南京大学出版社系列答案
学而优衔接教材南京大学出版社系列答案 小学课堂作业系列答案
小学课堂作业系列答案 金博士一点全通系列答案
金博士一点全通系列答案科目:高中化学 来源: 题型:选择题
| A. | CCl4、SiCl4、SiH4 | B. | H2S、NF3、CH4 | C. | BCl3、NH3、CO2 | D. | SO3、BF3、H3O+ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
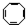 互为同分异构体且属于芳香烃的有机物的结构简式
互为同分异构体且属于芳香烃的有机物的结构简式 .
. 、
、 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
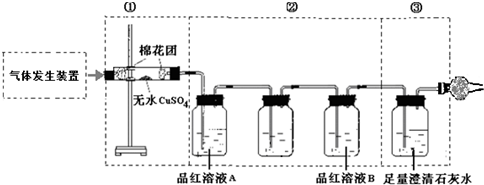
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 产率 | 75% | 65% | 88% | 72% |
| 教师对产率的评价 | 偏低 | 偏低 | 偏高 | 偏低 |
| A. | 第1组:过滤时滤纸有气泡 | |
| B. | 第2组:没有蒸发干,精盐中仍然有水分 | |
| C. | 第3组:过滤时滤液高于滤纸的边缘 | |
| D. | 第4组:滤液中还有少量泥沙就开始蒸发 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com