
һ�������£�ͨ�����з�Ӧ�����Ʊ������մɵ�ԭ��MgO��
MgSO3(s) + CO(g)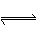 MgO(s) + CO2(g) +SO2(g) ��H��0
MgO(s) + CO2(g) +SO2(g) ��H��0
�÷�Ӧ�ں��ݵ��ܱ������дﵽƽ��������ı�ͼ�к�����x��ֵ�����´ﵽƽ���������y��x�仯���ƺ�������
| ѡ�� | x | y |
| A | �¶� | �����ڻ��������ܶ� |
| B | CO�����ʵ��� | CO2��CO�����ʵ���֮�� |
| C | SO2��Ũ�� | ƽ�ⳣ��K |
| D | MgSO4����������������� | CO��ת���� |
 Ӯ�ڿ�����ʦ��ʱ�ƻ�ϵ�д�
Ӯ�ڿ�����ʦ��ʱ�ƻ�ϵ�д� �������Ͽ�ʱͬ��ѵ��ϵ�д�
�������Ͽ�ʱͬ��ѵ��ϵ�д� �������ͬ����ϰϵ�д�
�������ͬ����ϰϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���������ĵ����з��֣��³�����������������ϱ���������Ⱦ��Ҫ��Դ��������������ϣ����Ƕ�������������ж��л������壮����һ���ж����������ͼ���£�
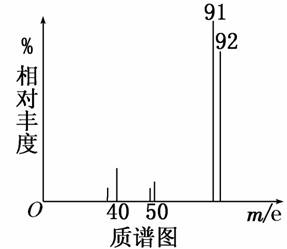
����ͼ��֪�÷��ӵ���Է���������________�����÷��ӵĺ˴Ź�����������4�����շ����л��������Ϊ________���䱽���ϵ�һ�ȴ�����________�֡�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
һδ��ƽ�����ӷ���ʽΪ______��XO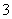 ��6H��===3X2��3H2O���ݴ��жϣ���������ͻ�ԭ��������ʵ���֮��Ϊ (����)
��6H��===3X2��3H2O���ݴ��жϣ���������ͻ�ԭ��������ʵ���֮��Ϊ (����)
A��1��1 B��3��1 C��5��1 D��7��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
һ���������ü������������������(NOx)����Ⱦ����֪��
�� ��CH4(g)��4NO2(g)==4NO(g)��CO2(g)��2H2O(g)����H����574 kJ��mol��1
�� ��CH4(g)��4NO(g)==2N2(g)��CO2(g)��2H2O(g)����H����1160 kJ��mol��1
����˵������ȷ����
A���ɷ�Ӧ �� ����֪��CH4(g)��4NO2(g)= 4NO(g)��CO2(g) ��2H2O(l)��
DH ����574 kJ/mol
B����Ӧ �٢� ת�Ƶĵ�������ͬ
C����0.2 mol CH4��ԭNO2��N2�������������·ų�������Ϊ173.4 kJ
D�����ñ�״���� 4.48LCH4 ��ԭ NO2�� N2��������������ת�Ƶĵ�������Ϊ1.60 mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��һ�������£�����CO + NO2 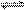 CO2 + NO �ķ�Ӧ���ﵽ��ѧƽ������¶ȣ���������ɫ��dz�������йظ÷�Ӧ��˵������ȷ����
CO2 + NO �ķ�Ӧ���ﵽ��ѧƽ������¶ȣ���������ɫ��dz�������йظ÷�Ӧ��˵������ȷ����
A������ӦΪ���ȷ�Ӧ B������ӦΪ���ȷ�Ӧ
C�����º�CO��Ũ������ D�����º�����ʵ�Ũ�Ȳ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�����й�˵����ȷ����
A��4CuO(s)=2Cu2O(s)+O2(g)�������²����Է����У�˵���÷�Ӧ��H>0
B����ϡ�����м�������ƹ��壬��ҺpH���ߵ���Ҫԭ���Ǵ�����ˮ��ʼ���
C��������K(HCN)<K(CH3COOH)��˵��CH3COOH�ĵ����һ����HCN��
D��H2S(g)+FeO(s)  FeS(s)+H2O(g)��������������ʱ����ѹǿ����Ӧ����V��(H2S)��H2S��ƽ��ת���ʾ�����
FeS(s)+H2O(g)��������������ʱ����ѹǿ����Ӧ����V��(H2S)��H2S��ƽ��ת���ʾ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
ˮ�ǵ���������ձ���ڵĻ�������ǿ���������ѧϰ�����ʽṹ�����ʵ��й�֪ʶȥ��ʶ����
��1��ˮ�����Ԫ��Ϊ����������Ļ�̬ԭ�ӵļ۵����Ų�ͼΪ______________�����ĵ�һ��������ͬ����Ԫ�����ɴ�С�ŵ�______λ��
��2�������ӻ�������ۣ�ˮ�����е���ԭ�Ӳ�ȡ���ӻ���ʽ��_______�����ݼ۲���ӶԻ������ۣ�ˮ���ӵ�VSEPRģ������Ϊ______________�����ݵȵ�����ԭ����д��ˮ�������ӵ�һ���ȵ�����(д�ṹʽ)_____________��
��3��ˮ���ӿ����γ�����ˮ���
��ˮ���ӿ����������ͭ�����γ�ˮ��ͭ����[Cu(H2O)4]2+��1molˮ��ͭ�����к��ЦҼ���ĿΪ_________��
��ͼ1��ˮ�����ᾧ��H5O2+��Cl-��H5O2+���ӵĽṹ��
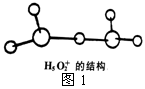
�ڸ������У����ڵ���������______________��
a����λ�� b�����Լ� c���Ǽ��Լ� d�����Ӽ�
e�������� f����� g�����»��� h���м� i���Ҽ�
��4����������ѧ��ѧ�ҽ�ˮ����һ���㹻ǿ�ĵ糡�У���20��ʱ��ˮ����˲�������γ��ˡ�ů��������ӽṹ�Ͻ�������ů����ԭ��_________________________________��
��5�������о����֣�ˮ�������13�����͵Ľᾧ�壬����ͨ������������Եı������Լ����ص����ʣ�����-30������̵ij����±������ļ�Ӳ�̶ȿɺ����������ֵܵ��ڵ����������180���������Ȼ������ȱ������еı��ܶȱ�ˮ�ų��ر���ͼ2Ϊ����һ�ֹǼ���ʽ������Ϊ��λ��ռ����졣
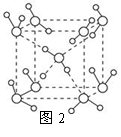
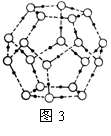
�ٸñ��е�ÿ��ˮ������_________�������
�ڱ��ڻ�����Һ̬ˮ�У�ˮ����֮���Ա����д��������ˮ������ϵ��һ�𣬷��Ӽ��������ķֲ������ṹ��Ƭ���⣬һ����Ϊ�����д����ʶ�̬ƽ��ġ��������Ķ���������ӷ�ʽ����ͼ�����ʮ�������DZ��ۻ��γɵ����������ṹ������ͼ3�еı��ۻ����Һ̬ˮȫ���γ���ͼ�����ʮ�����壬�Ҹö�����֮�����������ñ��ۻ�������������ƻ��İٷֱ�Ϊ________��
����������Ǿ���ͼ������ͣ���һ���ʵĿռ����ӷ�ʽ�����ֱ���������?____________��
����֪O��H��O����Ϊ295pm����ʽ������ֱ�������ܶ� g/cm3��(��֪2952=8.70��104��2953=2.57��107��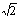 =1.41��
=1.41��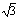 =1.73)
=1.73)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��֪������Ԫ�ص����ӣ�aA2����bB����cC3����dD����������ͬ�ĵ��Ӳ�ṹ��������������ȷ����
A��ԭ�Ӱ뾶 A��B��D��C B��ԭ������ d��c��b��a
C�����Ӱ뾶 C��D��B��A D�����ʵĻ�ԭ�� A��B��D��C
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��ҵ��ˮ�к��ж����к��ɷ֣������ŷŽ����������Ⱦ�����з��ദ����������ŷš�
��1������Cu2+�����ӵķ�ˮ��������FeS������������Ϊ��������ȥ���������ӷ���ʽ˵���������ӵ�ԭ�� ��ʵ���ҿ�����FeS��ȡH2S������H2Sͨ������NaOH��Һ�У�������Һ��Na+����������Ũ�ȹ�ϵ��c(Na+)= ��
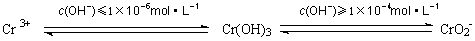 ��2��������ˮ�ж���Σ���ܴ����������ں���6�۸��ķ�ˮ�м���һ���������������������ʹ��6�۸���ԭ�ɣ�3�۸����ٵ�����ҺpH��6��8֮�䣬ʹFe3����Cr3��ת��ΪFe(OH)3��Cr(OH)3��������ȥ�������ӷ���ʽ��ʾ��ҺpH���ܳ���10��ԭ�� ��
��2��������ˮ�ж���Σ���ܴ����������ں���6�۸��ķ�ˮ�м���һ���������������������ʹ��6�۸���ԭ�ɣ�3�۸����ٵ�����ҺpH��6��8֮�䣬ʹFe3����Cr3��ת��ΪFe(OH)3��Cr(OH)3��������ȥ�������ӷ���ʽ��ʾ��ҺpH���ܳ���10��ԭ�� ��
��֪��
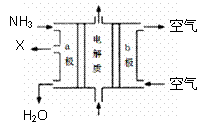 ��3����ˮ�еİ����Ի��������á�
��3����ˮ�еİ����Ի��������á�
�ٰ�����Ƴ���ͼ��ʾ�ļ���ȼ�ϵ�ء�������X�����ֱ���ŷŵ������С�a�缫�� ������缫��ӦʽΪ
��
�ڼ�ˮϡ�Ͱ�ˮ�Ĺ����У����б���ʽ����ֵ������ ��
A��c(H+) B��c(OH-)/c(NH3��H2O)
C��c(H+)��c(OH-) D��c(NH4+) +c(H+)
��T���£� NH3��H2O�ĵ��볣��ΪKa��NH4+��ˮ��ƽ�ⳣ��ΪKh������¶���ˮ�����ӻ�����Kw= ��
��һ�������£���ij�ܱ������м���һ������N2��H2�������淴Ӧ:
N2(g)��3H2(g) 2NH3(g)��H����92.2 kJ��mol��1�����0��10 s�ڣ�c(H2)��С��0.75 mol��L��1������˵����ȷ����(����)
2NH3(g)��H����92.2 kJ��mol��1�����0��10 s�ڣ�c(H2)��С��0.75 mol��L��1������˵����ȷ����(����)
A���÷�Ӧ���淴Ӧ�Ļ�ܲ�С��92.2 kJ��mol��1
B��10 s�ڰ�����ƽ����Ӧ����Ϊ0.025 mol��L��1��s��1
C��10 s��15 s��c(NH3)��������0.25 mol��L��1
D����ƽ����������NH3��ƽ��������Ӧ�����ƶ���v������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com