
某实验小组用0.50 mol/L NaOH溶液和0.50 mol/L硫酸溶液进行中和热的测定。测定中和热的实验装置如图所示.
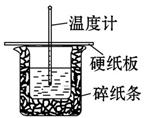
(1)大小烧杯之间填满碎泡沫塑料的作用是_________________,从实验装置上看,图中缺少的一种玻璃仪器_________________.
(2)写出该反应的用中和热表示的热化学方程式(中和热为57.3kJ/mol) 。
(3)取50 mL NaOH溶液和30 mL硫酸溶液进行实验,实验数据如下表
①请填写下表中的空白:
实验 次数 | 起始温度t1/℃ | 终止温度 t2/℃ | 温度差 (t2-t1)/℃ | 温度差平均值 (t2-t1)/℃ | ||
H2SO4 | NaOH | 平均值 | ||||
1 | 26.2 | 26.0 | 26.1 | 30.1 | 4.0 | |
2 | 27.0 | 27.4 | 27.2 | 33.3 | 6.1 | |
3 | 25.9 | 25.9 | 25.9 | 29.8 | 3.9 | |
4 | 26.4 | 26.2 | 26.3 | 30.4 | 4.1 | |
②近似认为0.50 mol/L NaOH溶液和0.50 mol/L硫酸溶液的密度都是1 g/cm3,中和后生成溶液的比热容C=4.18J/(g·℃)。则中和热ΔH=__________(取小数点后一位)。(已知:Q=m·c·Δt)
③上述实验数值结果与57.3kJ/mol有偏差,产生偏差的原因可能是(填字母)__________。
a.实验装置保温、隔热效果差
b.量取NaOH溶液的体积时仰视读数
c.分多次把NaOH溶液倒入盛有硫酸的小烧杯中
(4)实验中若用60mL0.25mol·L-1H2SO4溶液跟50mL0.55mol·L-1NaOH溶液进行反应,与上述实验相比,所放出的热量__________(填“相等”、“不相等”),所求中和热__________(填“相等”、“不相等”);,若用50mL0.50mol·L-1醋酸代替H2SO4溶液进行上述实验,测得反应前后温度的变化值会__________(填“偏大”、“偏小”、“不受影响”).
科目:高中化学 来源:2016-2017学年浙江省高一上10月月考化学试卷(解析版) 题型:填空题
有下列物质:①NaOH溶液 ②铜丝 ③液态HCl ④盐酸 ⑤Na2SO3固体 ⑥CO2 ⑦酒精 ⑧葡萄糖 ⑨氧化钠 ⑩熔融氯化钠
(1)上述物质中,可导电的是 。
(2)上述物质中,属于非电解质的是 。
(3)上述状态下,属于电解质但不导电的是 。
(4)写出Na2SO3的电离方程式: 。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年四川省高二上10月月考化学试卷(解析版) 题型:选择题
在一定温度下,向一个容积为2 L的密闭容器内(预先加入催化剂)通入2mol NH3,经过一段时间后,测得容器内的压强为起始时的1.2倍。则NH3的转化率为
A.25% B.20% C.10% D.80%
查看答案和解析>>
科目:高中化学 来源:2016-2017学年广西省高一上9月月考化学试卷(解析版) 题型:选择题
由CH4和O2组成的混合气体,标准状况下的密度为1g.L-1,则该混合气体中CH4和O2的体积比为( )
A.2:1 B.1:2 C.2:3 D.3:2
查看答案和解析>>
科目:高中化学 来源:2016-2017学年广西省高一上9月月考化学试卷(解析版) 题型:选择题
下列实验操作中错误的是( )
A. 分液时,分液漏斗下层液体从下口放出,上层液体从上口倒出
B. 蒸馏时,应使温度计水银球靠近蒸馏烧瓶支管口
C. 蒸发结晶时应将溶液蒸干
D. 称量时,称量物放在称量纸上置于托盘天平的左盘,砝码放在托盘天平的右盘中
查看答案和解析>>
科目:高中化学 来源:2016-2017学年广西省高二上9月月考化学试卷(解析版) 题型:选择题
已知下列热化学方程式:
(1)CH3COOH(l)+2O2(g)=2CO2(g)+2H2O(l)△H1=-870.3kJ·mol-1
(2)C(s)+O2(g)=CO2(g)△H2=-393.5kJ·mol-1
(3)H2(g)+1/2O2(g)=H2O(l)△H3=-285.8kJ·mol-1
则反应2C(s)+2H2(g)+O2(g) = CH3COOH(l) 的△H为( )
A.-488.3 kJ·mol-1 B.-244.15 kJ·mol-1
C.+488.3 kJ·mol-1 D.+244.5 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源:2016-2017学年广西省高二上9月月考化学试卷(解析版) 题型:选择题
在一定条件下当64gSO2气体完全被氧化成SO3气体时,共放出热量98.3kJ,据此推断,下列热化学方程式正确的是( )
A.SO2(g)+1/2O2(g) SO3(g);△H=-98.3KJ·mol-1
SO3(g);△H=-98.3KJ·mol-1
B.2SO2(g)+O2(g) 2SO3(l);△H=-196.6KJ·mol-1
2SO3(l);△H=-196.6KJ·mol-1
C.SO2(g)+1/2O2(g) SO3(g);△H=-78.64KJ·mol-1
SO3(g);△H=-78.64KJ·mol-1
D.2SO2(g)+O2(g) 2SO3(g);△H=+196.6KJ·mol-1
2SO3(g);△H=+196.6KJ·mol-1
查看答案和解析>>
科目:高中化学 来源:2016-2017学年宁夏高一上学期期中化学卷(解析版) 题型:选择题
下列各组数据中,前者刚好是后者两倍的是( )
A.2 mol水的摩尔质量和1 mol水的摩尔质量
B.200 mL 1 mol/L氯化钙溶液中c(Cl-)和100 mL 2 mol/L氯化钾溶液中c(Cl-)
C.64 g二氧化硫中氧原子数和标准状况下 22.4 L一氧化碳中氧原子数
22.4 L一氧化碳中氧原子数
D.20%NaOH溶液中NaOH的物质的量 浓度和10%NaOH溶液中NaOH的物质的量浓度
浓度和10%NaOH溶液中NaOH的物质的量浓度
查看答案和解析>>
科目:高中化学 来源:2016-2017学年内蒙古高二上10月月考化学卷(解析版) 题型:实验题
碳酸氢铵是我国主要的氮肥品种之一,在贮存和运输过程中容易挥发损失。为了鉴定其质量和确定田间施用量,必须测定其含氮量。
Ⅰ.某学生设计了一套以测定二氧化碳含量间接测定含氮量的方法。将样品放入圆底烧瓶中:
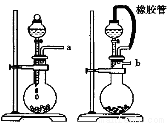
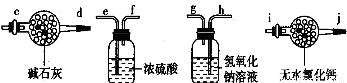
(1)请选择必要地装置,按气流方向连接顺序为 。
(2)分液漏斗中的液体最适合的是 。
A.稀盐酸 B.稀硫酸 C.浓硝酸 D.氢氧化钠
(3)连在最后的装置起到的作用 。
Ⅱ.如果氮肥中成分是(NH4)2SO4,则可以用甲醛法测定含氮量。甲醛法是基于甲醛与一定量的铵盐作用,生成相当量的酸,反应为2(NH4)2SO4+6HCHO=(CH2)6N4 +2H2SO4 + 6H2O,生成的酸再用氢氧化钠标准溶液滴定,从而测定氮的含量。步骤如下:
(4)用差量法称取固体(NH4)2SO4样品0.6g于烧杯中,加入约30mL蒸馏水溶解,最终配成100mL溶液。用 (填“酸式”或“碱式”)滴定管准确取出20.00mL的溶液于锥形瓶中,加入18%中性甲醛溶液5mL,放置5min后,加入1~2滴 指示剂(已知滴定终点的pH约为8.8),用浓度为0.08mol/L氢氧化钠标准溶液滴定,读数如下表:
滴定次数 | 滴定前读数(mL) | 滴定后读数(mL) |
1 | 1.20 | 16.21 |
2 | 3.00 | 18.90 |
3 | 4.50 | 19.49 |
达滴定终点时的现象为 ,由此可计算出该样品中的氮的质量分数为 。
(5)在滴定实验结束后发现滴定用的碱式滴定管玻璃尖嘴内出现了气泡,滴定开始时无气泡,则此实验测定的含氮量比实际值 (填“偏大”“偏小”或“无影响”)。
Ⅲ.如果测定碳酸氢铵中的含氮量时,使用甲醛法是否合理 (填“是”或“否”),理由是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com