
随着各地“限牌”政策的推出,电动汽车成为汽车届的“新宠”。特斯拉全电动汽车使用的是钴酸锂(LiCoO2)电池,其工作原理如右图,A 极材料是金属锂和碳的复合材料(碳作为金属锂的载体),电解质为一种能传导Li+的高分子材料,隔膜只允许特定的离子通过,电池反应式LixC6+Li1-xCoO2 C6+LiCoO2。下列说法不正确的是
C6+LiCoO2。下列说法不正确的是
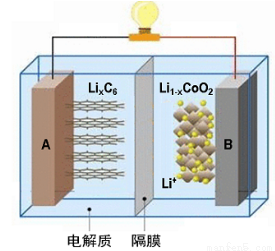
A.据题意分析可知该隔膜只允许Li+通过,放电时Li+从左边流向右边
B.充电时,A为阴极,发生还原反应
C.放电时,B为正极,电极反应式为:Li1-x CoO2+ xLi++ xe-= LiCoO2
D.废旧钴酸锂(LiCoO2)电池进行“放电处理”让Li+进入石墨中而有利于回收
科目:高中化学 来源:2016-2017学年山西省高二12月月考化学试卷(解析版) 题型:选择题
已知25℃时一些难溶物质的溶度积常数如下:
化学式 | Zn(OH)2 | ZnS | AgCl | Ag2S | MgCO3 | Mg(OH)2 |
溶度积 | 5×10-17 | 2.5×10-22 | 1.8×10-10 | 6.3×10-50 | 6.8×10-6 | 1.8×10-11 |
根据上表数据,判断下列化学方程式不正确的是
A.2AgCl+Na2S═2NaCl+Ag2S
B.MgCO3+H2O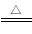 Mg(OH)2+CO2↑
Mg(OH)2+CO2↑
C.ZnS+2H2O═Zn(OH)2+H2S↑
D.Mg(HCO3)2+2Ca(OH)2═Mg(OH)2↓+2CaCO3↓+2H2O
查看答案和解析>>
科目:高中化学 来源:2016-2017学年内蒙古高一期中化学卷(解析版) 题型:选择题
已知反应SO2+2H2S=2H2O+3S,则氧化产物与还原产物的质量比为
A.1:1 B.2:1 C.3:1 D.1:2
查看答案和解析>>
科目:高中化学 来源:2016-2017学年内蒙古高一期中化学卷(解析版) 题型:选择题
下列化学反应中,水作为还原剂的是
A.CO+ H2O高温CO2+H2
H2O高温CO2+H2
B.3NO2+H2O=2HNO3+NO
C.CO2+H2O=H2CO3
D.2F2+2H2O=4HF+O2
查看答案和解析>>
科目:高中化学 来源:2016-2017学年江西省高二上段考二化学试卷(解析版) 题型:填空题
I、铁及其化合物与生产、生活关系密切。
(1)右图是实验室研究海水对铁闸不同部位腐蚀情况的剖面示意图.
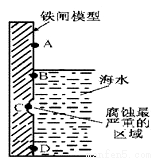
①该电化腐蚀称为___________。
②图中A、B、C、D四个区域,生成铁锈最多的是___________ (填字母)。
(2)己知:Fe(s)+O2(g)=FeO(s)H=-272.0kJ•mol-1
C(s)+O2(g)=CO2(g);△H=-393.5kJ•mol-1
2C(s)+O2(g)=2CO(g);△H=-221kJ•mol-1
则高炉炼铁过程中FeO(s)+CO Fe(S)+CO2(g) △H=____________。
Fe(S)+CO2(g) △H=____________。
II、甲醇是一种重要的化工原料和新型燃料。下图是甲醇燃料电池工作的示意图,其中A、B、D均为石墨电极,C为铜电极.工作一段时间后,断开K,此时A,B两极上产生的气体体积相同。
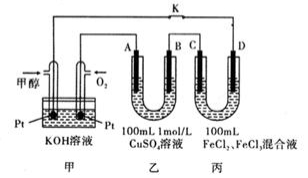
(1)甲中负极的电极反应式为_________________。
(2)乙中A极析出的气体在标准状况下的体积为_____________。
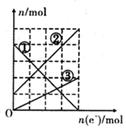
(3)丙装置溶液中金属阳离子的物质的量与转移电子的物质的量变化关系右图,则图中②线表示的是_____________离子的变化;反应结束后,要使丙装置中金属阳离子恰好完全沉淀,需要_________________mL 5.0 mol•L-1 NaOH溶液。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年江西省高二上段考二化学试卷(解析版) 题型:选择题
下列有关电解质溶液中粒子的物质的量浓度大小关系正确的是( )
A.等物质的量浓度的下列溶液:①H2CO3、②Na2CO3、③NaHCO3、④(NH4)2CO3: 其中c(CO32-)的大小关系为:②>④>③>①
B.pH=2 的H2C2O4 溶液与pH=12 的NaOH 溶液等体积混合: c(Na+)+c(H+) =c(OH-)+c(HC2O4-)+c(C2O42-)
C.向0.2 mol/LNaHCO3 溶液中加入等体积0.1 mol/LNaOH 溶液: c(CO32-)>c(HCO3-)>c(OH-)>c(H+)
D.常温下,同浓度的CH3COONa 与CH3COOH 溶液等体积混合,溶液的pH<7: c(CH3COOH)+c(OH-)>c(Na+)+c(H+)
查看答案和解析>>
科目:高中化学 来源:2016-2017学年江西省高二上段考二化学试卷(解析版) 题型:选择题
下列叙述中,不能用勒夏特列原理解释的是
A.配制FeCl3溶液时加入少量的浓盐酸
B.常温下,NaOH溶液中由水电离出的C(H+)<1×10-7mol/L
C.由H2、I2(g)、HI(g)气体组成的平衡体系加压后颜色变深
D.AgCl在水中的溶解度大于在饱和NaCl溶液中的溶解度
查看答案和解析>>
科目:高中化学 来源:2017届福建省高三上学期期中化学试卷(解析版) 题型:推断题
)某抗结肠炎药物有效成分的合成路线如下(部分反应略去试剂和条件):
已知:(a)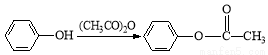
(b)
根据以上信息回答下列问题:
(1)C 的结构简式是 。抗结肠炎药物有效成分分子中的含氧官能团名称是 。
的结构简式是 。抗结肠炎药物有效成分分子中的含氧官能团名称是 。
(2)①的反应条件是 ,②的反 应类型是 。
应类型是 。
(3)下列对抗结肠炎药物有效成分可能具有的性质推测正确的是: 。
A.能发生取代反应 B.能发生消去反应
C.能发生加 聚反应 D.既有酸性又有碱性
聚反应 D.既有酸性又有碱性
(4)E与足量NaOH溶液反应的化学方程式是 。
(5)符合下列条件的E的同分异构体还有 种,写出其中核磁共振氢谱图有四种峰的结构简式 。
a.与E具有相同的官能团且官能团不在同一侧链
b.水解产物之一能与氯化铁发生显色反应
(6)已知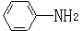 易被氧化,苯环上连有烷基时再引入一个取代基,常取代在烷基的邻对位,而当苯环上连有羧基时则取代在间位。据此写出以A为原料合成化合物
易被氧化,苯环上连有烷基时再引入一个取代基,常取代在烷基的邻对位,而当苯环上连有羧基时则取代在间位。据此写出以A为原料合成化合物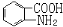 的合成路线。(仿照题中抗结肠炎药物有效成分的合成路线的表达
的合成路线。(仿照题中抗结肠炎药物有效成分的合成路线的表达 方式答题)
方式答题)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com