
某温度时,在2L的密闭容器中,X、Y、Z三种物质的量随时间的变化曲线如右图所示。
(1)由图中所给数据进行分析,该反应的化学方程式为___________________________________;
(2)反应从开始至2分钟末,用Z的浓度变化表示的平均反应速率为v(Z)=__________________。
Ⅱ(7分)将2mol H2O和2mol CO置于1L容器中,加热至高温,发生如下可逆反应:
2H2O(g)  2H2(g)+O2(g),2CO(g)+O2(g)
2H2(g)+O2(g),2CO(g)+O2(g)  2CO2(g)。
2CO2(g)。
(3)当上述系统达到平衡时,欲求混合气体的平衡组成,至少还需要知道两种气体的平衡浓度,但这两种气体不能同时是________和________,或________和________(填分子式)。
(4)若平衡时O2和CO2的物质的量分别为a mol和b mol,则平衡时H2O的物质的量为_______________________ (用含a、b的代数式表示)
科目:高中化学 来源: 题型:
下列各组离子在溶液中不能大量共存,且加入过量NaOH溶液或过量稀盐酸均能得到澄清溶液的是 ( )
A. Fe3+、CI-、Na+、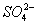 B. Al3+、Na+、
B. Al3+、Na+、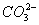 、
、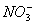
C. Ag+、Na+、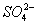 、
、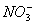 D. AlO2-、
D. AlO2-、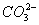 、K+、Na+
、K+、Na+
查看答案和解析>>
科目:高中化学 来源: 题型:
室温下,有关下列四种溶液的叙述正确的是(忽略溶液混合的体积变化)
| ① | ② | ③ | ④ | |
| pH | 12 | 12 | 2 | 2 |
| 溶液 | 氨水 | 氢氧化钠溶液 | 醋酸 | 盐酸 |
A.在①、②中分别加入氯化铵晶体,两溶液的pH值均增大
B.分别将等体积的①和②加水稀释120倍,所得溶液的pH:①>②
C.把①、④两溶液等体积混合后所得溶液中:c(Cl-)>c(NH4+)>c(OH-)>c(H+)
D.将溶液②和溶液③等体积混合,混合后所得溶液pH=7
查看答案和解析>>
科目:高中化学 来源: 题型:
在冶金工业上,通常均不能用化学还原剂制得的金属组是( )
A.Na、Ba、Mg、A1 B.Zn、Fe、Cu、Ag
C.Na、K、Zn、Fe D.Mg、Al、Zn、Fe
查看答案和解析>>
科目:高中化学 来源: 题型:
某原电池总反应的离子方程式为2Fe3++Fe=3Fe2+,能实现该反应的原电池组成是( )
A.正极为铁,负极为铜,电解质溶液为FeCl3溶液
B.正极为碳,负极为铁,电解质溶液为Fe(NO3)3溶液
C.正极为铁,负极为锌,电解质溶液为Fe2(SO4)3溶液
D.正极为银,负极为铁,电解质溶液为CuSO4溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
在一定条件下,对于反应2A(g)+B(g)  2C(g),下列说法中正确的是
2C(g),下列说法中正确的是
A.此反应的平衡常数K= 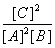
B.改变条件该反应的平衡常数K一定不变
C.改变压强并加入催化剂,平衡常数会随之变化
D.平衡时增大A和B的浓度,平衡常数会减小
查看答案和解析>>
科目:高中化学 来源: 题型:
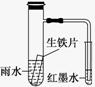
右图小试管内为红墨水,具支试管内盛有pH=4久置的雨水和生铁片。实验观察到:开始时导管内液面下降,一段时间后导管内液面回升,略高于小试管内液面。下列说法正确的是
A.生铁片中的碳是原电池的负极,发生还原反应
B.雨水酸性较强,生铁片始终发生析氢腐蚀
C.墨水回升时,碳电极反应式为O2+2H2O+4e-===4OH-
D.具支试管中溶液酸性增强
查看答案和解析>>
科目:高中化学 来源: 题型:
下列溶液中有关微粒的物质的量浓度关系不正确的是( )
A. 物质的量浓度相等的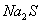 和
和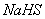 混合溶液中:
混合溶液中:
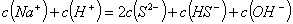
B. 常温下将醋酸钠、盐酸两溶液混合后,溶液呈中性,则混合后溶液中:
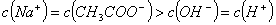
C. 常温下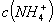 相等的①
相等的①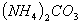 、②
、②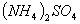 、③
、③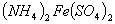 三种溶液中,溶质的物质的量浓度大小:①>②>③
三种溶液中,溶质的物质的量浓度大小:①>②>③
D. 等体积、等物质的量浓度的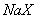 和弱酸
和弱酸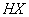 混合后呈酸性的溶液中:
混合后呈酸性的溶液中:
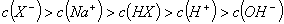
查看答案和解析>>
科目:高中化学 来源: 题型:
右图表示某固态单质A及其化合物之间的转化关系(某些产物和反应条件已略去)。化合物B在常温常压下为气体,B和C的相对分子质量之比为4∶5,化合物D是重要的工业原料。
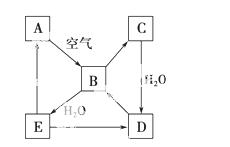
(1)写出A在加热条件下与H2反应的化学方程式:
________________________________________________________;
(2)写出E与A的氢化物反应生成A的化学方程式:
_____________________________________________________________;
(3)写出一个由D生成B的化学方程式:
_____________________________________________________________;
(4)将5 mL 0.10 mol·L-1的E溶液与10 mL 0.10 mol·L-1的NaOH溶液混合。
①写出反应的离子方程式:___________________________________________
_______________________________________;
②反应后溶液的pH________7(填“大于”“小于”或“等于”),理由是______________________________________________________________;
③加热反应后的溶液,其pH________(填“增大”“不变”或“减小”),理由是_______________________________________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com