
���� ����������̽��
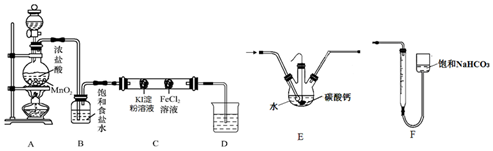
��1��װ��A���Ʊ������ķ���װ�ã��Ŷ������̵�����ΪԲ����ƿ��
��2�����ɵ���������ˮ�������Ȼ��⣬ͨ������ʳ��ˮ��ȥ�Ȼ����������ʣ�
��3�������������Կ��������⻯�����ɵⵥ�ʣ��������۱���ɫ��
��4������������������Һ��Ӧ�����Ȼ��ơ��������ƺ�ˮ�������ᷢ�����з�Ӧ����������
��5�����װ��E������ͼ��װ��C�������Ʊ��ϸ�Ũ�ȵ�HClO��Һ����Բ����ƿ�ײ�����һ����������ס�Ĺ�����״̼��ƣ����ɵ�������ˮ��Ӧ��������ʹ����ᣬ��������������̼�ᣬ�����̼��Ʒ�Ӧ���ɶ�����̼��
��������ˮ��Ӧ���ڻ�ѧƽ�⣬���ɵ������̼��Ʒ�Ӧ�ٽ�ƽ��������У�
�ڷ�Ӧ��������������ʣ���ʯ��ʯ���Һ�棬���õ���Һ��ϡ�����ϣ�������������CO2���壬˵����Һ�к���̼����ƣ������ɵĶ�����̼��̼��Ʒ�Ӧ���ɵ�̼����ƣ�������Һ�д��ڴ����ᡢ�Ȼ��ơ�������ƣ���С��ͬѧ��÷�Ӧ��̼�����������M gΪ̼��ƣ���Ӧ������õ�200mL��Һ��ȡ��10mL������ϡ�����ϣ�����Fװ�ò�ò������������ΪV L���ѻ���ɱ�״���������ݷ�Ӧ������ϵ��CaCO3��Ca��HCO3��2��2CO2�������ɶ�����̼�����̼��Ƶ��������õ������Ȼ��Ƶ�̼��Ƶ����������ݸ�Ԫ���غ�õ�ԭ��Һ�к������ε�Ũ�ȣ�
��� �⣺����������̽��
��1��װ��A���Ʊ������ķ���װ�ã���������Ϊ����͵����������ȷ�Ӧ����������ʢ�Ŷ������̵�����ΪԲ����ƿ���ʴ�Ϊ��Բ����ƿ��
��2�����ɵ���������ˮ�������Ȼ��⣬�Ȼ��⼫������ˮ���Ȼ�����Һ������������������ˮ�ķ�Ӧ��ͨ������ʳ��ˮ��ȥ�Ȼ����������ʣ�
�ʴ�Ϊ����ȥ�����е��Ȼ��⣻
��3�������������Կ��������⻯�����ɵⵥ�ʣ�2KI+Cl2=I2+2KCl���ⵥ���������۱���ɫ���ʴ�Ϊ������ɫ��
��4������������������Һ��Ӧ�����Ȼ��ơ��������ƺ�ˮ�������ᷢ�����з�Ӧ������������Ӧ�����ӷ���ʽΪ��ClO-+Cl-+2H+=Cl2��+H2O��
�ʴ�Ϊ��ClO-+Cl-+2H+=Cl2��+H2O��
��5���ٸ÷��������Ƶýϸ�Ũ��HClO��ԭ������Һ�д��ڻ�ѧƽ�⣺Cl2+H2O H++Cl-+HClO��̼�����H+��Ӧ��ʹƽ�������ƶ���HClOŨ�����õ��ϸ�Ũ��HClO��
�ʴ�Ϊ��Cl2+H2O?H++Cl-+HClO��̼�����H+��Ӧ��ʹƽ�������ƶ���HClOŨ������
�ڷ�Ӧ��������������ʣ���ʯ��ʯ���Һ�棬���õ���Һ��ϡ�����ϣ�������������CO2���壬˵����Һ�к���̼����ƣ������ɵĶ�����̼��̼��Ʒ�Ӧ���ɵ�̼����ƣ�������Һ�д��ڴ����ᡢ�Ȼ��ơ�������ƣ���С��ͬѧ��÷�Ӧ��̼�����������M gΪ̼��ƣ���Ӧ������õ�200mL��Һ��ȡ��10mL������ϡ�����ϣ�����Fװ�ò�ò������������ΪV L���ѻ���ɱ�״���������ݷ�Ӧ������ϵ��CaCO3��Ca��HCO3��2��2CO2����200ml��Һ�����ɶ�����̼��̼�������=��$\frac{V}{22.4}��\frac{1}{2}$��mol��$\frac{200}{10}$��100g/mol����ԭ��Һ�к������ε�Ũ��=$\frac{M-\frac{V}{44.8}mol��20��100g/mol}{100g/mol��0.2L}$=$\frac{M}{20}$-$\frac{V}{0.448}$��
�ʴ�Ϊ��CaCl2��Ca��HCO3��2��$\frac{M}{20}$-$\frac{V}{0.448}$��
���� ���⿼�����������ʺ���ɵ�ʵ��̽��������ʵ����̷��������ݴ������������ʵ�֪ʶ�㣬���ջ����ǽ���ؼ�����Ŀ�Ѷ��еȣ�


 �ŵ������ϵ�д�
�ŵ������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| A�� | Ca2+��Al3+��HCO3-��Cl- | B�� | K+��Ba2+��Cl-��NO3- | ||
| C�� | Na+��AlO2-��OH-��SO42- | D�� | Na+��NH4+��Cl-��K+ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ��ѧ�� | N-H | N-N | N��N | O-H |
| E/��kJ•mol-1�� | 390 | 190 | 946 | 460 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ��Ӧ���ͼӾ۷�Ӧ
��Ӧ���ͼӾ۷�Ӧ ��Ӧ����ȡ����Ӧ
��Ӧ����ȡ����Ӧ ��Ӧ����ȡ����Ӧ
��Ӧ����ȡ����Ӧ�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
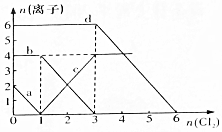 ��֪Cl-��Br-��Fe2+��I-�Ļ�ԭ��������ǿ������FeBr2��FeI2�Ļ����Һ��ͨ��������������Һ��ijЩ���ӵ����ʵ����仯��ͼ��ʾ����ش�
��֪Cl-��Br-��Fe2+��I-�Ļ�ԭ��������ǿ������FeBr2��FeI2�Ļ����Һ��ͨ��������������Һ��ijЩ���ӵ����ʵ����仯��ͼ��ʾ����ش��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �ӻ��������Ŀ����״�Ͳ����ӻ���ԭ�ӹ����Ŀ����״����ͬ | |
| B�� | �����ӻ��������״��������ȣ� NH3��N�ǵ����ӻ� | |
| C�� | ���ӻ�����ڿռ�Ӧ������ӶԻ������ۣ���ʹ�ų�����С | |
| D�� | sp3�ӻ����Ӧ��ͬԭ����������ͬ��s��p����ӻ����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����ʹ��Һ��pH���� | |
| B�� | ����ʹ��Һ��c��H+��•c��CH3COO-����С | |
| C�� | ����ʹ��Һ��$\frac{c��C{H}_{3}CO{O}^{-}��}{c��C{H}_{3}COOH��}$��ֵ���� | |
| D�� | ��Һ��$\frac{c��{H}^{+}��•c��C{H}_{3}CO{O}^{-}��}{c��C{H}_{3}COOH��}$���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
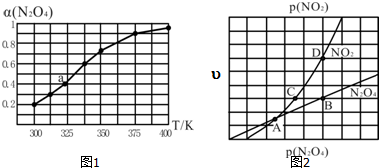
 ��ҵ����һ����C02�������״�ȼ�ϵķ�����CO2��g��+3H2��g��?CH3OH��g��+H2O��g����H=-49.0kJ•mol-1����6mol CO2��8mol H2����2L���ܱ������У����H2�����ʵ�����ʱ��仯��ͼ��ʾ��ʵ�ߣ���ͼ������a��1��6����ʾ����1minʱH2�����ʵ�����6mol��
��ҵ����һ����C02�������״�ȼ�ϵķ�����CO2��g��+3H2��g��?CH3OH��g��+H2O��g����H=-49.0kJ•mol-1����6mol CO2��8mol H2����2L���ܱ������У����H2�����ʵ�����ʱ��仯��ͼ��ʾ��ʵ�ߣ���ͼ������a��1��6����ʾ����1minʱH2�����ʵ�����6mol���鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com