
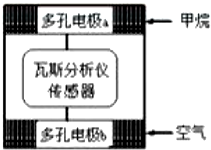
 瓦斯爆炸是煤矿开采中的重大危害,一种瓦斯分析仪能够在煤矿巷道中的甲烷浓度达到一定浓度时,可以通过传感器显示.该瓦斯分析仪工作原理类似燃料电池的工作原理,其装置如下图所示,其中的固体电解质是 Y2O3-Na2O,O2-可以在其中自由移动.下列有关叙述正确的是( )
瓦斯爆炸是煤矿开采中的重大危害,一种瓦斯分析仪能够在煤矿巷道中的甲烷浓度达到一定浓度时,可以通过传感器显示.该瓦斯分析仪工作原理类似燃料电池的工作原理,其装置如下图所示,其中的固体电解质是 Y2O3-Na2O,O2-可以在其中自由移动.下列有关叙述正确的是( )| A. | 瓦斯分析仪工作时,电池内电路中电子由电极b 流向电极a | |
| B. | 电极b 是正极,O2-由电极 a流向电极b | |
| C. | 电极a的反应式为:CH4+4O2--8e-=CO2+2H2O | |
| D. | 当固体电解质中有1 mol O2- 通过时,电子转移 4 mol |
分析 瓦斯分析仪工作原理类似燃料电池的工作原理,其装置如图乙所示,其中的固体电解质是Y2O3-Na2O,O2-可以在其中自由移动.电子在外电路转移,通甲烷气体的为负极,通空气一端为正极,电池总反应为CH4+2O2=CO2+H2O,正极反应为:O2+4e-=2O2-,负极反应为:CH4+4O2--8e-=CO2+2H2O,结合原电池的原理和电极反应回答问题.
解答 解:A.电子不能在电池内电路流动,只能在外电路中流动,且电子由负极经导线流向正极,故A错误;
B.电极b氧气得电子,生成O2-,而电极a需要O2-作为反应物,故O2-由正极(电极b)流向负极(电极a),故B错误;
C.甲烷所在电极a为负极,电极反应为:CH4+4O2--8e-=CO2+2H2O,故C正确;
D.1mol O2得4mol电子生成2molO2-,故当固体电解质中有1mol O2-通过时,电子转移2mol,故D错误.
故选C.
点评 本题考查原电池知识,为高频考点,侧重于学生分析能力和基本理论的理解和运用的考查,注意把握金属的活泼性强弱以及电极方程式的书写,难度不大.


 激活思维优加课堂系列答案
激活思维优加课堂系列答案 活力试卷系列答案
活力试卷系列答案 课课优能力培优100分系列答案
课课优能力培优100分系列答案科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2:1 | B. | 1:2 | C. | 11:2 | D. | 2:11 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
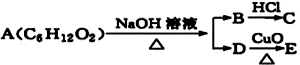 ,已知C能与NaHCO3反应产生气体,且C、E均不发生银镜反应,则A的可能结构有( )
,已知C能与NaHCO3反应产生气体,且C、E均不发生银镜反应,则A的可能结构有( )| A. | 1种 | B. | 2种 | C. | 3种 | D. | 4种 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com