
在标准状况下,将SO2和Cl2气体混合,测得混合气体相对HCl的密度是1.85.将该混合气体2.24 L溶于100 mL水中制成溶液,已知该溶液的密度为1.05 g/cm3.(已知:SO2+Cl2+2H2O![]() H2SO4+2HCl)计算该混合溶液中H+的物质的量浓度.(计算最终结果保留两位小数)
H2SO4+2HCl)计算该混合溶液中H+的物质的量浓度.(计算最终结果保留两位小数)
科目:高中化学 来源: 题型:
| 阳离子 | K+、Ag+、Mg2+、Ba2+ | ||||||||
| 阴离子 | NO
|
| 序号 | 实验内容 | 实验结果 |
| Ⅰ | 想该溶液中加入足量稀盐酸 | 生成白色沉淀并在标准状况下放出0.56L气体 |
| Ⅱ | 将Ⅰ中产生的混合液过滤,将沉淀洗涤、灼烧至恒重,称量所得固体的质量 | 固体质量为2.4g |
| Ⅲ | 向Ⅱ中所得的滤液中滴加BaCl2溶液 | 无明显现象 |
| 阴离子 | NO
|
CO
|
SiO
|
SO
| ||||||||
| c/mol?L-1 | ? ? |
0.25mol/L 0.25mol/L |
0.4mol/L 0.4mol/L |
0 0 |
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
2- 4 |
2- 4 |
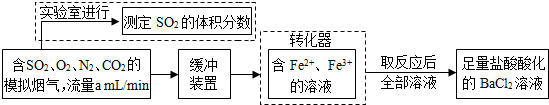
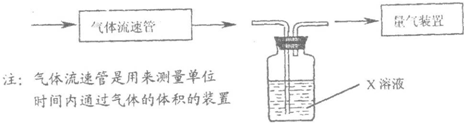
2- 4 |
| 1 |
| x |
| 1 |
| x |
| 3 |
| x |
+ 4 |
- 3 |
+ 4 |
- 3 |
- 3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列离子反应方程式书写正确的是 ( )
A.在Ba(OH)2溶液中加入少量的硫酸氢钠溶液Ba2++2OH-+2H++SO![]() =BaSO4↓+2H2O
=BaSO4↓+2H2O
B.向次氯酸钙溶液中通入SO2气体Ca2++2ClO-+SO2+H2O=CaSO3↓+2HClO
C.标准状况下,将112mLCl2缓慢注入10mL 1mol·L-1的FeBr2溶液中
2Fe2++4Br-+3Cl2 =2Fe3++6Cl-+2Br2
|
↓+HCO![]()
查看答案和解析>>
科目:高中化学 来源:2015届天津市高一第一次月考化学试卷(解析版) 题型:填空题
(15分)(1)3.01×1022个OH¯的物质的量为 ;这些OH¯与 molNH3的质量相等,与 g Na+含有的离子数相同。
(2)在标准状况下,2.24LNOx气体的质量为4.6g,则x的值为 。
(3)有四种正盐的混合溶液,含有0.2 mol·L-1 Na+、0.25 mol·L-1 Mg2+、0.4mol·L-1
Cl-,则SO 的浓度为
的浓度为
(4)、用14.2g硫酸钠配制成500mL溶液,其物质的量浓度为 mol/L。若从中取出50mL,其物质的量浓度为 mol/L,溶液中含Na+的个数为
若将这50mL溶液用水稀释到100mL, SO42-的物质的量浓度为 mol/L。
查看答案和解析>>
科目:高中化学 来源:2013届度江西省高二第二学期第一次月考化学试卷 题型:选择题
下列离子反应方程式书写正确的是
A.在Ba(OH)2溶液中加入少量的硫酸氢钠溶液Ba2++2OH-+2H++SO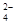 =BaSO4↓+2H2O
=BaSO4↓+2H2O
B.向次氯酸钙溶液中通入SO2气体Ca2++2ClO-+SO2+H2O=CaSO3↓+2HClO
C.标准状况下,将112mLCl2缓慢注入10mL 1mol·L-1的FeBr2溶液中
2Fe2++4Br-+3Cl2 =2Fe3++6Cl-+2Br2
D.向苯酚钠溶液中通入少气体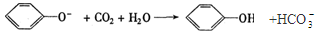
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com