
����Ŀ��A��B��C��D��ԭ���������������ǰ������Ԫ�أ�A�����ڱ���ԭ�Ӱ뾶��С��Ԫ�أ�������ɵĵ��ʻ�������ͼת����ϵ�����мס��������ǵ��ʣ��ҡ����ͼ�����������ж�����������������Ϻ�ɫ��������ش�����������

��1��DԪ�ص�Ԫ�ط���Ϊ______________��CԪ�������ڱ��е�λ��Ϊ_____________��
��2���õ���ʽ��ʾ�����γɹ���_____________��
��3����Ӧ���ڹ�ҵ������ͨ������_____________��Ӧ��
��4���ס�����Ũ������γ�ԭ��أ�����________________���ѧʽ���������������缫��ӦʽΪ__________________________��
���𰸡� Cu ����������A�� ![]() ���� Cu NO3-+e-+2H+=NO2��+H2O
���� Cu NO3-+e-+2H+=NO2��+H2O
��������A��B��C��D��ԭ���������������ǰ������Ԫ�أ�A�����ڱ���ԭ�Ӱ뾶��С��Ԫ�أ�AΪHԪ�أ�������ɵĵ��ʻ�������ͼת����ϵ�����мס��������ǵ��ʣ��ҡ����ͼ�����������ж��������������Ϊ�������������Ϻ�ɫ��������Ϊͭ�����ݿ�ͼ����Ϊ������Ϊ����ͭ����Ϊ��������Ϊˮ�����B��C��D�ֱ�ΪO��Al��Cu��
(1)DΪCu��CΪAl�������ڱ���λ�ڵ������ڢ�A�壬�ʴ�Ϊ��Cu���������ڢ�A�壻
(2)ˮΪ���ۻ�����õ���ʽ��ʾˮ���γɹ���Ϊ![]() ���ʴ�Ϊ��
���ʴ�Ϊ��![]() ��
��
(3)��Ӧ������������ͭ���������ȷ�Ӧ���ʴ�Ϊ�����ȣ�
(4)����ͭ��Ũ������γ�ԭ��أ�����Ũ���ᷢ���ۻ���ͭ���ױ�Ũ�����������ܽ⣬���ͭ���������缫��ӦʽΪCu -2e����Cu2���������������ܷ�ӦΪCu+4H++2NO3-=Cu2+ +2NO2��+2H2O����������ĵ缫��ӦʽΪNO3-+e-+2H+=NO2��+H2O���ʴ�Ϊ��Cu��NO3-+e-+2H+=NO2��+H2O��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ȥ�����е��������ۣ���ѡ��(����)
A. ���� B. ˮ C. ���� D. ����������Һ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ֶ�����Ԫ��ԭ�Ӱ뾶����Դ�С��������ۻ��������ԭ�������ı仯��ϵ��ͼ��ʾ������˵����ȷ����
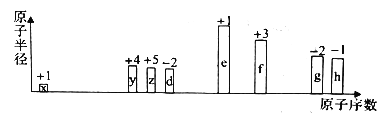
A. ���Ӱ뾶�Ĵ�С˳����d
B. ��x�γɼ�����ķе���y>z>d
C. ��ȥʵ����Թ��в�����g���ʣ������ȵ�����������Һ
D. g��h���������Ӧ��ˮ��������ԣ�h>g
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ӹ�ҵ�У������Ȼ�����Һ��Ϊӡˢ��·ͭ��ʴ��Һ���밴Ҫ��ش��������⣺
��1�������Ȼ�����Һ�м���һ�����ij���ʯ��ˮ��������ҺpH���ɵú��ɫ����,�÷�Ӧ�����ӷ���ʽΪ��______________________________________���ù����е�����Һ��pHΪ5����c(Fe����)Ϊ��____________mol��L��1������֪��Ksp[Fe(OH)3]= 4.0��10-38��
��2��ij̽��С�����������·������Һ����Դ���գ�
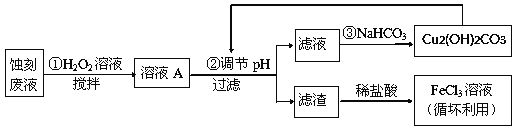
��������FeCl3��Һʴ��ͭ���ķ�Һ�к��еĽ����������У�_______________��
��FeCl3ʴ��Һ��ͨ������һ���������ᣬ���м��������Ŀ���ǣ�_________________��
�۲�����м���H2O2��Һ��Ŀ���ǣ�______________________________________��
����֪�������������������pH
Cu(OH)2 | Fe(OH)2 | Fe(OH)3 | |
��ʼ����ʱ | 4.7 | 7.0 | 1.9 |
������ȫʱ | 6.7 | 9.0 | 3.2 |
���ݱ��������Ʋ����pH�ķ�Χ�ǣ�________________��
��д�������������CO2�����ӷ���ʽ��__________����֪Cu2(OH)2CO3������ˮ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ʵ���Ũ�Ⱦ�Ϊ0.100mol/L���������ʵ���Һ�У�c��NH4+�������ǣ� ��
A.NH4ClB.NH4HSO4C.NH3��H2OD.CH3COONH4
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й����л����˵����ȷ����( )
A.����ϩ�ɷ����ӳɷ�Ӧ
B.ʯ����ɵõ����͡�ú�͵�
C.����ķе���ڱ���
D.������ʹ���Ը��������Һ��ɫ�����Ա����ܷ���������Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�о���ѧϰС��Ϊ����֤CH4�Ƿ���л�ԭ�ԣ����������ʵ�飺
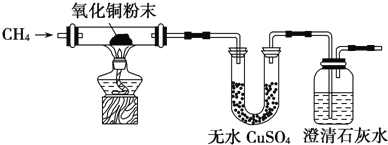
��1��ʵ������й۲쵽��ˮCuSO4����������ʯ��ˮ���ֻ���������CH4��CuO��Ӧ�Ļ�ѧ����ʽΪ________________________________��
��2���о�С�齫CH4ͨ����ˮʱ��������ˮ����ɫ������Ϊԭ�������___________________�������һ��ʵ�鷽��֤����Ľ��ۣ������ֱ�ʾ�����ػ�ʵ��װ��ͼ��_______________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ݷ�Ӧ3Cu+8HNO3��ϡ��=3Cu��NO3��2+2NO��+4H2O���ش��������⣺
��1����ԭ������
��2���������뻹ԭ�������ʵ���֮����
��3����˫���ű��ϵ���ת�Ƶķ������Ŀ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��300mL Al2��SO4��3��Һ�У���Al3+Ϊ1.62g���ڸ���Һ�м���0.1mol/L Ba��OH��2��Һ300mL����Ӧ����Һ��SO42�������ʵ�����Ũ��Ϊ�� ����������������Һ�����֮�ͣ�
A.0.4mol/L
B.0.3mol/L
C.0.2mol/L
D.0.1mol/L
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com