
| A. | ①②⑤ | B. | ②③⑥ | C. | ②③④⑤ | D. | ②④ |
分析 Fe过量,为了减缓反应速率,且不影响生成氢气的总量,可减小氢离子的浓度,但不能改变氢离子的物质的量,以此来解答.
解答 解:①加NaOH固体,与盐酸反应,生成氢气减少,故错误;
②Na2SO4不参加反应,溶液体积增大,浓度减小,则反应速率减小,但生成氢气的总量不变,故正确;
③在酸性条件下硝酸根离子具有强氧化性,与铁反应生成NO,故错误;
④加H2O,减小氢离子浓度,不能改变氢离子的物质的量,故正确;
⑤加入CaCO3固体,消耗H+,生成氢气的总量较少,故错误;
⑥加入NaCl固体,溶液浓度不变,反应速率不变,故错误.
故选D.
点评 本题考查影响反应速率的因素,为高考常考考点,注意Fe过量,生成氢气由盐酸决定,把握浓度对反应速率的影响即可解答,题目难度不大.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:推断题
 某烃A是有机化学工业的基本原料,其产量可以用来衡量一个国家的石油化工发展水平,A可发生如图所示的一系列化学反应.据图回答下列问题:
某烃A是有机化学工业的基本原料,其产量可以用来衡量一个国家的石油化工发展水平,A可发生如图所示的一系列化学反应.据图回答下列问题: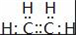 ,D中官能团的名称是羟基.
,D中官能团的名称是羟基.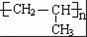 .
.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| 周期/族 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | ○ |
| 2 | ① | ② | ③ | ④ | ||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ | ⑪ | ⑫ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氢键 分子间作用力 非极性键 | |
| B. | 氢键 极性键 分子间作用力 | |
| C. | 氢键 氢键 极性键 | |
| D. | 分子间作用力 氢键 非极性键 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 与等体积、pH=3的盐酸比较,跟足量锌粒反应产生的H2更少 | |
| B. | 加水稀释到原体积的10倍后溶液pH变为4 | |
| C. | 加入少量乙酸钠固体,溶液pH升高 | |
| D. | 升高温度,溶液中所有离子浓度均增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
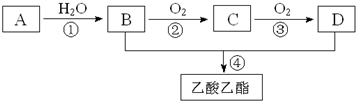
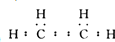 ,其空间构型平面形.
,其空间构型平面形.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com