
某气态烃A在标准状况下的密度为1.25g/L,其产量可以用来衡量一个国家的石油化工发展水平。B和D都是生活中常见的有机物,D能跟碳酸氢钠反应,F有香味。它们之间的转化关系如下图所示:
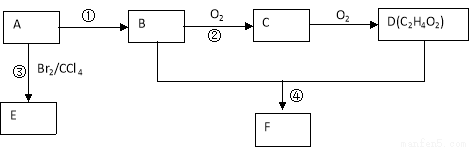
(1)A的结构式为 , D中官能团的名称为 。
(2)反应①的反应类型是 ,反应③的化学方程式为 。
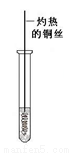
(3)反应②在Cu做催化剂的条件下进行,该实验的步骤是将红亮的铜丝置于酒精灯上加热,待铜丝变为黑色时,迅速将其插入到装有B的试管中(如右上图所示)。重复操作2-3次,观察到的现象是__________。该反应的化学方程式为 。
(4)D与碳酸氢钠溶液反应的离子方程式为 。
(5)B、D在浓硫酸的作用下实现反应④,实验装置如右图所示:
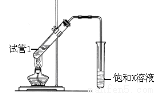
图中X的化学式为_________。浓硫酸的作用是 。
试管Ⅰ中在加热前应加_______,防止液体暴沸。导管末端为伸入小试管液面下的原因是__________。该反应的化学方程式为 。分离产物F的方法是__________。
 课前课后同步练习系列答案
课前课后同步练习系列答案 课堂小作业系列答案
课堂小作业系列答案 黄冈小状元口算速算练习册系列答案
黄冈小状元口算速算练习册系列答案 成功训练计划系列答案
成功训练计划系列答案 倍速训练法直通中考考点系列答案
倍速训练法直通中考考点系列答案科目:高中化学 来源:2017届湖南省高三上8月单元测化学试卷(解析版) 题型:选择题
下列说法正确的是
A.按系统命名法,有机物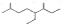 的名称为3,7—二甲基—4—乙基辛烷
的名称为3,7—二甲基—4—乙基辛烷
B.高聚物脲醛树脂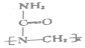 的合成单体之一是
的合成单体之一是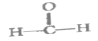
C.1mol葡萄糖能水解生成2molCH3CH2OH和2molCO2
D.在酸性条件下,CH3CO18OC2H5的水解产物是CH3CO18OH和C2H5OH
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河南省五岳八校高一下期末联考化学试卷(解析版) 题型:选择题
硫代硫酸钠溶液与稀硫酸反应的化学方程式为: Na2S203+H2S04=Na2S04+S02+S↓+H20,下列各组实验中最先出现浑浊的是( )
实验 | 反应温度℃ | Na2SO4 | Na2S2O3 溶液 | 稀 H2SO4 | H2O | |
V/mL | c/ (moL-L-1) | V/mL | d (moL-L-1) | V/mL | ||
A | 25 | 5 — | 0.1 | 10 | 0.1 | 5 |
B | 25 | 5 | 0.2 | 5 | 0.2 | 10 |
C | 35 | 5 | 0.1 | 10 | 0.1 | 5 |
D | 35 | 5 | 0.2 | 5 | 0.2 | 10 |
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河南省五岳八校高二下期末联考化学试卷(解析版) 题型:选择题
下列关于同温、同压下的两种气体12C18O和14N2的判断正确的是( )
A.体积相等时密度相等 B.原子数相等时具有的中子数相等
C.体积相等时具有的电子数相等 D.质量相等时具有的质子数相等
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河南省五岳八校高二下期末联考化学试卷(解析版) 题型:选择题
头孢克洛是人工合成的第二代口服头孢菌抗生素,主要用于呼吸道感染、中耳炎、尿道感染等疾病的治疗,其结构如图所示,下列关于头孢克洛的说法不正确的是( )
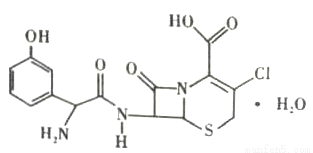
A.分子式可以表示为C15H16C1N3O6S
B.既能和盐酸反应又能和烧碱溶液反应
C.分子结构中有3个手性碳原子
D.1mol该化合物与NaOH溶液作用时消耗NaOH的物质的量最多为4mol
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河北省唐山市高一下期末化学试卷(解析版) 题型:选择题
X、Y、Z、M是元素周期表中前20号元素,其原子序数依次增大。X原子的最外层电子数是其内层电子总数的3倍,Y原子的最外层电子数与其电子层数相等,Z-与M2+具有相同的核外电子层结构。下列推测正确的是
A. 原子半径Y>Z,离子半径Z-<M2+
B. MX2与水发生反应时,MX2只做氧化剂
C. X、Y形成的化合物既能与强酸反应又能与强碱反应
D. MX2、MZ2两种化合物中,阳离子与阴离子个数比均为1:2
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河北省唐山市高一下期末化学试卷(解析版) 题型:选择题
已知反应:X+Y=M+N为放热反应,则下列说法正确的是
A.断裂X和Y的化学键所吸收的能量一定高于形成M和N的化学键所放出的能量
B.X和Y的总能量一定高于M和N的总能量
C.Y的能量一定高于N
D.因为该反应为放热反应,故不必加热就可发生
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河北省唐山市高二下期末化学试卷(解析版) 题型:填空题
甲、乙、丙三位同学按下列方法制取氢氧化铝,请你参与并回答有关问题。
甲:用可溶性铝盐与稀氨水反应制取氢氧化铝。写出该反应的离子方程式: 。
乙:根据右图电解装置制取氢氧化铝。请回答:
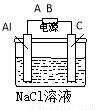
(1) 电源中A极是 极,铝极的电极反应式为 ;
(2)从原理分析,电解质NaCl的作用是 。
丙:利用铝屑、稀H2SO4、NaOH溶液为主要原料制取Al(OH)3固体。
(1)先设计了如下三种方案:
Ⅰ Al3+→Al(OH)3
Ⅱ Al→AlO2-→Al(OH)3
Ⅲ 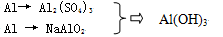
从节省原料的角度分析,你认为最合理的方案是 。(填Ⅰ、Ⅱ或Ⅲ)
(2)设计了如下实验步骤:
①配制500 mL 0.5 mol•L-1NaOH溶液所用到的仪器有:托盘天平(含砝码)、烧杯、玻璃棒、 ;
②在烧杯A中加入50 mL 0.5 mol•L-1NaOH溶液,再加入足量铝屑给溶液稍加热。其作用是 ,用蒸馏水把铝屑冲洗,干燥后称其质量为m1 g(全部用于制氢氧化铝);
③在盛有适量稀H2SO4的烧杯B中放入 g(含m1的式子表示)铝屑,充分搅拌使铝屑反应完全;
④在盛有适量浓NaOH溶液的烧杯C中入一定质量的铝屑,充分搅拌使铝屑反应完全。该反应的化学方程式为 ;
⑤将烧杯B和烧杯C中的溶液混合,得到氢氧化铝白色沉淀;
⑥将沉淀过滤、洗涤、干燥得Al(OH)3固体m2 g。
试计算此实验中Al(OH)3的产率是 。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河南省周口市高二下期末化学试卷(解析版) 题型:实验题
【化学选修2 -化学与技未】
I.某含锰矿物的主要成分有MnCO3、MnO2、FeCO3、SiO2 、A12O3等。已知FeCO3、MnCO3难溶于水。一种运用阴离子膜电解法的新技术可用于从碳酸锰矿中提取金属锰,主要物质转化关系如下:
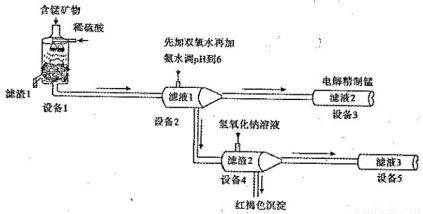
(1)设备Ⅰ中反应后,滤液1里锰元素只以Mn2+的形式存在,且滤渣1中也无MnO2。 滤渣1的主要成分是 (填化学式)。
(2)设备1中发生氧化还原反应的离子方程式是 。
(3)设备2中加足量双氧水的作用是 。设计实验方案检验滤液2中是否存在Fe2+: 。
(4)设备4中加入过量氢氧化钠溶液,沉淀部分溶解,用化学平衡移动原理解释原因: 。
(5)设备3中用阴离子膜法提取金属锰的电解装置如图:
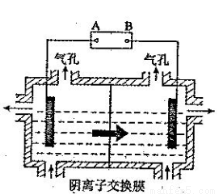
①电解装置中箭头表示溶液中阴离子移动的方向;则A电极是直流电源的 极。实际生产中,阳极以稀硫酸为电解液,阳极的电极反应式为__ ___。
②该工艺之所以采用阴离子交换膜,是为了防止Mn2+ 进入阳极区发生副反应生成MnO2造成资源浪费,写出该副反应的电极反应式 。
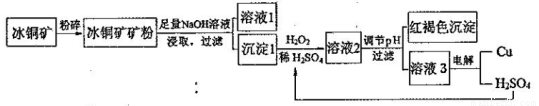
II.冰铜矿的主要成分是Cu2S、FeS,含有少许Al2O3和SiO2杂质。由冰铜矿冶炼金属铜的流程如下:
已知各离子沉淀的范围如下表
离子 | Fe3+ | Fe2 + | Cu2+ |
开始沉淀pH | 1.9 | 7.0 | 6.7 |
沉淀完全pH | 3.4 | 9.0 | 10.0 |
请回答下列问题:
(1)将冰铜矿粉碎的目的是提高浸出率,另外一种提高浸出率的措施是 。
(2)溶液1的成分是 ,若向其中通入足量的CO2可以析出的沉淀是 ,此时溶液中的溶质将变成 。
(3)沉淀1加入H2O2和稀H2SO4后,溶液中阴离子只有SO42-,金属阳离子有Cu2+ 和F3+,则该过程的离子方程式为: 。
(4)溶液2调节的pH范围为 。
(5)对红褐色沉淀进行洗涤并干燥处理,可以得到纯净的Fe(OH)3,可用于制备红色颜料Fe2O3。检验红褐色沉淀是否洗净的方法是 。
(6)用惰性电极对溶液3进行电解,电解CuSO4溶液的化学方程式为: ;当两极共产生标准状况下44.8 L气体且阴阳两极产生的气体体积之比为1: 1时,则析出的铜的质量为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com