
| A. | CaO+H2O═Ca(OH)2,可以放出大量的热,故可把该反应设计成原电池,把其中的化学能转化为电能 | |
| B. | 其他条件均相同,带有“盐桥”的原电池比不带“盐桥”的原电池电流持续时间长 | |
| C. | 原电池工作时,正极表面一定有气泡产生 | |
| D. | 钢铁水闸可用牺牲阴极或外加电流的阳极保护法防止其腐蚀 |
分析 A、只有自发进行的、放热的氧化还原反应才能设计成原电池;
B、有盐桥的原电池可以保证电解质溶液中持续的离子的定向移动;
C、在原电池的正极上放电的是电解质溶液中的阳离子;
D、在原电池中正极被保护,在电解池中阴极被保护.
解答 解:A、只有自发进行的、放热的氧化还原反应才能设计成原电池,由于此反应不是氧化还原反应,故不能设计成原电池,故A错误;
B、当没有盐桥时,电解质溶液中的离子移动只能持续较短的时间,而有盐桥的原电池可以保证电解质溶液中持续的离子的定向移动,故带有盐桥的原电池电流持续的时间更长,故B正确;
C、在原电池的正极上放电的是电解质溶液中的阳离子,而可能是氢离子,也可能是金属阳离子,故不一定是气泡生成,故C错误;
D、在原电池中正极被保护,即牺牲阳极的阴极保护法;在电解池中阴极被保护,即外加电流的阴极保护法,故D错误.
故选B.
点评 本题考查了原电池的工作原理以及金属的腐蚀和防护原理,难度不大,应注意的是只有自发进行的、放热的氧化还原反应才能设计成原电池.


科目:高中化学 来源: 题型:推断题
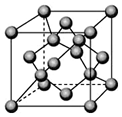 已知A、B、C、D都是元素周期表中前36号的元素.A元素的一种核素没有中子.B的基态原子核外电子有9种不同的运动状态;C元素是无机非金属材料的主角,它的单质可以用作电脑芯片;D元素是地壳中含量第二的金属元素.请回答:
已知A、B、C、D都是元素周期表中前36号的元素.A元素的一种核素没有中子.B的基态原子核外电子有9种不同的运动状态;C元素是无机非金属材料的主角,它的单质可以用作电脑芯片;D元素是地壳中含量第二的金属元素.请回答:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
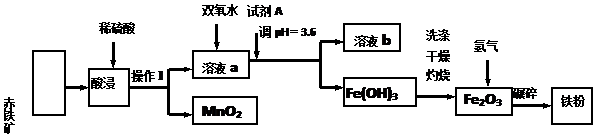
| 沉淀物 | Fe(OH)3 | Al(OH)3 | Fe (OH)2 | Cu (OH)2 |
| pH | 3.4 | 5.2 | 9.7 | 6.7 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | pH相同的①NH4Cl②NH4Al(SO4)3③NH4HSO3,三种溶液中的c(NH4+):①<②<③ | |
| B. | 20mL0.1mol/L的CH3COONa溶液与10mL0.1mol/L的HCl溶液混合后呈酸性,所得溶液中:c(CH3COO-)>c(Cl-)>c(CH4COOH)>c(H+) | |
| C. | 0.1mol/L的NaHCO3溶液与0.1mol/L的NaOH溶液等体积混合,所得溶液中:c(Na+)>c(CO32-)>c(HCO3-)>c(OH-) | |
| D. | 常温下,pH=7的NH4Cl与氨水的混合溶液中:c(Cl-)>c(NH4+)>c(H+)=c(OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na2SO4、BaC12、K2CO3、KNO3 | B. | HC1、NaNO3、Na2CO3、(NH4)2SO4 | ||
| C. | NaOH、KC1、K2CO3、MgCl2 | D. | NaAlO2、NaC1、Na2CO3、AgNO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 稀释溶液,$\frac{c(HC{O}_{3}^{-}C)•c(O{H}^{-})}{c(C{O}_{3}^{2-})}$不变 | |
| B. | 通入CO2,溶液pH增大 | |
| C. | 升高温度,平衡常数减小 | |
| D. | 加入NaOH固体,$\frac{c(HC{O}_{3}^{-})}{c(C{O}_{3}^{2-})}$增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 足量的CO2和水蒸气的混合气体与少量的Na2O2充分反应,最终必生成NaOH | |
| B. | 足量的MnO2与含4molHCl的浓盐酸加热充分反应,产生的Cl2必为1mol | |
| C. | 含2molHCl的某盐酸滴入足量的碳酸钠溶液中充分反应后,得到CO2气体必为1mol | |
| D. | 过量的二氧化碳通入偏铝酸钠溶液中,最终生成的产物必为Al(OH)2和碳酸氢钠 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com