
| 1 |
| 3 |
| 4a-3b |
| 3 |
| ||
| 0.5L |
| 4a-6b |
| 3 |
| 4a-6b |
| 3 |


 活力课时同步练习册系列答案
活力课时同步练习册系列答案科目:高中化学 来源: 题型:
| A、①②⑤⑦ | B、④⑤⑦ |
| C、③④⑥ | D、⑤⑥⑦ |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
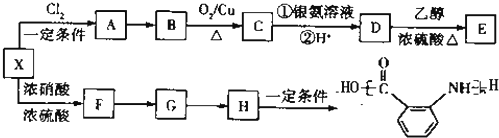
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、NaCl、Na2SO4 |
| B、NaCl、NaBr、Na2SO4 |
| C、NaCl、Na2SO4、I2 |
| D、NaCl、NaI、Na2SO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、C2H6与氯气发生取代反应、C2H4与HCl发生加成反应均可得到纯净的C2H5Cl |
| B、将甲烷和乙烯的混合气体通过盛有浓溴水的洗气瓶,即可提纯甲烷 |
| C、乙烯结构中含有碳碳双键,苯中不含有碳碳双键,但两者均可以发生加成反应 |
| D、苯使酸性KMn04溶液、溴水都褪色,发生的都是氧化反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 某探究小组用测量HNO3与大理石反应过程中质量减小的方法,研究影响反应速率的因素.限选试剂:1.00mol?L-1 HNO3、2.00mol?L-1HNO3,细颗粒大理石、粗颗粒大理石,35℃水浴.
某探究小组用测量HNO3与大理石反应过程中质量减小的方法,研究影响反应速率的因素.限选试剂:1.00mol?L-1 HNO3、2.00mol?L-1HNO3,细颗粒大理石、粗颗粒大理石,35℃水浴.| 实验编号 | T/℃ | 大理石规格 | HNO3浓度/mol?L-1 |
| ① | 常温 | 粗颗粒 | 2.00 |
| ② | 常温 | 1.00 | |
| ③ | 粗颗粒 | 2.00 | |
| ④ | 2.00 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com